
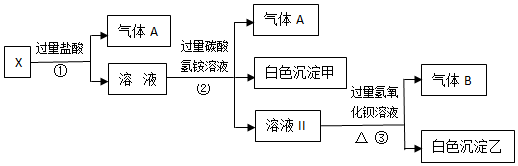
分析 溶液呈无色,则不含Fe3+,加入过量盐酸只产生气体,则一定含有CO32-,不含Ag+,反应后溶液呈酸性,加入过量碳酸氢铵溶液,生成气体和白色沉淀,则发生反应应为:Al3++3HCO3-═Al(OH)3↓+3CO2↑,则原溶液中含有AlO2-,则一定不含Ba2+、Al3+、Fe3+,因这些离子与AlO2-发生相互促进的水解而不能大量共存,根据溶液电中性原则,一定含有Na+,最后加入过量氢氧化钡溶液,因之前加入的碳酸氢铵过量,则生成的白色沉淀可能为BaCO3,不能确定SO42-是否存在,以此来解答.
解答 解:(1)气体A的成分是CO2,所涉及反应有:CO32-+2H+═H2O+CO2↑,Al3++3HCO3-═Al(OH)3↓+3CO2↑,气体B为NH3,所涉及反应为:NH4++OH-=NH3↑+H2O,故答案为:CO2;NH3;
(2)步骤①发生反应的所有离子方程式为CO32-+2H+═H2O+CO2↑、AlO2-+4H+═Al3++2H2O,故答案为:CO32-+2H+═H2O+CO2↑、AlO2-+4H+═Al3++2H2O;
(3)溶液中含有AlO2-,加入过量盐酸发生反应:AlO2-+4H+═Al3++2H2O,加入过量碳酸氢铵溶液,生成气体和白色沉淀,则步骤②形成白色沉淀甲的离子方程式为Al3++3HCO3-═Al(OH)3↓+3CO2↑,故答案为:Al3++3HCO3-═Al(OH)3↓+3CO2↑;
(4)由以上分析可知,X溶液中一定存在的离子是CO32-,AlO2-,Na+,因最后加入过量氢氧化钡溶液,因之前加入的碳酸氢铵过量,则生成的白色沉淀可能为BaCO3,不能确定SO42-是否存在,可向所得沉淀乙中滴加足量的稀硝酸,若沉淀不完全溶解,则证明含有SO42-,
故答案为:CO32-、AlO2-、Na+;SO42-;向所得沉淀乙中滴加足量的稀硝酸,若沉淀不完全溶解,则证明含有SO42-.
点评 本题考查无机物的推断,为高频考点,把握离子的性质、发生的反应为解答的关键,侧重分析与推断能力的考查,注意沉淀的判断及元素化合物知识的应用,题目难度不大.


 名师指导一卷通系列答案
名师指导一卷通系列答案科目:高中化学 来源: 题型:选择题
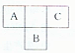 短周期元素A、B、C,在周期表中所处的位置如图所示、A、B、C三种元素原子质子数之和为32.D元素原子的最外层电子数为其次外层电子数的2倍.则下列说法正确的是( )
短周期元素A、B、C,在周期表中所处的位置如图所示、A、B、C三种元素原子质子数之和为32.D元素原子的最外层电子数为其次外层电子数的2倍.则下列说法正确的是( )| A. | A、B两种元素的气态氢化物均能与它们对应的最高价氧化物对应的水化物发生反应,且反应类型相同 | |
| B. | A的气态氢化物比B的气态氢化物稳定,是由于A的氢化物分子间有氢键 | |
| C. | 元素D形成的气态氢化物一定是正四面体型分子 | |
| D. | 四种元素的原子半径:B>D>A>C |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
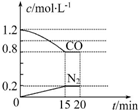 “霾”是当今世界环境热点话题.某地空气质量恶化原因之一是机动车尾气和燃煤产生的烟气.NO和CO气体均为汽车尾气的成分,这两种气体在催化转换器中发生如下反应:
“霾”是当今世界环境热点话题.某地空气质量恶化原因之一是机动车尾气和燃煤产生的烟气.NO和CO气体均为汽车尾气的成分,这两种气体在催化转换器中发生如下反应:查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | ①⑤⑥ | B. | ④⑥ | C. | ②④⑦ | D. | ③④⑧ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | H2CO3═2H++CO32- | B. | NaHSO4═Na++HSO4- | ||
| C. | NaHCO3?Na++HCO3- | D. | Ba(OH)2═Ba2++2OH- |
查看答案和解析>>
科目:高中化学 来源: 题型:推断题
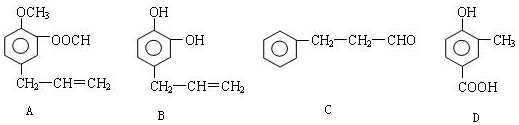
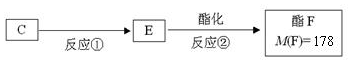
 .
.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 2.3 g | B. | 3.45 g | C. | 1.15 g | D. | 0.575 g |
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
| 砝码质量/g | 50 | 20 | 20 | 10 | 5 |
| 称量(取用砝码过程) |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 硫酸、纯碱、醋酸钠和生石灰分别属于酸、碱、盐和氧化物 | |
| B. | 酒精、硫酸钡和水分别属于电解质、强电解质和弱电解质 | |
| C. | 胶体区别于其它分散系的本质特性是具有丁达尔现象 | |
| D. | 利用半透膜可除去淀粉溶液中的少量NaCl |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com