

分析 根据图中各物质转化关系,A为固态单质,常温下C、E、F都是无色气体,则A与B的反应应为碳与浓酸硫或浓硝酸的反应,E能与黄绿色溶液(应为氯水)反应,生成I遇氯化钡有白色沉淀,则I中应含有硫酸根,I为H2SO4,H为HCl,所以A与B的反应为碳与浓硫酸的反应,A为C,B为浓H2SO4,E为SO2,D为H2O,C是气体能与淡黄色固体反应,则应为二氧化碳与过氧化钠的反应,所以C为CO2,F为O2,G为Na2CO3,HCl与Na2CO3反应生成二氧化碳、氯化钠和水,符合各物质转化关系,据此答题.
解答 解:根据图中各物质转化关系,A为固态单质,常温下C、E、F都是无色气体,则A与B的反应应为碳与浓酸硫或浓硝酸的反应,E能与黄绿色溶液(应为氯水)反应,生成I遇氯化钡有白色沉淀,则I中应含有硫酸根,I为H2SO4,H为HCl,所以A与B的反应为碳与浓硫酸的反应,A为C,B为浓H2SO4,E为SO2,D为H2O,C是气体能与淡黄色固体反应,则应为二氧化碳与过氧化钠的反应,所以C为CO2,F为O2,G为Na2CO3,HCl与Na2CO3反应生成二氧化碳、氯化钠和水,符合各物质转化关系,
(1)根据上面的分析可知,C为二氧化碳,二氧化碳的固体名称为干冰,F为O2,
故答案为:干冰;O2;
(2)A与B反应的化学方程式是C+2H2SO4(浓)$\frac{\underline{\;\;△\;\;}}{\;}$2SO2↑+CO2↑+2H2O,
故答案为:C+2H2SO4(浓)$\frac{\underline{\;\;△\;\;}}{\;}$2SO2↑+CO2↑+2H2O;
(3)G为Na2CO3,H为HCl,反应的离子方程式为:CO32-+2H+=CO2↑+H2O,E转变为H和I的离子方程式是SO2+Cl2+2H2O═4H++2Cl-+SO42-,
故答案为:CO32-+2H+=CO2↑+H2O;SO2+Cl2+2H2O═4H++2Cl-+SO42-.
点评 本题考查无机物的推断,题目难度中等,物质的颜色为解答该题的突破口,注意把握反应的转化关系的重要信息,侧重于学生分析能力的考查,注意相关知识的学习


 黄冈天天练口算题卡系列答案
黄冈天天练口算题卡系列答案科目:高中化学 来源: 题型:选择题
| A. | 配制FeCl2和烧碱溶液所用的蒸馏水通常要煮沸 | |
| B. | 可在FeCl2溶液的上面加一层苯,以隔绝空气 | |
| C. | 向FeCl2溶液中滴加烧碱溶液时,胶头滴管尖嘴不能伸入到试管内 | |
| D. | 产生Fe(OH)2沉淀后,不能震荡试管 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题

查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 某学习小组为证明并观察铜与稀HNO3反应的产物是NO,设计了如图1所示的实验装置.请你根据他们的思路,回答有关的问题.
某学习小组为证明并观察铜与稀HNO3反应的产物是NO,设计了如图1所示的实验装置.请你根据他们的思路,回答有关的问题.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
 如图把锌片和铜片用导线相连后插入稀硫酸溶液构成原电池.某实验兴趣小组做完实验后,在读书卡上的记录如下所示,则卡片上的描述合理的是( )
如图把锌片和铜片用导线相连后插入稀硫酸溶液构成原电池.某实验兴趣小组做完实验后,在读书卡上的记录如下所示,则卡片上的描述合理的是( )| A. | ①②③ | B. | ②④ | C. | ④⑤⑥ | D. | ③④⑤ |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题

查看答案和解析>>
科目:高中化学 来源: 题型:选择题

| A. | 六星烷的化学式为C18H24 | |
| B. | 它们之间互为同系物 | |
| C. | 三星烷与丙苯互为同分异构体,四星烷与 互为同分异构体 互为同分异构体 | |
| D. | 星烷的一氯代物均只有2种,而三星烷的二氯代物有4种 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 金属氧化物 过氧化钠 Na2O | B. | 酸 硫酸 H2SO4 | ||
| C. | 盐 苛性钠 NaOH | D. | 碱 纯碱 Na2CO3 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
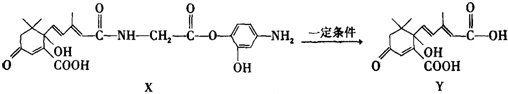
| A. | 1mol X与足量NaOH溶液反应,最多消耗4mol NaOH | |
| B. | Y既可以与FeCl3溶液发生显色反应,又可使酸性KMnO4溶液褪色 | |
| C. | X可以发生氧化、取代、酯化、加聚、缩聚反应,并能与盐酸反应生成有机盐 | |
| D. | X结构中有2个手性碳原子 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com