
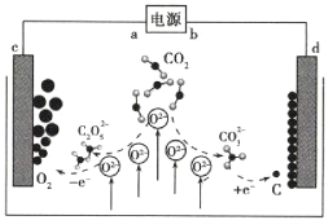
【题目】《Journal of Energy Chemistry》报道我国科学家设计![]() 熔盐捕获与转化装置如图。下列有关说法正确的是( )
熔盐捕获与转化装置如图。下列有关说法正确的是( )
A.![]() 为负极
为负极
B.熔盐可用![]() 溶液代替
溶液代替
C.转移![]() 电子可捕获
电子可捕获![]() (标准状况下)
(标准状况下)
D.![]() 的电极反应式为
的电极反应式为![]()
【答案】D
【解析】
根据装置图可知,熔盐捕获CO2生成的C2O![]() 在c极发生氧化反应生成单质O2,所以c为阳极,相应的反应为2CO2+O2-= C2O
在c极发生氧化反应生成单质O2,所以c为阳极,相应的反应为2CO2+O2-= C2O![]() 、2 C2O
、2 C2O![]() -4e-=4CO2+O2;熔盐捕获CO2生成的CO32-在d极发生得电子的还原反应生成C,d为阴极,相应的反应为CO2+O2-= CO
-4e-=4CO2+O2;熔盐捕获CO2生成的CO32-在d极发生得电子的还原反应生成C,d为阴极,相应的反应为CO2+O2-= CO![]() 、CO
、CO![]() +4e-=C+3O2-;总反应为CO2
+4e-=C+3O2-;总反应为CO2![]() C+O2,熔盐在电解前后不变,可连续使用;阳极与电源正极相接、阴极与电源负极相接,即a极为电源正极、b极为电源负极。
C+O2,熔盐在电解前后不变,可连续使用;阳极与电源正极相接、阴极与电源负极相接,即a极为电源正极、b极为电源负极。
A.c极电极反应是2C2O![]() -4e-═4CO2+O2,发生氧化反应,是电解池的阳极,则a为正极,故A错误;
-4e-═4CO2+O2,发生氧化反应,是电解池的阳极,则a为正极,故A错误;
B.如果用氢氧化钾溶液代替熔盐,KOH溶液捕获二氧化碳生成K2CO3或KHCO3,c极是氢氧根离子放电,d极是氢离子放电,本质上电解水,KOH被消耗完后不能捕获更多的CO2,不能连续使用,所以熔盐不可用KOH溶液代替,故B错误;
C.由总反应为CO2![]() C+O2可知,转移4mol的电子捕获1mol二氧化碳,转移lmol电子可捕获CO25.6L(标况下),故C错误;
C+O2可知,转移4mol的电子捕获1mol二氧化碳,转移lmol电子可捕获CO25.6L(标况下),故C错误;
D.d极是电解池的阴极,发生还原反应生成单质碳,电极反应式为:CO![]() +4e-=C+3O2-,故D正确;
+4e-=C+3O2-,故D正确;
故选D。


科目:高中化学 来源: 题型:
【题目】汽车尾气里含有的NO气体是由于内燃机燃烧的高温引起氮气和氧气反应所致:
N2(g)+O2(g)![]() 2NO(g),△H>0,已知该反应在240℃,平衡常数K=64×10-4。请回答:
2NO(g),△H>0,已知该反应在240℃,平衡常数K=64×10-4。请回答:
(1)某温度下,向2L的密闭容器中充入N2和O2各1mol,5分钟后O2的物质的量为0.5mol,则N2的反应速率为______。
(2)假定该反应是在恒容条件下进行,判断该反应达到平衡的标志______.
A.消耗1molN2同时生成1molO2![]() 混合气体密度不变
混合气体密度不变
C.混合气体平均相对分子质量不变D.2v正(N2)=v逆(NO)
(3)将N2、O2的混合气体充入恒温恒容密闭容器中,如图变化趋势正确的是______(填字母序号)。

(4)向恒温恒容的密闭容器中充入等物质的量的N2和O2,达到平衡状态后再向其中充入一定量NO,重新达到化学平衡状态![]() 与原平衡状态相比,此时平衡混合气中NO的体积分数______
与原平衡状态相比,此时平衡混合气中NO的体积分数______![]() 填“变大”、“变小”或“不变”
填“变大”、“变小”或“不变”![]()
(5)该温度下,某时刻测得容器内N2、O2、NO的浓度分别为2.5×10-1mol/L、4.0×10-2mol/L和3.0×10-3mol/L,此时反应______(填“处于化学平衡状态”、“向正反应方向进行”或“向逆反应方向进行”),理由是______。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(1)反应Fe(s)+CO2(g) ![]() FeO(s)+CO(g),平衡常数为K1;反应Fe(s)+H2O(g)
FeO(s)+CO(g),平衡常数为K1;反应Fe(s)+H2O(g) ![]() FeO(s)+H2(g),平衡常数为K2。在不同温度时K1、K2的值如表:
FeO(s)+H2(g),平衡常数为K2。在不同温度时K1、K2的值如表:
700℃ | 900℃ | |
K1 | 1.47 | 2.15 |
K2 | 2.38 | 1.67 |
反应CO2(g)+H2(g) ![]() CO(g)+H2O(g),平衡常数K,则K=___(用K1和K2表示),且由上述计算可知,反应CO2(g)+H2(g)
CO(g)+H2O(g),平衡常数K,则K=___(用K1和K2表示),且由上述计算可知,反应CO2(g)+H2(g) ![]() CO(g)+H2O(g)是___反应(填“吸热”或“放热”)。
CO(g)+H2O(g)是___反应(填“吸热”或“放热”)。
(2)一定温度下,向某密闭容器中加入足量铁粉并充入一定量的CO2气体,发生反应Fe(s)+CO2(g) ![]() FeO(s)+CO(g) ΔH>0,CO2的浓度与时间的关系如图所示:
FeO(s)+CO(g) ΔH>0,CO2的浓度与时间的关系如图所示:
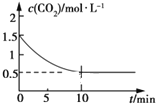
①该条件下反应的平衡常数为___;若铁粉足量,CO2的起始浓度为2.0 mol·L-1,则平衡时CO2的浓度为___mol·L-1。
②下列措施中能使平衡时![]() 增大的是___(填序号)。
增大的是___(填序号)。
A.升高温度 B.增大压强
C.再充入一定量的CO2 D.再加入一定量铁粉
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】化学上常用燃烧法确定有机物的组成。如图所示装置是用燃烧法确定烃或烃的含氧衍生物分子式的常用装置,这种方法是在电炉加热时用纯氧氧化管内样品,根据产物的质量确定有机物的组成。
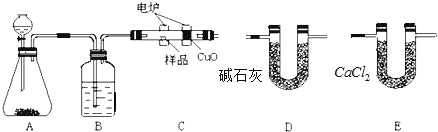
回答下列问题:
(1)若A中装有二氧化锰固体,发生反应的化学方程式为_____。
(2)B装置的作用是_____,燃烧管C中CuO的作用是_____。
(3)产生氧气按从左向右流向,燃烧管C与装置D、E的连接顺序是:C→____→____。
(4)准确称取1.8g 烃的含氧衍生物X 的样品,经充分燃烧后,D管质量增加2.64g,E管质量增加1.08g,则该有机物的实验式(即最简式)是____,实验测得X的蒸气密度是同温同压下氢气密度的45倍,则X的分子式为_____,1molX分别与足量Na、NaHCO3反应放出的气体在相同条件下的体积比为1:1,X可能的结构简式为_____(任写一种合理结构)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某小组同学欲探究NH3催化氧化反应,按如图装置进行实验。
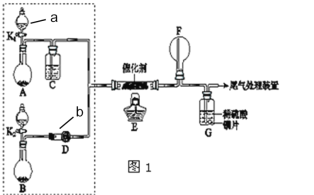
已知A、B装置可选药品:浓氨水、H2O2、蒸馏水、生石灰、MnO2。
(1)仪器a的名称为___;仪器b的名称为___。
(2)装置A烧瓶中固体的作用为___(填序号)
A.催化剂 B.氧化剂 C.还原剂 D.反应物
(3)仪器b中盛放的试剂可以是____(填序号)
A.浓硫酸 B.碱石灰 C.五氧化二磷 D.硫酸铜
(4)装置E中发生反应的化学方程式____。
(5)甲乙两同学分别按上述装置进行实验,一段时间后。
①甲观察到装置F中只有白烟生成,白烟的成分是___(写化学式)。
②乙观察到装置F中有红棕色气体,装置G中溶液变成蓝色。用离子方程式解释装置G中溶液变成蓝色的原因:___;
(6)为帮助甲实现在装置F中也观察到红棕色气体,可在原实验的基础上进行改进。你的改进措施是___。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】常温下浓度均为0.1mol/L 的四种盐溶液,其pH 如表所示,下列说法正确的是( )
序号 | ① | ② | ③ | ④ |
溶液 | CH3COONa | NaHCO3 | Na2CO3 | NaClO |
pH | 8.8 | 9.7 | 11.6 | 10.3 |
A. 将等浓度的CH3COOH 和HClO溶液,pH小的是HClO
B. Na2CO3和NaHCO3溶液中粒子种类不同
C. 溶液水的电离程度:①>②>④>③
D. NaHCO3溶液中:c (Na+) =c (CO32- )+c (HCO3- )+c (H2CO3)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】药物中间体Q、医用材料PVA的合成路线如图。

已知:
Ⅰ.—NH2+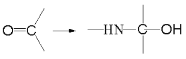
Ⅱ.A的分子式是C6H6
Ⅲ.W是最简单的α—氨基酸
IV.C→D是取代反应
请回答下列问题:
(1)A→B的反应类型是___。
(2)B→C是硝化反应,试剂a是___。
(3)E的化学名称是___。
(4)F的含有碳碳双键和酯基的同分异构体有___种(含顺反异构体,不含F),其中核磁共振氢谱有3组吸收峰,且能发生银镜反应的结构简式是___。
(5)G→X的化学方程式是___。
(6)W能发生聚合反应,所形成的高分子化合物的结构简式是___。
(7)将下列E+W→Q的流程图补充完整(在虚线框内写出物质的结构简式):___。
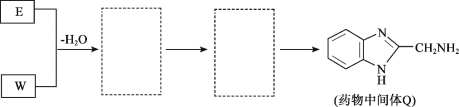
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】实验室用浓盐酸和![]() 制
制![]() ,并以干燥的
,并以干燥的![]() 为原料进行实验,装置如下图所示。
为原料进行实验,装置如下图所示。
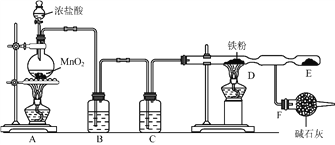
⑴装置![]() 烧瓶中发生反应的化学方程式为:_________________________________。
烧瓶中发生反应的化学方程式为:_________________________________。
⑵装置![]() 、
、![]() 中应盛放的试剂名称分别为__________、_________;从
中应盛放的试剂名称分别为__________、_________;从![]() 装置导出的气体若不经过
装置导出的气体若不经过![]() 、
、![]() 装置而直接进入
装置而直接进入![]() 管,将对实验产生的不良后果是___________________________。
管,将对实验产生的不良后果是___________________________。
⑶实验时,先点燃![]() 处的酒精灯,让氯气充满装置,再点燃
处的酒精灯,让氯气充满装置,再点燃![]() 处酒精灯,写出
处酒精灯,写出![]() 中反应的化学方程式:_________________________________________。
中反应的化学方程式:_________________________________________。
⑷![]() 装置所起的作用是____________________,____________________。
装置所起的作用是____________________,____________________。
⑸用廉价的石灰乳吸收氯气可制得漂粉精,写出工业制漂粉精反应的化学方程式:
___________________________________________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】测定Cu(NO3)2nH2O的结晶水含量,下列方案中肯定不可行的是( )
A.称量样品→加热→冷却→称量CuO
B.称量样品→加热→冷却→称量Cu(NO3)2
C.称量样品→加热→用已知质量的无水氯化钙吸收水蒸气并称量
D.称量样品→加NaOH→过滤→加热→冷却→称量CuO
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com