
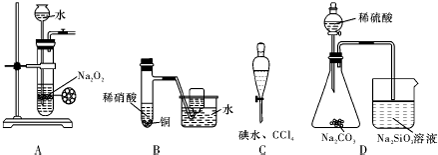
| A. | 制备少量氧气 | B. | 制备并收集少量NO气体 | ||
| C. | 四氯化碳萃取碘水中的碘 | D. | 证明非金属性强弱:S>C>Si |
分析 A.过氧化钠与水反应剧烈,不能用简易气体发生装置制备;
B.稀硝酸与铜反应生成NO;
C.碘易溶于四氯化碳,且四氯化碳不溶于水;
D.可根据最高价氧化物对应的水化物的酸性强弱比较非金属性强弱.
解答 解;A.过氧化钠与水反应剧烈,且为粉末状固体,不能用简易气体发生装置制备,可用分液漏斗和锥形瓶制备,故A错误;
B.稀硝酸与铜反应生成NO,可用排水法收集,故B正确;
C.碘易溶于四氯化碳,且四氯化碳不溶于水,可用分液的方法分离,故C正确;
D.锥形瓶内生成气体,可证明硫酸的酸性比碳酸强,烧杯生成沉淀,可证明碳酸的酸性比硅酸强,酸性越强,对应的元素的非金属性越强,故D正确.
故选A.
点评 本题考查实验方案的评价,为高考常见题型,侧重于学生的分析、实验能力的考查,注意把握实验的严密性和可行性的评价,注意物质的性质的差异,难度不大.


 开心蛙状元测试卷系列答案
开心蛙状元测试卷系列答案科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:多选题
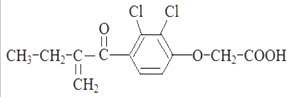
| A. | 分子式是C13H14O4Cl2 | |
| B. | 一定条件下能发生消去反应 | |
| C. | -定条件下能发生加聚反应 | |
| D. | 1mol利尿酸最多能与5molH2发生加成反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | Ksp(AB2)小于Ksp(CD),说明AB2的溶解度一定小于CD的溶解度 | |
| B. | 除零族元素外,短周期元素的最高化合价在数值上都等于该元素所属的族序数 | |
| C. | 2C+SiO2$\frac{\underline{\;高温\;}}{\;}$Si+2CO↑,此反应能够进行是因为碳的还原性比硅强 | |
| D. | 弱酸也可以通过复分解反应制强酸,如:H2S+CuSO4=H2SO4+CuS↓ |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
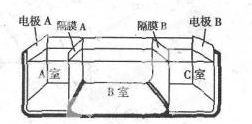 水是一种重要的自然资源,是人类赖以生存不可缺少的物质.请回答下列问题:
水是一种重要的自然资源,是人类赖以生存不可缺少的物质.请回答下列问题:查看答案和解析>>
科目:高中化学 来源: 题型:解答题
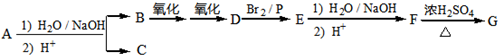
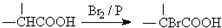
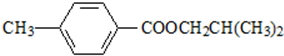 .
.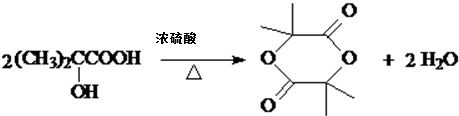 ,该反应属于取代反应(或酯化反应)(填反应类型).
,该反应属于取代反应(或酯化反应)(填反应类型).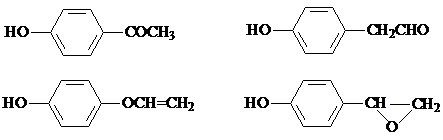 .
.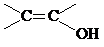 )结构.
)结构.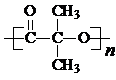 .
.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 硫酸铁可用作净水剂 | B. | 二氧化硅可用作计算机芯片 | ||
| C. | 铜制容器可用于盛装浓硝酸 | D. | 醋酸铅可用于分离提纯蛋白质 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 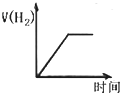 | B. | 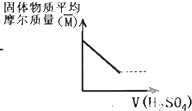 | ||
| C. | 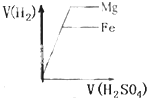 | D. | 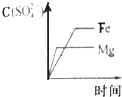 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | b=c | |
| B. | R元素位于周期表的ⅤA族 | |
| C. | 滴定终点时,溶液的颜色由无色变为蓝色 | |
| D. | 若滴定消耗Na2S2O3溶液20.00mL,则反应①转移电子6.02×1020个 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com