
部分弱酸的电离平衡常数如下表:
| 弱酸 | HCOOH | HCN | H2CO3 |
| 电离平衡常数 (25℃) | Ka=1.77×10-4 | Ka=4.9×10-10 | Ka1=4.3×10-7 Ka2=5.6×10-11 |
BC
解析试题分析:A、氢氰酸的电离平衡常数小于碳酸而大于碳酸氢根离子,所以氢氰酸酸性小于碳酸而大于碳酸氢根离子,根据强酸制取弱酸知碳酸和氰化物的盐反应生成氢氰酸和碳酸氢盐,离子方程式为CN-+H2O+CO2═HCN+HCO3-,错误;B、因为HCOOH的电离平衡常数大于HCN的电离平衡常数,所以等pH的HCOOH和HCN,HCN的浓度大,因此中和等体积、等pH的HCOOH和HCN消耗NaOH的量前者小于后者,正确;C、根据物料守恒可得两溶液分别存在:c(Na+)-c(HCOO-)=c(HCOOH),c(K+)-c(CN-)=c(HCN),根据越弱越水解的规律,c(HCOOH)< c(HCN),则c(Na+)-c(HCOO-) < c(K+)-c(CN-),正确;D、根据越弱越水解的规律,c(NH4+) 相等的HCOONH4溶液、NH4CN溶液、NH4HCO3溶液中,c(NH4CN) > c(NH4HCO3) c(HCOONH4),错误。
考点:本题考查弱电解质的电离平衡、水解规律、离子浓度比较。


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:单选题
己知25℃时,Ksp(AgCl) =1.8×10-10,Ksp(AgBr) =5.4×10-13,Ksp(AgI) =8.5×10-17。某溶液中含有C1-、Br-和I-,浓度均为0.010mo1·L-1,向该溶液中逐滴加入0.010mol·L-1的AgNO3溶液时,三种阴离子产生沉淀的先后顺序为
| A.C1-、Br-、I- | B.Br-、C1-、I- |
| C.I-、Br-、C1- | D.Br-、I-、C1- |
查看答案和解析>>
科目:高中化学 来源: 题型:单选题
25 ℃在等体积的①pH=0的H2SO4溶液,②0.05 mol·L-1的Ba(OH)2溶液,③pH = 10的Na2S溶液,④pH=5的NH4NO3溶液中,发生电离的水的物质的量之比是( )
| A.1∶10∶1010∶109 | B.1∶5∶5×109∶5×109 |
| C.1∶20∶1010∶109 | D.1∶10 ∶104∶109 |
查看答案和解析>>
科目:高中化学 来源: 题型:单选题
T ℃时,某NaOH溶液中c(H+)=10-amol·L-1,c(OH-)=10-bmol·L-1,已知a+b=12。向该溶液中逐滴加入pH=c的盐酸(T ℃),测得混合溶液的部分pH如表中所示:
| 序号 | NaOH溶液的体积/mL | 盐酸的体积/mL | 溶液的pH |
| ① | 20.00 | 0.00 | 8 |
| ② | 20.00 | 20.00 | 6 |
查看答案和解析>>
科目:高中化学 来源: 题型:单选题
下列溶液中离子浓度大小关系错误的是
A.0.1 mol/L的NH4Cl溶液中: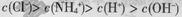 |
B.0.1mol/L的CH3COONa溶液中: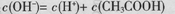 |
C.0.1 mol/LNa2S的溶液中: |
D.pH=2的盐酸与pH=12的氨水等体积混合后: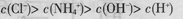 |
查看答案和解析>>
科目:高中化学 来源: 题型:单选题
25℃时,几种弱酸的电离常数如下:
| 弱酸的化学式 | CH3COOH | HCN | H2S |
| 电离常数(25℃) | 1.8×10-5 | 4.9×10-10 | K1=1.3×10-7 K2=7.1×10-15 |
查看答案和解析>>
科目:高中化学 来源: 题型:单选题
下列说法或表达正确的是
| A.CH3COONa溶液中加入少量KNO3固体后的碱性溶液一定有: C(Na+)-c(CH3COO-)=c(OH-)-c(H+) |
| B.向ZnS白色悬浊液中加入CuSO4溶液,有黑色沉淀产生,是因为Ksp (ZnS)<Ksp (CuS) |
| C.向沸腾的NaOH溶液中滴加FeCl3饱和溶液,可以制备Fe(OH)3胶体 |
| D.热水中加入NaCl溶解至饱和后溶液的pH等于7 |
查看答案和解析>>
科目:高中化学 来源: 题型:单选题
常温下,0.2mol/L一元酸HA与等浓度的NaOH溶液等体积混合后,所得溶液中部分微粒组分及浓度如图所示,下列说法正确的是
| A.HA是强酸 |
| B.该混合液pH=7 |
| C.图中x表示HA,Y表示OH-,Z表示H+ |
| D.该混合溶液中:c(A-)+c(Y)=c(Na+) |
查看答案和解析>>
科目:高中化学 来源: 题型:单选题
在不同温度下,水溶液中c(H+)与c(OH-)有如图所示关系,下列说法正确的是( )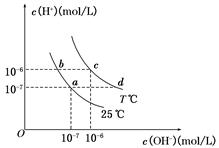
A.a点对应的溶液和c点对应的溶液pH值大小:
pH(c)>pH(a)
B.d点对应的溶液中大量存在:K+、Ba2+、NO3-、I-
C.25℃时,Ka(HF)=3.6×10-4,Ka(CH3COOH)=1.75×10-5,
0.1mol/L的NaF溶液与0.1mol/L 的CH3COOK溶液相比:
c(Na+)-c(F-)>c(K+)-c(CH3COO-)
D.如b点对应的溶液中只含NaHA,则溶液中粒子浓度大小:
c(HA-)>c(H2A)>c(H+)>c(A2-)
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com