
【选修3:物质结构与性质】
在电解冶练铝的过程中加入冰晶石,可起到降低Al2O3熔点的作用。冰晶石的生产原理为2Al(OH)3+12HF+3Na2CO3═2Na3AlF6+3CO2↑+9H2O.根据题意完成下列填空:
(1)冰晶石的晶体不导电,但熔融时能导电,则在冰晶石晶体中存在__________(填序号).
a.离子键 b.极性键 c.配位键 d.范德华力
(2)CO2分子的空间构型为__________,中心原子的杂化方式为__________,和CO2 互为等电子体的氧化物是__________;
(3)反应物中电负性最大的元素为_________(填元素符号),写出其原子最外层的电子排布图__________;
(4)冰晶石由两种微粒构成,冰晶石的晶胞结构如图甲所示,●位于大立方体的顶点和面心,○位于大立方体的12条棱的中点和8个小立方体的体心,那么大立方体的体心处所代表的微粒是______(填具体的微粒符号).

(5)Al单质的晶体中原子的堆积方式如图乙所示,其晶胞特征如图丙所示,原子之间相互位置关系的平面图如图丁所示:
若已知Al的原子半径为d cm,NA代表阿伏伽德罗常数,Al的相对原子质量为M,则一个晶胞中Al原子的数目为_________个;Al晶体的密度为__________(用字母表示)。
 科学实验活动册系列答案
科学实验活动册系列答案科目:高中化学 来源:2015-2016学年湖南省高二下期中理科化学试卷(解析版) 题型:选择题
物质的量之比为2:5的锌与稀硝酸反应,若硝酸被还原的产物为N2O,反应结束后锌没有剩余,则该反应中被还原的硝酸与未被还原的硝酸的物质的量之比是( )
A.1:4 B.1:5 C.2:3 D.2:5
查看答案和解析>>
科目:高中化学 来源:2015-2016学年重庆市高二下期中化学试卷(解析版) 题型:选择题
现代化学测定有机物组成及结构的分析方法较多,下列有关说法正确的是(
A.元素分析仪不仅可以测出试样常见的组成元素及含量,还可以测定具分子的空间结构
B.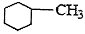 的核磁共振氢谱中有4组峰
的核磁共振氢谱中有4组峰
C.通过红外线光谱图分析可以区分乙醇和乙酸乙酯
D.质谱法和红外光谱法不属于测定有机物组成和结构的现代分析方法
查看答案和解析>>
科目:高中化学 来源:2015-2016学年宁夏银川二中高二下期中化学试卷(解析版) 题型:选择题
利尿酸是奥运会上被禁用的兴奋剂之一,其结构简式如下:
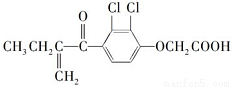
下列叙述正确的是( )
A.利尿酸分子内处于同一平面的原子数不超过10个
B.1mol利尿酸能与7molH2发生加成反应
C.利尿酸的衍生物利尿酸甲酯的分子式是C14H14Cl2O4
D.利尿酸能与FeCl3溶液发生显色反应
查看答案和解析>>
科目:高中化学 来源:2015-2016学年宁夏银川二中高二下期中化学试卷(解析版) 题型:选择题
下列除杂方法正确的是( )
①除去乙烷中少量的乙烯:通入H2,加催化剂反应
②除去乙酸乙酯中少量的乙酸:用饱和碳酸钠溶液洗涤,分液
③除去苯中少量的苯酚:滴加适量溴水,过滤
④除去乙醇中少量的乙酸:加足量生石灰,蒸馏
⑤除去苯中少量的甲苯:加足量KMnO4溶液,分液.
A.①②③B.②③④C.②④⑤D.③④⑤
查看答案和解析>>
科目:高中化学 来源:2016届江西省高三5月模拟考试理综化学试卷(解析版) 题型:选择题
常温下,用0.10mol•L-1NaOH溶液分别滴定20.00mL浓度均为0.10mol•L-1CH3COOH溶液和HCN溶液所得滴定曲线如下图。下列说法正确的是

A.点①和点②所示溶液中:c(CH3COO-)<c(CN-)
B.点③和点④所示溶液中:c(Na+)>c(OH-)>c(CH3COO-)>c(H+)
C.点①和点②所示溶液中:c(CH3COO-)-c(CN-)=c(HCN)-c(CH3COOH)
D.点②和点③所示溶液中都有:c(CH3COO-)+c(OH-)=c(CH3COOH)+c(H+)
查看答案和解析>>
科目:高中化学 来源:2015-2016学年江西吉安一中高二下第二次段考化学试卷(解析版) 题型:简答题
三聚氰胺(化学式:C3N6H6)是一种非食品类的重要有机化工原料、广泛用于塑料、造纸、建材等行业。下图是我国科技工作者研制的以尿素为原料生产三聚氰胺的工艺——--“常压气相一步法联产纯碱新技术”:
已知:①尿素的熔点是132.7℃,常压下超过160℃即可分解;
②三聚氰胺的熔点是354℃,加热易升华,微溶于水;
③以尿素为原料生产三聚氰胺的原理是:6CO(NH2)2 C3N6H6+6NH3+3CO2
C3N6H6+6NH3+3CO2
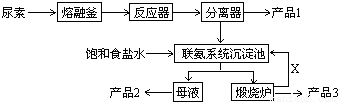
请回答:
(1)尿素是一种常用含氮量最高的化肥,其氮元素的质量百分数为_______________,在实验室使其熔化的容器名称叫_____________。
(2)写出各主要成份的化学式:产品2________、X_________;
(3)联氨系统沉淀池中发生的化学反应方程式为____________________。
(4)工业上合成尿素的化学反应方程式为______________________(反应条件可以不写)。
(5)为了使母液中析出更多的产品2,常用的方法是_______
A.加入固体NaCl B.加入固体NaHCO3 C.通入CO2气体 D.通入NH3
(6)若生产过程中有4%的尿素损耗,每吨尿素可生产三聚氰胺______吨。(精确到0.001)
查看答案和解析>>
科目:高中化学 来源:2015-2016学年江西吉安一中高二下第二次段考化学试卷(解析版) 题型:选择题
NA为阿伏加罗常数的值,下列叙述正确的是
A.1molCH3+中含有的电子数为10NA
B.1mol铁粉与1mol水蒸气充分反应转移的电子数为3A
C.0.1mol/L的Al2(SO4)3溶液中,Al3+的数目小于0.2NA
D.电解精炼铜时,若转移了NA个电子,则阴极析出32g铜
查看答案和解析>>
科目:高中化学 来源:2016届湖北省黄冈市高三4月考试理综化学试卷(解析版) 题型:简答题
[化学—选修2:化学与技术]粉煤灰是燃煤电厂排出的主要固体废物。我国火电厂粉煤灰的主要氧化物组成为SiO2、Al2O3、CaO等。一种利用粉煤灰制取氧化铝的工艺流程如下 :
: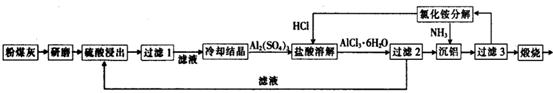
(1)粉煤灰研磨的目的是_______________________。
(2)第1次过滤时滤渣的主要成分有__________、__________(填化学式,下同),第3次过滤时滤渣的成分是__________。
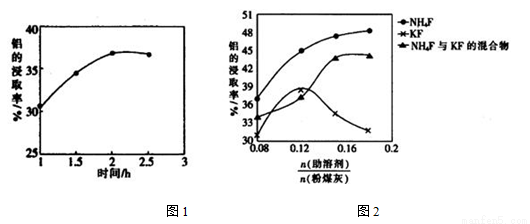
(3)在104℃用硫酸浸取时,铝的浸取率与时间关系如图1,适宜的浸取时间为__________h;铝的浸取率与 的关系如图2所示,从浸取率角度考虑,三种助溶剂NH4F、KF及NH4F与KF的混合物,在
的关系如图2所示,从浸取率角度考虑,三种助溶剂NH4F、KF及NH4F与KF的混合物,在 相同时,浸取率最高的是__________(填助溶剂化学式);用含氟的化合物作这种助溶剂的缺点是__________(举一例)。
相同时,浸取率最高的是__________(填助溶剂化学式);用含氟的化合物作这种助溶剂的缺点是__________(举一例)。
(4)流程中循环使用的物质有__________。(填化学式)
(5)用盐酸溶解硫酸铝晶体,再通入HCl气体,析出AlCl3·6H2O,请简要说明该过程能够发生的原因____________________。
(6)用粉煤灰制取含铝化合物的主要意义是____________________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com