
人们应用原电池原理制作了多种电池,以满足不同的需要。以下每小题中的电池广泛使用于日常生活、生产和科学技术等方面,请根据题中提供的信息,填写空格。
(1)蓄电池在放电时起原电池作用,在充电时起电解池的作用。铅蓄电池在放电时发生的电池反应式为:Pb+PbO2+2H2SO4=2PbSO4+2H2O。
正极电极反应式为____________ ____ 。
(2)FeCl3溶液常用于腐蚀印刷电路铜板,发生2FeCl3+Cu=2FeCl2+CuCl2,若将此反应设计成原电池,则负极所用电极材料为________________,当线路中转移0.2mol电子时,则被腐蚀铜的质量为 g
(3)将铝片和铜片用导线相连,一组插入浓硝酸中,一组插入烧碱溶液中,分别形成了原电池,在这两个原电池中,负极分别为___________ _____。
A.铝片、铜片 B.铜片、铝片 C.铝片、铝片
(4)燃料电池是一种高效、环境友好的供电装置,如图是电解质为稀硫酸溶液的氢氧燃料电池原理示意图,回答下列问题:
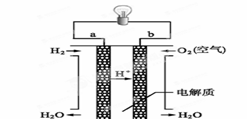
① 氢氧燃料电池的总反应化学方程式是:_________ ___。
② 电池工作一段时间后硫酸溶液的浓度____ _____(填“增大”、“减小”或“不变”)。
科目:高中化学 来源: 题型:
已知:①A是石油分解的主要成分,A的产量通常用来衡量一个国家的石油化工水平;②2CH3CHO+O2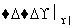 2CH3COOH。现以A为主要原料合成乙酸乙酯,其合成路线如下图所示。
2CH3COOH。现以A为主要原料合成乙酸乙酯,其合成路线如下图所示。
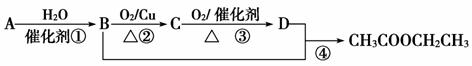
回答下列问题:
(1)写出A的结构式_________________;C的结构简式______________________;
(2)B、D分子中的官能团分别是________________、_________________。
(3)写出下列反应的反应类型:①_______________,②_______________,④________________。
(4)写出下列反应的化学方程式:
①________________________________________________________________________;
②________________________________________________________________________;
④________________________________________________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
在一定条件下,密闭容器中可发生可逆反应:N2(g) + 3H2(g)  2NH3(g) 。
2NH3(g) 。
下列说法中,表明这一反应已经达到化学平衡状态的是
A.N2、H2、NH3的浓度相等 B.N2、H2、NH3的浓度不再变化
C.N2、H2、NH3在密闭容器中共存 D.反应停止,正、逆反应速率都等于零
查看答案和解析>>
科目:高中化学 来源: 题型:
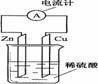
右图为铜锌原电池示意图,按该装置进行实验下列说法正确的是
A.锌片逐渐溶解 B.烧杯中溶液逐渐呈蓝色
C.电子由铜片通过导线流向锌片 D.该装置能将电能转变为化学能
查看答案和解析>>
科目:高中化学 来源: 题型:
2013·北京理综,7)下列金属防腐的措施中,使用外加电流的阴极保护法的是 ( )
A.水中的钢闸门连接电源的负极
B.金属护栏表面涂漆
C.汽车底盘喷涂高分子膜
D.地下钢管连接镁块
查看答案和解析>>
科目:高中化学 来源: 题型:
瑞典皇家科学院2001年10月10日宣布,2001年诺贝尔化学奖授予“手性碳原子的催化氢化、氧化反应”研究领域作出贡献的美、日三位科学家。在有机物中,若碳原子上连接的四个原子或原子团不相同,则这个碳原子称为手性碳原子。下列分子中含有“手性碳原子”的是 ( )
A.CBr2F2 B.CH3CH2OH C.CH3CH2CH3 D.CH3CH(OH)COOH
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com