
| A. | 纯铁比生铁不易生锈 | |
| B. | 当镀锡铁制品的镀层破损时,镀层仍能对铁制品起保护作用 | |
| C. | 在海轮外壳连接锌块能保护钢制外壳不受腐蚀,此方法叫做牺牲阳极的阴极保护法 | |
| D. | 电解精炼铜,阳极质量减少64g时,电子转移不一定是2mol |
分析 A、生铁中金属铁、碳、潮湿的空气能构成原电池;
B、镀层破损后,铁比锡活泼作负极被腐蚀;
C、在海轮外壳连接锌块,保护外壳不受腐蚀是采用了牺牲阳极的阴极保护法;
D、根据粗铜中含有杂质(铁)的摩尔质量比铜小,转移的电子的物质的量大于2mol分析.
解答 解:A、生铁中金属铁、碳、潮湿的空气能构成原电池,金属铁为负极,易被腐蚀而生锈,所以纯铁比生铁不易生锈,故A正确;
B、镀层破损后,铁比锡活泼作负极被腐蚀,所以镀锡铁板的镀层不能对铁制品起保护作用,加快铁板的腐蚀,故B错误;
C、在海轮外壳连接锌块,锌被腐蚀,从而保护了铁,所以保护外壳不受腐蚀是采用了牺牲阳极的阴极保护法,故C正确;
D、电解精炼铜时,若阳极质量减少64g,由于阳极有铁杂质存在,铁的摩尔质量小于铜的,所以阳极减少64g,转移的电子的物质的量大于2mol,则阴极得到的电子数大于2mol,故D正确;
故选B.
点评 本题考查了金属的腐蚀与防护,难度不大,会运用化学知识解决生产、生活问题,学以致用.


 期末1卷素质教育评估卷系列答案
期末1卷素质教育评估卷系列答案科目:高中化学 来源: 题型:解答题

查看答案和解析>>
科目:高中化学 来源: 题型:选择题
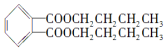 ,下列有关说法正确的是( )
,下列有关说法正确的是( )| A. | 邻苯二甲酸二丁酯的分子式为C16H21O4 | |
| B. | 用邻苯二甲酸与1-丁醇合成邻苯二甲酸二丁酯的反应属于取代反应 | |
| C. | 邻苯二甲酸二丁酯属于酯类,可增加白酒的香味,对人体无害 | |
| D. | 邻苯二甲酸二丁酯不能发生加成反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 5mol•L-1 | B. | 9mol•L-1 | C. | 11mol•L-1 | D. | 12mol•L-1 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 0.1 mol C2H6O分子中含有C-H键数为0.5NA | |
| B. | 标准状况下,11.2 L CH3CH2OH中含有的分子数目为0.5NA | |
| C. | 3.0 g甲醛(HCHO)和乙酸的混合物中含有的原子总数为0.4NA | |
| D. | 常温常压下,12 g冰醋酸溶解于水,其电离出的氢离子数为0.2NA |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 0.448 L | B. | 0.224L | C. | 0.336L | D. | 无法求解 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 加碘食盐不能使淀粉溶液变蓝 | |
| B. | 凡含有食品添加剂的食物对人体健康均有害,不可食用 | |
| C. | 为防止电池中的重金属等污染土壤和水体,应集中回收并填埋处理,开发废电池的综合利用技术 | |
| D. | 乙醇是不可再生的能源 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | NH4HSO3溶于过量NaOH溶液中:HSO3-+OH-═SO32-+H2O | |
| B. | 酸性KMnO4溶液与FeSO4溶液反应:MnO4-+5Fe2++8H+═Mn2++5Fe3++4H2O | |
| C. | CaCO3溶于CH3COOH溶液中:CaCO3+2H+═Ca2++H2O+CO2↑ | |
| D. | 标准状况下足量Cl2通入100mL0.1 mol•L-1FeBr2溶液中:2Fe2++2Br-+2Cl2═2Fe3++Br2+4Cl- |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 稀HCl溶液 | B. | 稀Na2SO4溶液 | C. | CuCl2溶液 | D. | AgNO3溶液 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com