
关于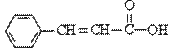 的下列说法中正确的是
的下列说法中正确的是
A.分子式为C9H9O2
B.含有三种官能团
C.可使溴的四氯化碳溶液或酸性KMnO4溶液褪色
D.可以发生取代反应和加成反应,但不能发生聚合反应
 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:
对某一可逆反应来说,使用催化剂的作用是( )
|
| A. | 提高反应物的平衡转化率 |
|
| B. | 以同样程度改变正逆反应的速率 |
|
| C. | 增大正反应速率,减小逆反应速率 |
|
| D. | 改变平衡混合物的组成 |
查看答案和解析>>
科目:高中化学 来源: 题型:
在密闭容器中进行下列反应:
CO2(g)+C(s)⇌2CO(g)△H>0,起始通入2molCO,达到平衡后,改变下列条件,则指定物质的浓度、百分含量(填“不变”“增大”“减小”)及平衡如何变化(填“正移”“逆移”“不移动”):
(1)增加C,平衡 ,c(CO) .
(2)减小密闭容器的体积,保持温度不变,则平衡 ,c(CO2) .
(3)通入N2,保持密闭容器的体积和温度不变,则平衡 ,c(CO2) .
(4)保持密闭容器的体积不变,升高温度,则平衡 ,c(CO)
(5)恒压通入N2,CO2的百分含量
(6)恒压再通入2molCO,CO2的百分含量 .
查看答案和解析>>
科目:高中化学 来源: 题型:
下列有关金属腐蚀与防护的说法正确的是( )
|
| A. | 纯银器表面在空气中因电化学腐蚀渐渐变暗 |
|
| B. | 当镀锡铁制品的镀层破损时,镀层仍能对铁制品起保护作用 |
|
| C. | 在海轮外壳连接锌块保护外壳不受腐蚀是采用了牺牲阳极的阴极保护法 |
|
| D. | 可将地下输油钢管与外加直流电源的正极相连以保护它不受腐蚀 |
查看答案和解析>>
科目:高中化学 来源: 题型:
A、B、C、D、E五种溶液分别是NaOH、NH3•H2O、CH3COOH、HCl、NH4HSO4中的一种.常温下进行下列实验:
①将1L pH=3的A溶液分别与0.001mol/L x L B溶液、0.001mol/L y L D溶液充分反应至中性,x、y的大小关系式y<x;
②浓度均为0.1mol/L A和E溶液,pH:A<E
③浓度均为0.1mol/L C和D溶液等体积混合,溶液呈酸性.
回答下列问题:
(1)C是 溶液,D是 溶液.
(2)用水稀释0.1mol/L B溶液时,溶液中随水量的增加而减小的是 .
A.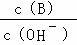 B.
B. C.c (H+)•c (OH﹣) D.n (OH﹣)
C.c (H+)•c (OH﹣) D.n (OH﹣)
(3)等pH、等体积的两份溶液A和E,分别与锌粉反应,若最后仅有一份溶液中存在锌粉,且放出的氢气的质量相同.则 (填化学式)溶液中锌粉有剩余.
(4)常温下,向0.01mol/L C溶液中滴加0.01mol/L D溶液至中性,得到的溶液中所有离子的物质的量浓度由大到小的顺序为 .
(5)已知常温下Mg(OH)2在pH=12的D溶液中Mg2+的浓度为1.8×10﹣7mol/L,则 Ksp[Mg(OH)2]= .
查看答案和解析>>
科目:高中化学 来源: 题型:
从某废触媒[主要成分为活性炭、ZnO、FeO、(CH3COO)2Zn]中制取醋酸锌晶体的实验步骤如图:
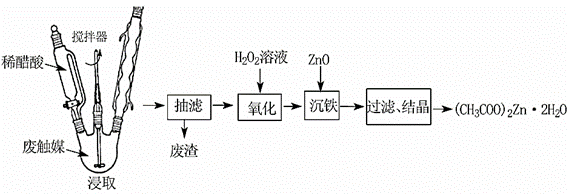
(1)浸取时,在三口烧瓶中加入废触媒及稀醋酸,给三口烧瓶加热并同时开动搅拌器的目的是 。
(2)若先将废触媒在马弗炉中通氧气500℃处理一段时间,浸出率会大大提高,其原因是 。抽滤时用的硅酸盐质仪器有 和 。
(3)流程图中加入H2O2的目的是 。
(4)所得晶体(CH3COO)2Zn·2H2O热重分析(TG/%=固体样品的剩余质量/固体样品的起始质量),文献表明分解分三个阶段,在200℃以下脱去两分子结晶水,形成的(CH3COO)2Zn在242℃熔融,370℃完全分解为ZnO同时生成CO2及一种含氧衍生物(核磁共振氢谱只有1组峰)。(CH3COO)2Zn分解生成氧化锌的反应方程式为 。

查看答案和解析>>
科目:高中化学 来源: 题型:
下列有关反应的离子方程式的书写中,正确的是
A.C12通入水中:C12+H2O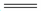 2H++Cl-+ClO-
2H++Cl-+ClO-
B.硫酸铝溶液与过量氨水反应:Al3++3NH3·H2O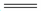 3
3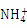 +Al(OH)3↓
+Al(OH)3↓
C.实验室用石灰石和盐酸反应制取
D.向Na2SO3溶液中加入稀硝酸:
查看答案和解析>>
科目:高中化学 来源: 题型:
某同学分析Zn与稀H2SO4的反应。
(1)该反应的离子方程式是 。
(2)制H2时,用稀硫酸而不用浓硫酸,原因是_________。
(3)已知:Zn(s)+1/2O2(g)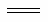 ZnO(s) ΔH=-332 kJ/mol
ZnO(s) ΔH=-332 kJ/mol
ZnO(s) + H2SO4(aq) 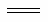 ZnSO4(aq) + H2O(l) ΔH =-112kJ/mol
ZnSO4(aq) + H2O(l) ΔH =-112kJ/mol
H2(g) +1/2 O2(g)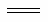 H2O(l) ΔH =-286kJ/mol
H2O(l) ΔH =-286kJ/mol
则Zn与稀H2SO4反应生成1mol H2 时的反应热ΔH = kJ/mol。
(4)该同学用如下装置进行实验,分析影响反应速率的因素。

实验时,从断开K开始,每间隔1分钟,交替断开或闭合K,并连续计数每1 分钟内从a管流出的水滴数,得到的水滴数如下表所示:
| 1分钟水滴数(断开K) | 34 | 59 | 86 | 117 | … | 102 |
| 1分钟水滴数(闭合K) | 58 | 81 | 112 | 139 | … | 78 |
分析反应过程中的水滴数,请回答:
①由水滴数58>34、81>59,说明在反应初期,闭合K时比断开K时的反应速率______(填“快”或“慢”),主要原因是_________。
②由水滴数102>78,说明在反应后期,断开K时的反应速率快于闭合K时的反应速率,主要原因是_________。
③ 从能量转换形式不同的角度,分析水滴数86>81、117>112的主要原因是_______。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com