
��14�֣�A��B���ֹ������ʵ��ܽ����������ͼ��ʾ����ش�
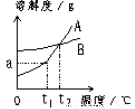
��1�� ��ʱ��A��B�������ʵ��ܽ����ͬ��
��2���ҹ���Щ������һ��˵�����������̼����ɹ�Ρ�������ļ�ָNa2CO3������ָNaCl����ô��ͼ��__________����A��B�����ܽ��������Na2CO3���ܽ���������ƣ�
��3�������������������κ����̵õ�Na2CO3��������������NaCl�����Լ���Na2CO3��Ħ������Ϊ ��2mol Na2CO3��Լ���� ��̼ԭ�ӣ�
��4��ij�о���ѧϰС����̵õļ���з�������ȡNa2CO3���壨����������NaCl����Ʒ12.5g���������Ƴ���Һ������������μ���������ϡ���ᣬʹ������ȫ�ų������ռ���0.1molCO2���塣�÷�Ӧ�Ļ�ѧ����ʽΪ ��������Ʒ�к�Na2CO3�����ʵ���Ϊ ������Ϊ ��
��ÿ��2�֣���14�֣�
��1��t2 ��2��A
��3��106g/mol����λ�����֣���ͬ�� 1.204��1024
��4��2HCl��Na2CO3==2NaCl��H2O��CO2�� 0.1 mol 10.6 g
��������
�����������1����ͼ���֪����t2 ��ʱ��A��B�������ʵ��ܽ����ͬ��
��2�������̼����ɹ�Σ�˵���������¶ȵ�ʱ�ܽ�Ƚ�С���¶ȸ�ʱ�ܽ�Ƚϴ�����A���߷������⣬��A���ܽ��������Na2CO3���ܽ���������ƣ�
��3������Ħ����������ֵ������Է���������ȿ�֪��̼���Ƶ�Ħ��������106g/mol��2mol Na2CO3��Լ����2mol��6.02��1023mol-1= 1.204��1024 ��Cԭ�ӣ�
��4��̼������������ϡ���ᷴӦ�����Ȼ��ơ�ˮ��������̼���壬��ѧ����ʽΪ2HCl��Na2CO3==2NaCl��H2O��CO2��������CԪ���غ㣬��֪��̼������Ʒ�к���0.1mol��̼���ƣ�������0.1mol��106g/mol=10.6g��
���㣺�����ͼ��ķ��������ʵ������йؼ���


 ��һ����ͬ���ɽ�����ϵ�д�
��һ����ͬ���ɽ�����ϵ�д� ������Ӧ���ϵ�д�
������Ӧ���ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ��2014-2015ѧ���㽭̨����ѧ�߶���ѧ�ڵ�һ��ͳ����ѧ�Ծ��������棩 ���ͣ������
��8�֣���ͼ��ʾ��ͨ��5 min�ڢۼ�����2.16 g��ͬʱ��A�����ռ�����״���µ�����224 mL����A����ԭ���Һ�����Ϊ200 mL��
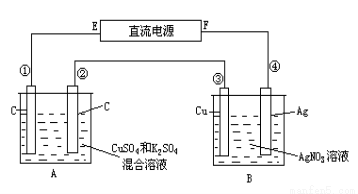
����1��д���١��ڵĵ缫��Ӧʽ�� ______________ _______________
��2��ͨ������ȷ��ͨ��ǰA����ԭ�����ҺCu2+��Ũ���� ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2014-2015ѧ�����۳���ص�һ���и߶��ϵ�һ�ο��Ի�ѧ��B���Ծ��������棩 ���ͣ�ѡ����
��һ�ܱ������н������·�Ӧ��2SO2(g)��O2(g) 2SO3(g)����֪��Ӧ������ijһʱ��SO2��O2��SO3��Ũ�ȷֱ�Ϊ0.2mol/L��0.1mol/L��0.2mol/L������Ӧ��ƽ��ʱ�����ܴ��ڵ������ǣ� ��
2SO3(g)����֪��Ӧ������ijһʱ��SO2��O2��SO3��Ũ�ȷֱ�Ϊ0.2mol/L��0.1mol/L��0.2mol/L������Ӧ��ƽ��ʱ�����ܴ��ڵ������ǣ� ��
A��SO2Ϊ0.4mol/L��O2Ϊ0.2mol/L B��SO2Ϊ0.25mol/L
C��SO2��SO3��Ϊ0.15mol/L D��SO3Ϊ0.4mol/L
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2014-2015ѧ�����۳���ص�һ���и߶��ϵ�һ�ο��Ի�ѧ��A���Ծ��������棩 ���ͣ�ѡ����
��֪���и��鷴Ӧ�ķ�Ӧ�P�¶ȣ���Ӧ��ʼʱ���ų�H2�����������ǣ����е����ʾ�Ϊ��Ӧ�
��� | ��������С����״��ͬ�ķ�ĩ�����ʵ��� | ���Ũ�ȼ���� | ��Ӧ�¶�/�� |
A | Mg 0.1 mol | 3 mol/L������10 mL | 60 |
B | Mg 0.1 mol | 3 mol/L������10 mL | 30 |
C | Fe 0.1 mol | 3 mol/L������10 mL | 60 |
D | Mg 0.1 mol | 3 mol/L������10 mL | 60 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2014-2015ѧ�����۳���ص�һ���и߶��ϵ�һ�ο��Ի�ѧ��A���Ծ��������棩 ���ͣ�ѡ����
��֪H2(g)��Br2(l)��2HBr(g) ��H����72kJ��mol��1������1mol Һ���Br2(g)��Ҫ���յ�����Ϊ30kJ����������������±���
| H2(g) | Br2(g) | HBr(g) |
1mol�����еĻ�ѧ������ʱ��Ҫ���յ�����/kJ | 436 | a | 369 |
�����aΪ
A��404 B��260 C��230 D��200
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2014-2015ѧ�����۳���ص�һ���и�һ�ϵ�һ�ο��Ի�ѧ��B���Ծ��������棩 ���ͣ�ѡ����
ʵ��������Ҫ����2mol/L��NaCl��Һ950mL������ʱӦѡ�õ�����ƿ�Ĺ��ͳ�ȡ��NaCl�����ֱ��ǣ� ��
A��950mL�� 111.2g B��500mL��117g
C��1000mL��117g D��1000mL��111.2g
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2014-2015ѧ�����۳���ص�һ���и�һ�ϵ�һ�ο��Ի�ѧ��B���Ծ��������棩 ���ͣ�ѡ����
����˵����ȷ���ǣ� ��
A��Ħ����7������������֮һ
B��18 gˮ�ڱ�״���µ����ԼΪ22.4 L
C��27 g AlԼ����6.02��1023����ԭ��
D������0.1 mol/L��NaCl��Һ��NaCl���������Ϊ5.85 g
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2014-2015ѧ�����۳���ص�һ���и�һ�ϵ�һ�ο��Ի�ѧ��A���Ծ��������棩 ���ͣ�ѡ����
��һ���ƿ����Ϊ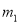 ����ƿ�������������Ϊ
����ƿ�������������Ϊ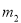 ������ͬ״���£�����Ϊ����ij����Aʱ������Ϊ
������ͬ״���£�����Ϊ����ij����Aʱ������Ϊ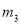 ����A����Է��������ǣ� ��
����A����Է��������ǣ� ��
A��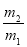 ��29 B��
��29 B��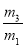 ��29 C��
��29 C��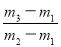 ��29 D��
��29 D��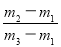 ��29
��29
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2014-2015ѧ�����ʡ��һ�ϵڶ��ο��Ի�ѧ�Ծ��������棩 ���ͣ�ѡ����
��100 mL����Һ����0.1 mol NaCl��0.1 mol AlCl3������Һ��Cl-�����ʵ���Ũ��Ϊ( )��
A��4 mol��L��1 B��2 mol��L��1 C��0.4 mol��L��1 D��0.2 mol��L��1
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com