
【题目】(环境污染与资源短缺问题日益突出,资源的循环利用尤为重要。工业 上利用含 Cu2O(含少量 Al2O3、Fe2O3 和 SiO2)的矿渣提取铜的工艺流程如下:

已知:①Cu2O 在酸性条件下易转化成单质 Cu 和含 Cu2+的溶液;
②几种氢氧化物沉淀时的 pH 如下表:
氢氧化物 | Al(OH)3 | Fe(OH)2 | Fe(OH)3 | Cu(OH)2 |
沉淀时的 pH | 4.0~5.2 | 5.8~8.8 | 1.1~3.2 | 5.4~6.7 |
回答下列问题:
(1)经检测固体 A 含有的成分为 Cu 和另一种杂质,从固体 A 中分离出 Cu 的可 用试剂为_____溶液(填化学式)。
(2)矿渣经酸浸、过滤、洗涤后铁元素的主要存在形式为__________填离子符号),检验该离子的常用化学试剂是_________________。
(3)加 NaClO 氧化并调整溶液的 pH 为_____,得到沉淀 B 和一种具有漂白 性的物质 D,该反应离子方程式为_________。
(4)25℃时,加 NaOH 固体调节溶液 pH 得到 Al(OH)3 沉淀,若 pH=5.3 时,所得 溶液中 c(Al3+)=_____。已知 25℃时 Ksp[Al(OH)3]=1.3×10-33。
(5)用惰性电极电解获得金属铜时,起始阶段阳极产物与阴极产物的物质的量之比为___________。
【答案】NaOH溶液 Fe2+ KSCN溶液和新制氯水 3.2~4.0 5ClO-+2Fe2++5H2O=2Fe(OH)3↓+Cl-+4HClO 1.3×10-6.9mol/L 1:1
【解析】
矿渣中含有Cu2O、Al2O3、Fe2O3和SiO2,加入硫酸酸浸,Cu2O、Al2O3、Fe2O3都与硫酸反应二氧化硅不反应,过滤后得到的固体A中含有Cu和SiO2,滤液中含有亚铁离子、铜离子、铝离子,加入NaClO氧化并调节pH,可得到氢氧化铁沉淀,在滤液中继续加入氢氧化钠溶液调节pH,可得到氢氧化铝沉淀,过滤后滤液中含有铜离子,电解可得到铜,以此解答该题。
(1)由以上分析可知固体A主要由SiO2、Cu组成,SiO2溶于氢氧化钠,从固体A 中分离出 Cu 的可用NaOH溶液;
(2)2Fe3++Cu=2Fe2++Cu2+,由于固体A中含有单质铜,可知酸浸、过滤后,滤液中铁元素的存在形式为Fe2+;加入KSCN溶液不变红,再滴入新制氯水变红,则证明含有Fe2+,检验Fe2+的常用化学试剂是KSCN溶液和新制氯水;
(3)沉淀B为Fe(OH)3,为保证Fe3+完全沉淀,而其它离子不沉淀,所以加 NaClO 氧化并调整溶液的pH为3.2~4.0,根据题意,反应得到沉淀Fe(OH)3和一种具有漂白性的物质 D,D是次氯酸,该反应离子方程式为5ClO-+2Fe2++5H2O=2Fe(OH)3↓+Cl-+4HClO;
(4)25℃时,加 NaOH 固体调节溶液 pH 得到Al(OH)3沉淀,若 pH=5.3 时,所得 溶液中 c(Al3+)= =1.3×10-6.9mol/L。
=1.3×10-6.9mol/L。
(4)氧化过程加入了次氯酸钠,还原产物是氯离子,所以用惰性电极电解获得金属铜时,起始阶段阳极产物是氯气、阴极产物是铜,根据电荷守恒,阳极产物与阴极产物的物质的量之比为1:1。


科目:高中化学 来源: 题型:
【题目】硫酸锰是一种重要的化工中间体,是锰行业研究的热点。一种以高硫锰矿(主要成分为含锰化合物及FeS)为原料制备硫酸锰的工艺流程如下:
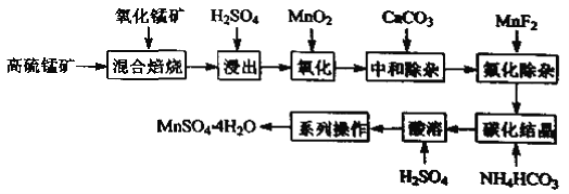
已知:①“混合焙烧”后烧渣含MnSO4、Fe2O3及少量FeO、Al2O3、MgO。
②金属离子在水溶液中的平衡浓度与pH的关系如图所示(25℃):
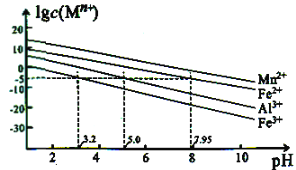
③此实验条件下Mn2+开始沉淀的pH为7.54;当离子浓度≤105mol·L1时,可认为离子沉淀完全。
请回答:
(1)传统工艺处理高硫锰矿时,不经“混合焙烧”,而是直接用H2SO4浸出,其缺点为____。
(2)“氧化”时,发生反应的离子方程式为____。若省略“氧化”步骤,造成的后果是____。
(3)“中和除杂”时,生成沉淀的主要成分为____(填化学式)。
(4)“氟化除杂”时,若使溶液中的Mg2+和Ca2+沉淀完全,需维持c(F-)不低于____。(已知:Ksp(MgF2)=6.4×1010;Ksp(CaF2)=3.6×1012)
(5)“碳化结晶”时,发生反应的离子方程式为_____。
(6)用惰性电极电解MnSO4溶液可制备MnO2,电解过程中阳极的电极反应式为____。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】A、B、C、D均为四种短周期元素,它们的原子序数依次增大。A与其他几种元素均不在同一周期;B元素最高价氧化物对应的水化物能与其最简单氢化物反应生成一种盐X;C能形成两种常温下为液态的氢化物;D与C同主族。则下列说法中不正确的是( )
A.原子半径大小关系:A<C<B
B.在0.1molL-1的X溶液中,溶液中阳离子的数目小于0.1NA
C.C、D两种元素分别与A形成的最简单化合物的沸点C比D的要高
D.化合物X受热易分解
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】中国科学院院士张青莲教授曾主持测定了铟(49In)等9种元素相对原子质量的新值,被采用为国际新标准。已知:铟与铝(13Al)同主族。下列说法错误的是( )
A.In的金属性大于Al
B.In最外层有2种能量的电子
C.![]() In的中子数为66
In的中子数为66
D.![]() In原子的相对原子质量为115
In原子的相对原子质量为115
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】捕获二氧化碳生成甲酸的过程如图所示。下列说法正确的是(NA为阿伏加德罗常数的值)
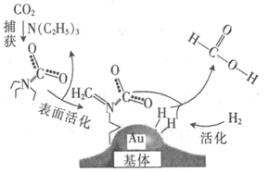
A.标准状况下,22.4 L CO2中所含的电子数目为16NA
B.10.1 g N(C2H5)3中所含的极性共价键数目为2.1NA
C.2 mol Au与2 mol H2中所含的分子数目均为2NA
D.100 g 46%的甲酸水溶液中所含的氧原子数目为5NA
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在容积为2 L的密闭容器中,有反应mA(g)+nB(g)![]() pC(g)+qD(g),经过5 min达到平衡,此时各物质的变化为A物质的量浓度减少amol·L-1,B的平均反应速率v(B)=a/15 mol·L-1·min-1,C物质的量浓度增加2a/3 mol·L-1,这时若增大系统压强,发现A与C的百分含量不变,则m∶n∶p∶q为( )
pC(g)+qD(g),经过5 min达到平衡,此时各物质的变化为A物质的量浓度减少amol·L-1,B的平均反应速率v(B)=a/15 mol·L-1·min-1,C物质的量浓度增加2a/3 mol·L-1,这时若增大系统压强,发现A与C的百分含量不变,则m∶n∶p∶q为( )
A.3∶1∶2∶2B.1∶3∶2∶2C.3∶1∶2∶1D.1∶1∶1∶1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】将0.2 mol·L-1的KOH溶液与0.1 mol·L-1的H2SO3溶液等体积混合后,溶液中各粒子浓度大小关系正确的是( )
A.c(K+)+c(H+)=c(OH-)+c(![]() )+c(
)+c(![]() )
)
B.2c(K+)=c(![]() )+c(
)+c(![]() )+c(H2SO3)
)+c(H2SO3)
C.c(K+)>c(![]() )>c(
)>c(![]() )>c(H2SO3)
)>c(H2SO3)
D.c(![]() )+c(
)+c(![]() )+c(H2SO3)=0.1 mol·L-1
)+c(H2SO3)=0.1 mol·L-1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】最近科学家获得了一种稳定性好、抗氧化能力强的活性化合物A;其结构如下:
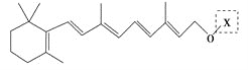
为了研究X的结构,将化合物A在一定条件下水解只得到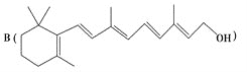 和C。经元素分析及相对分子质量测定,确定C的分子式为C7H6O3,C遇FeCl3水溶液显紫色,与NaHCO3溶液反应有CO2产生。
和C。经元素分析及相对分子质量测定,确定C的分子式为C7H6O3,C遇FeCl3水溶液显紫色,与NaHCO3溶液反应有CO2产生。
请回答下列问题:
(1)化合物B能发生下列哪些类型的反应________。
A.取代反应 B.加成反应
C.缩聚反应 D.氧化反应
(2)写出化合物C所有可能的结构简式______________________________。
(3)C可通过下图所示途径合成,并制取冬青油和阿司匹林。
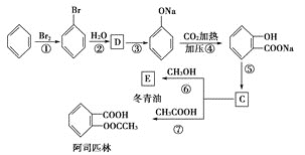
(ⅰ)写出有机物的结构简式:D:______________,C:________________,E:______________。
(ⅱ)写出变化过程中①、⑥的化学方程式(注明反应条件)
反应①__________________________________;反应⑥_____________________________。
(ⅲ)变化过程中的②属于____________反应,⑦属于________反应。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法错误的是
A.中和热测定实验中需要的玻璃仪器有:烧杯、量筒、温度计、环形玻璃搅拌棒
B.乙烯的燃烧热是1411.3kJ·mol-1,则乙烯燃烧的热化学方程式为:C2H4(g)+3O2(g)=2CO2(g)+2H2O(g)ΔH=-1411.3kJ·mol-1
C.P(s,红磷)=P(s,黑磷),ΔH=-39.3kJ·mol-1;P(s,白磷)=P(s,红磷),ΔH=-17.6kJ·mol-1由此推知,最稳定的磷单质是黑磷
D.MgCO3分解的能量关系如图所示: 则ΔH=ΔH1+ΔH2+ΔH3
则ΔH=ΔH1+ΔH2+ΔH3
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com