
【题目】下列说法正确的是
A.物质发生化学反应时都伴随着能量变化
B.吸热反应一定要在加热或高温条件下才能进行
C.浓硫酸溶于水时共价健断裂并放出大量的热,所以该过程是放热反应
D.焰色反应有能量变化,所以焰色反应是化学反应
 尖子生新课堂课时作业系列答案
尖子生新课堂课时作业系列答案 英才计划同步课时高效训练系列答案
英才计划同步课时高效训练系列答案科目:高中化学 来源: 题型:
【题目】金属元素及其化合物在科学研究和生产生活中有着广泛的用途
(1)氢气还原氧化铜时,产生的红色物质,冷却后加入稀硫酸发现溶液呈淡蓝色,写出该现象发生的离子方程式__________________________。
(2)取铝合金(含铝90%)1.5 g 与适量的 盐酸恰好完全反应(合金中其它成分不参加反应)。滤去不溶物,向滤液加入0.6 molL-1 的氨水使Al3+ 恰好完全沉淀。上述铝合金和盐酸反应的过程中生成氢气_____L(标准状况)。使Al3+ 恰好完全沉淀时,消耗氨水____mL。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】三氯化铬是合成其它铬盐的重要原料,在无机合成和有机合成中有重要的作用,是合成饲料添加剂的主要成份,工业上主要用作媒染剂及催化剂.易溶于水,溶于乙醇,几乎不溶于乙醚,易潮解,易升华.在高温下能被氧气氧化,碱性条件下能被H2O2氧化为Cr(Ⅵ)且2CrO42﹣+2H+Cr2O72﹣+H2O.制三氯化铬的流程如下: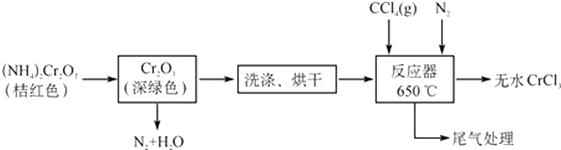
(1)三氯化铬碱性条件下被H2O2氧化为Cr(Ⅵ)的离子反应方程式为 .
(2)已知CCl4沸点为57.6℃,为保证稳定的CCl4气流,适宜的加热方式是 .
(3)用如图装置制备CrCl3时,主要步骤包括: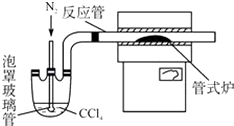
①将产物收集到蒸发皿中;②加热反应管至400℃,开始向三颈烧瓶中通入氮气,继续升温到650℃;③三颈烧瓶中装入150mLCCl4 , 并加热CCl4 , 温度控制在50~60℃之间;④反应管出口端出现了CrCl3升华物时,切断加热管式炉的电源;⑤停止加热CCl4 , 继续通入氮气;⑥检查装置气密性.
正确的操作顺序为:⑥→③→ , 步骤②中通如氮气的作用 .
(4)已知反应管中发生的主要反应有:Cr2O3+3CCl4→2CrCl3+3COCl2 , 因光气剧毒,实验需在通风橱中进行,并用乙醇处理COCl2 , 生成一种含氧酸酯(C5H10O3),用乙醇处理尾气的化学方程式 .
(5)样品中三氯化铬质量分数的测定称取样品0.3300g,加水溶解并定容于250mL容量瓶中.移取25.00mL于碘量瓶(一种带塞的锥形瓶)中,加热至沸后加入1gNa2O2 , 充分加热煮沸,适当稀释,然后加入过量的2mol/LH2SO4至溶液呈强酸性,此时铬以Cr2O72﹣存在,再加入1.1gKI,密塞,摇匀,于暗处静置5分钟后,加入1mL指示剂,用0.0250mol/L硫代硫酸钠溶液滴定至终点,平行测定三次,平均消耗标准硫代硫酸钠溶液24.00mL.已知:Cr2O72﹣+6I﹣+14H+=2Cr3++3I2+7H2O,2Na2S2O3+I2═Na2S4O6+2NaI.
①指示剂为 , 滴定终点的现象为 .
②移入碘量瓶的CrCl3溶液需加热煮沸,加入Na2O2后也要加热煮沸,其主要原因是 .
③样品中无水三氯化铬的质量分数为 . (计算结果精确到0.1%)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】镍具有铁磁性和延展性,能导电和导热。镍单质及其化合物的化学性质与铁相似。
(1)镍易溶于稀的无机酸中,并放出氢气,写出镍与盐酸反应的化学方程式:_____________。
(2)在隔绝空气的条件下,加热NiC2O4使其分解,就能得到暗绿色的氧化亚镍,写出该反应的化学方程式: _____________。
(3)Ni2O3不溶于水,可溶于盐酸并放出氯气,写出该反应的离子方程式: _____________。
(4)氢镍电池是一种碱性可充电电池,污染小,比能量较大。氢镍电池的总反应式是:H2+2NiO(OH) ![]() 2Ni(OH)2。写出放电时的正极反应式: _____________。
2Ni(OH)2。写出放电时的正极反应式: _____________。
(5)纳米材料镍粉(Ni)是一种高性能电极材料,其制备过程如下:
步骤I:取0.2mol/L的硝酸亚镍溶液,调节pH除铁后,加入活性炭过滤。
步骤Ⅱ:向所得滤液中滴加1.5mol/L的NaHCO3溶液使Ni2+完全沉淀,生成:xNiCO3·yNi(OH)2·zH2O。
步骤Ⅲ:将产生的沉淀用大量高纯水清洗并用离心机甩干。
步骤Ⅳ:加入稍过量的肼溶液(N2H4·H2O),使上述沉淀还原完全,将生成的Ni水洗后,再用95%的乙醇浸泡后晾干。为测定xNiCO3·yNi(OH)2·zH2O的组成,进行如下实验:
①准确称取7.54g样品与过量的肼溶液(N2H4·H2O)充分反应,共收集到1.12LN2和CO2的混合气体(已换算成标准状况)。
②另取等质量的样品充分灼烧,冷却后称得残留固体NiO的质量为4.5g。
通过计算确定xNiCO3·yNi(OH)2·zH2O的化学式_______________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】A是一种常见的单质,B、C为中学化学常见的化合物,A、B、C均含有元素X。它们有如图所示的转化关系(部分产物及反应条件已略去)。下列说法中不正确的是 ( )
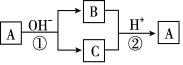
A. X元素可能为Al B. X元素一定为非金属元素
C. A可能是Cl2 D. 反应①和②一定为氧化还原反应
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】用漂白粉溶液浸泡过的有色布条,如晾晒在空气中,过一段时间,其漂白效果更好的原因是:
A. 漂白粉被氧化了
B. 漂白粉和空气中的二氧化碳充分反应生成了次氯酸
C. 有色布条被空气中的氧气氧化
D. 漂白粉溶液失去了部分水分,浓度增大了
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com