
CO、H2在一定条件下合成乙醇:2CO(g)+4H2(g)CH3CH2OH(g)+H2O(g) △H=—255.6 kJ·mol—1,下列说法错误的是( )
A.反应物的总能量大于生成物的总能量
B.增大H2浓度可以使CO转化率达到100℅
C.使用合适的催化剂、升高温度均可加大反应速率
D.反应达到平衡时,正反应和逆反应的化学反应速率相等且不为零
 新非凡教辅冲刺100分系列答案
新非凡教辅冲刺100分系列答案科目:高中化学 来源: 题型:阅读理解
| 实验组 | 温度/℃ | 起始量/mol | 平衡量/mol | 达到平衡所需时间/min | |
| H2O | CO | H2 | |||
| 1 | 650 | 2 | 4 | 1.6 | 5 |
| 2 | 900 | 2 | 4 | 0.9 | t |
查看答案和解析>>
科目:高中化学 来源: 题型:
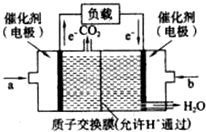
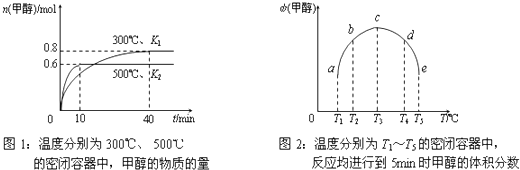
 (2012?梧州模拟)已知CO和H2在一定条件下合成甲醇的反应为:CO(g)+2H2(g)?CH3OH(g)现在容积均为1L的a、b、c三个密闭容器中分别充入1mol CO和2mol H2的混合气体,控制在不同的温度下进行反应,5min时测得相关数据的关系如图所示.下列说法正确的是( )
(2012?梧州模拟)已知CO和H2在一定条件下合成甲醇的反应为:CO(g)+2H2(g)?CH3OH(g)现在容积均为1L的a、b、c三个密闭容器中分别充入1mol CO和2mol H2的混合气体,控制在不同的温度下进行反应,5min时测得相关数据的关系如图所示.下列说法正确的是( )查看答案和解析>>
科目:高中化学 来源: 题型:阅读理解
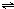 ClO(g)+3H2(g)△H>0.
ClO(g)+3H2(g)△H>0.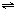 CH3OH(g)△H=-90.1kJ?mol-1,恒容条件下达平衡,下列措施中能使n(CH3OH)/n(CO)增大的有
CH3OH(g)△H=-90.1kJ?mol-1,恒容条件下达平衡,下列措施中能使n(CH3OH)/n(CO)增大的有
查看答案和解析>>
科目:高中化学 来源: 题型:
| △H1-△H2 |
| 2 |
| △H1-△H2 |
| 2 |
查看答案和解析>>
科目:高中化学 来源: 题型:阅读理解
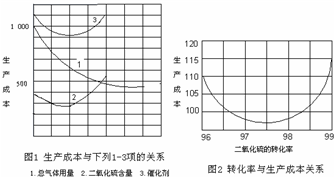
 2SO3(g)△H<0
2SO3(g)△H<0
| 1 |
| 2 |
| 1 |
| 2 |
| 1 |
| 2 |
| 1 |
| 2 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com