
| A. | 实验室中进行可燃性气体燃烧性质实验时,必须先验纯,后点燃 | |
| B. | 不慎将浓碱沾到皮肤上,应立即用大量水冲洗,然后涂上硼酸溶液 | |
| C. | 配制稀硫酸时,可先在量筒中加一定体积的水,再在搅拌下慢慢加入浓硫酸 | |
| D. | 不慎将酸溅到眼中,应立即用水冲洗,边洗边眨眼睛 |
分析 A.可燃性气体燃烧时先检验纯度,以免爆炸;
B.浓碱沾到皮肤上,用大量的水冲洗,以降低浓度,硼酸酸性较弱,可中和;
C.不能在量筒中稀释;
D.酸液溅到眼中,应立即用水冲洗,以降低浓度.
解答 解:A.不纯的可燃性气体点燃易导致爆炸,可燃性气体燃烧时先检验纯度,故A正确;
B.浓碱沾到皮肤上,用大量的水冲洗,以降低浓度,硼酸酸性较弱,且不具有腐蚀性,可用硼酸中和,故B正确;
C.量筒只能用于量取一定体积的液体,不能在量筒中稀释,故C错误;
D.酸液溅到眼中,应立即用水冲洗,以降低浓度,降低危害,故D正确.
故选C.
点评 本题考查化学实验的评价,侧重考查实验安全问题的处理,有利于培养学生的分析能力和实验能力,能培养学生良好的实验行为、意识,难度不大.


 开心快乐假期作业暑假作业西安出版社系列答案
开心快乐假期作业暑假作业西安出版社系列答案 名题训练系列答案
名题训练系列答案科目:高中化学 来源: 题型:解答题
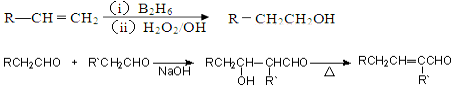
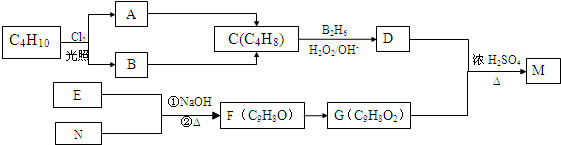
 、
、 ;
; $→_{△}^{浓H_{2}SO_{4}}$
$→_{△}^{浓H_{2}SO_{4}}$ +H2O.
+H2O.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | Al(OH)3 | B. | Cu(OH)2 | C. | Mg(OH)2 | D. | Al2O3 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 达到化学平衡时,4v正(O2)=5v逆(NO) | |
| B. | 若单位时间内生成x mol NO的同时,消耗x mol NH3,则反应达到平衡状态 | |
| C. | 达到化学平衡时,NH3(g)、O2(g) NO(g)、H2O(g)的浓度比为4:5:4:6 | |
| D. | 化学反应速率关系是:2v正(NH3)=3v正(H2O) |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| 反应阶段 | 溶液中的存在的金属离子 | 残留的金属粉末 | 发生的离子反应 |
| 第一阶段 | 只有一种 | 有两种 | (1) |
| 第二阶段 | 只有一种 | 只有一种 | |
| 第三阶段 | 只有两种 | (2) | (3) |
| 笫四阶段 | 有三种 | (4) | |
| 笫五阶段 | (5) |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
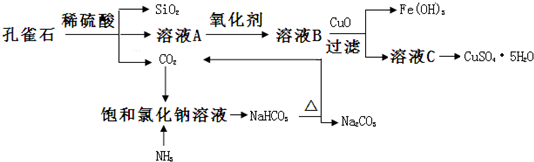
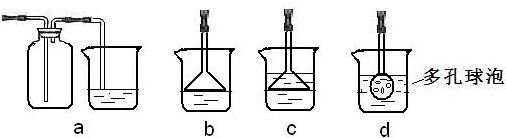
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com