
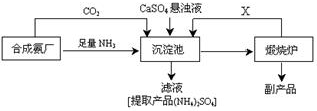
分析 由制备(NH4)2SO4的工艺流程可知,合成氨的反应在合成塔中进行,发生的反应为N2+3H2$?_{催化剂}^{高温、高压}$2NH3,在沉淀池中二氧化碳、氨气、硫酸钙反应生成碳酸钙和(NH4)2SO4,过滤得到滤液中含(NH4)2SO4,在煅烧炉中发生CaCO3$\frac{\underline{\;高温\;}}{\;}$CaO+CO2↑,则CO2可在此制备实验中循环使用,得到副产品为CaO,以此来解答.
解答 解:(1)合成氨反应的化学方程式是N2+3H2$?_{催化剂}^{高温、高压}$2NH3,该反应在合成塔中发生,淀池中发生的主要反应方程式是CaSO4+CO2+2NH3+H2O═CaCO3↓+(NH4)2SO4,该反应能够发生的原因是生成的CaCO3溶解度小于CaSO4有利于反应向正向进行,
故答案为:N2+3H2$?_{催化剂}^{高温、高压}$2NH3;合成塔;CaSO4+CO2+2NH3+H2O═CaCO3↓+(NH4)2SO4;生成的CaCO3溶解度小于CaSO4有利于反应向正向进行;
(2)在上述流程的沉淀池中通入足量氨气的目的是一方面提供反应物,另一方面使溶液呈碱性有利于CO2的吸收,在煅烧炉中发生CaCO3$\frac{\underline{\;高温\;}}{\;}$CaO+CO2↑,则X为CO2可在此制备实验中循环使用,
故答案为:一方面提供反应物,另一方面使溶液呈碱性有利于CO2的吸收;CO2;
(3)煅烧炉中发生CaCO3$\frac{\underline{\;高温\;}}{\;}$CaO+CO2↑,则得到副产品为生石灰,从绿色化学和资源综合利用的角度说明上述流程的主要优点是该流程中,产生的CO2循环使用,得到的产品和副产品都是有用的物质,无废物产生,从物质的性质和工业生产实际的角度考虑该流程主要缺陷是由于CaSO4的溶解度较小,此反应的产率会比较低,
故答案为:生石灰;该流程中,产生的CO2循环使用,得到的产品和副产品都是有用的物质,无废物产生;由于CaSO4的溶解度较小,此反应的产率会比较低.
点评 本题考查物质的制备实验,为高频考点,把握制备流程、发生的反应、实验技能为解答的关键,侧重分析与实验能力的综合考查,题目难度不大.


科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 范德华力 | B. | 共价键 | C. | 氢键 | D. | 离子键 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | X、Y的单质均具有较高的熔沸点 | |
| B. | 最高价氧化物对应水化物的酸性由强到弱的顺序:W、Y、X | |
| C. | 原子半径由大到小的顺序:X、Y、Z | |
| D. | Z、W形成的化合物中既含有离子键,又含有共价键 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 氢是宇宙物质中含量最多的元素 | |
| B. | 氢是名副其实的碱金属元素 | |
| C. | 氢气是无污染的新型能源 | |
| D. | 固态“金属氢”汽化的过程属于物理变化 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 醋酸、纯碱、氯化钠 | B. | 硝酸、生石灰、硫酸钡 | ||
| C. | 盐酸、熟石灰、石英 | D. | 硫酸、烧碱、碳酸氢钠 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
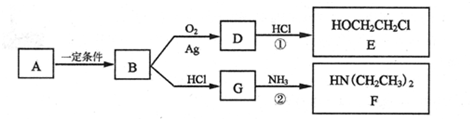
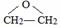 .
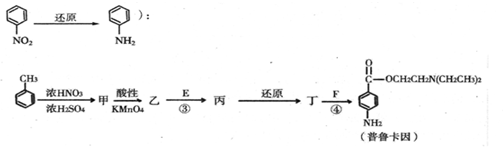
.
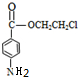 ;
; ;
;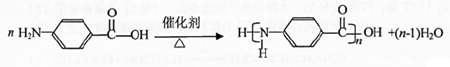 .
.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 海水提溴过程中,提取溴单质只能用有机物萃取的方法 | |
| B. | 电解饱和食盐水可制得金属钠 | |
| C. | 海水晒盐过程中主要涉及物理变化 | |
| D. | 海带提碘中,氧化过程可通入过量的氯气 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com