

| 选项 | 溶液M | 物质X | 物理量y |
| A | 含Mg2+、Al3+、NH4+的溶液 | KOH溶液 | 沉淀的物质的量 |
| B | 含CO32-、HCO3-的溶液 | 盐酸 | 二氧化碳的体积 |
| C | 含OH-、AlO2-、SiO3 2-、CO32-的溶液 | NaHSO4溶液 | 沉淀的质量 |
| D | 含Ba(OH)2、NaOH、NaAlO2的溶液 | CO2 | 沉淀的物质的量 |
| A. | A | B. | B | C. | C | D. | D |
分析 A.含Mg2+、Al3+、NH4+的溶液 中滴入KOH溶液开始有沉淀生成,沉淀达到最大量,和铵根离子反应生成一水合氨,氢氧化铝溶解最后沉淀不变;
B.含CO32-、HCO3-的溶液滴入盐酸和碳酸根离子反应生成碳酸氢根离子,滴入生成二氧化碳气体;
C.含OH-、AlO2-、SiO3 2-、CO32-的溶液滴入NaHSO4溶液,显和氢氧根离子反应生成水,和AlO2-、SiO3 2-反应生成氢氧化铝沉淀和硅酸沉淀,继续和碳酸根离子反应,最后氢氧化铝沉淀溶解,剩余硅酸沉淀;
D.含Ba(OH)2、NaOH、NaAlO2的溶液通入CO2气体和氢氧根离子反应,开始生成沉淀碳酸钡,随反应进行生成氢氧化铝沉淀,二氧化碳和碳酸钡反应生成碳酸氢钡溶于水,氢氧化铝沉淀不溶解.
解答 解:A.含Mg2+、Al3+、NH4+的溶液 中滴入KOH溶液开始有沉淀生成,沉淀达到最大量,和铵根离子反应生成一水合氨,氢氧化铝溶解最后沉淀不变,图象中开始错误,故A错误;
B.含CO32-、HCO3-的溶液滴入盐酸和碳酸根离子反应生成碳酸氢根离子,继续滴入生成二氧化碳气体,最后达到不变,故B错误;
C.含OH-、AlO2-、SiO3 2-、CO32-的溶液滴入NaHSO4溶液,先和氢氧根离子反应生成水,和AlO2-、SiO3 2-反应生成氢氧化铝沉淀和硅酸沉淀,继续和碳酸根离子反应,出现平台,最后氢氧化铝沉淀溶解,剩余硅酸沉淀不变,曲线变化符合,故C正确;
D.含Ba(OH)2、NaOH、NaAlO2的溶液通入CO2气体和氢氧根离子反应,开始生成沉淀碳酸钡,图象变化不符合,随反应进行生成氢氧化铝沉淀,二氧化碳和碳酸钡反应生成碳酸氢钡溶于水,氢氧化铝沉淀不溶解,故D错误;
故选C.
点评 本题考查了离子性质、反应生成沉淀和生成气体的量的变化,注意沉淀生成合成的溶解的性质判断,掌握基础是解题关键,题目难度中等.


科目:高中化学 来源: 题型:选择题
| A. | NaHSO4和Ba(OH)2 | B. | AlCl3和NaOH | C. | NaAlO2和H2SO4 | D. | Na2CO3和HCl |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 上述反应中氧化剂和还原剂的物质的量之比为5:6 | |
| B. | 产生白色烟雾的原因是生成的P2O5白色固体小颗粒(烟)吸水性很强,吸收空气中的水分,生成酸滴(雾) | |
| C. | 上述反应中消耗3molP时,转移电子的物质的量为15mol | |
| D. | 产物P2O5为酸性氧化物,但不是磷酸的酸酐 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题

| A. | 电子从Zn极流出,流入Fe极,经盐桥回到Zn极 | |
| B. | 烧杯b中发生的电极反应为Zn-2e-═Zn2+ | |
| C. | 烧杯a中发生反应O2+4H++4e-═2H2O,溶液pH降低 | |
| D. | 向烧杯a中加入少量KSCN溶液,则溶液会变成红色 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | ①③④ | B. | ②③⑤ | C. | ②④⑤ | D. | 全部 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 发现了电子 | B. | 根据α提出了带核的原子结构模型 | ||
| C. | 引入的量子学说 | D. | 提出较为系统的化学原子学说 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | NH3常用作制冷剂 | B. | 烧碱:治疗胃酸过多的一种药剂 | ||
| C. | Na2SiO3常用作制木材防火剂 | D. | NaHCO3常用作面粉发泡剂 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | NH3$→_{催化剂}^{O_{2}}$NO$\stackrel{NaOH溶液}{→}$NaNO3 | |
| B. | Fe2O3$→_{高温}^{Al}$Fe$→_{点燃}^{Cl_{2}}$FeCl3 | |
| C. | SiO2$→_{△}^{H_{2}O}$H2SiO3$\stackrel{NaOH溶液}{→}$NaSiO3 | |
| D. | NaSO4溶液$\stackrel{BaCl_{2}溶液}{→}$BaSO4$\stackrel{盐酸}{→}$BaCl2 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
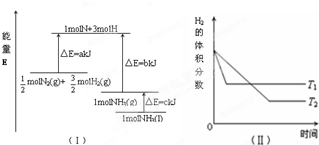
| A. | 该反应的热化学方程式:$\frac{1}{2}$N2(g)+$\frac{3}{2}$H2(g)=NH3(g)△H=-(b-a)kJ•mol-1 | |
| B. | 该反应的热化学方程式:N2(g)+3H2(g)=2NH3(1)△H=2(a-b-c)kJ•mol-1 | |
| C. | T1>T2,且正反应为放热反应 | |
| D. | 其他条件不变,升高温度,正、逆反应速率均增大,且H2的转化率增大 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com