
【题目】磁性材料A由两种元素组成,为探究其组成和性质,设计并完成如下实验:

(1) A的化学式为______。
(2) 用化学方程式表达气体C与氯水反应生成D的过程:________。
(3) B溶于盐酸后生成的物质F可用于净水,其原因是____________。
【答案】Fe3S4 Cl2+SO2+2H2O=H2SO4+2HCl Fe3+水解生成了氢氧化铁胶体,能吸附水中悬浮的小颗粒,达到净水的目的
【解析】
无色气体C与足量的氯水反应得到溶液D,D中加入氯化钡溶液和盐酸溶液,有白色沉淀E生成,故E为BaSO4,D为硫酸和盐酸的混合液,C为二氧化硫。B溶于盐酸后生成的物质F可用于净水,再结合其A由两种元素组成的磁性材料,可知,B为三氧化二铁,然后分析;
(1)氧化铁的质量为2.400g,其物质的量为![]() ,含铁原子的物质的量为0.030mol,则铁的质量为0.030 mol×56g/mol=1.680g,则化合物中硫元素的质量为2.960-1.680=1.280g,硫的物质的量为
,含铁原子的物质的量为0.030mol,则铁的质量为0.030 mol×56g/mol=1.680g,则化合物中硫元素的质量为2.960-1.680=1.280g,硫的物质的量为![]() ,则铁与硫的物质的量比为0.030:0.040=3:4,则化学式为:Fe3S4;
,则铁与硫的物质的量比为0.030:0.040=3:4,则化学式为:Fe3S4;
(2)二氧化硫与氯气在水中发生氧化还原反应生成硫酸和盐酸,氯气作氧化剂,二氧化硫作还原剂,反应的化学方程式为:Cl2+SO2+2H2O=H2SO4+2HCl;
(3) B为三氧化二铁,溶于盐酸后生成的物质F可用于净水即为三价铁离子水解:Fe3++3H2O![]() Fe(OH)3+3H+,Fe3+水解生成了氢氧化铁胶体,能吸附水中悬浮的小颗粒,达到净水的目的。
Fe(OH)3+3H+,Fe3+水解生成了氢氧化铁胶体,能吸附水中悬浮的小颗粒,达到净水的目的。


科目:高中化学 来源: 题型:
【题目】海水中含有大量Na+、C1-及少量Ca2+、Mg2+、SO42-,用电渗析法对该海水样品进行淡化处理,如右图所示。下列说法正确的是
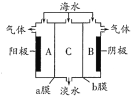
A. b膜是阳离子交换膜
B. A极室产生气泡并伴有少量沉淀生成
C. 淡化工作完成后A、B、C三室中pH大小为pHA<pHB<pHC
D. B极室产生的气体可使湿润的KI淀粉试纸变蓝
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】生产上用过量烧碱溶液处理某矿物(含Al2O3、MgO),过滤后得到滤液用NaHCO3溶液处理,测得溶液pH和Al(OH)3生成的量随加入NaHCO3溶液体积变化的曲线如下:
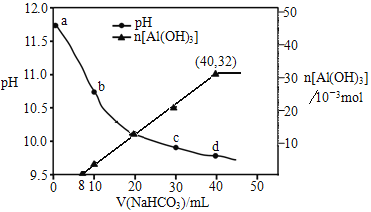
下列有关说法不正确的是
A. NaHCO3溶液的物质的量浓度为0.8 mol/L
B. b点与c点溶液所含微粒种类相同
C. a点溶液中存在的离子是Na+、AlO2-、OH-、H+
D. 生成沉淀的离子方程式为:HCO3-+AlO2-+H2O === Al(OH)3↓+CO32-
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】有下列物质:
①硫酸 ②盐酸 ③氯气 ④硫酸钡 ⑤酒精 ⑥铜 ⑦醋酸 ⑧氯化氢 ⑨蔗糖 ⑩氨气 CO2 NaHCO3 A l(OH)3 NaOH
(1)属于非电解质的为____(填序号,下同),属于弱电解质的为___,能导电的是___。
(2)写出下列反应的离子方程式
①NaHCO3溶于醋酸:______________________。
②过量CO2与NaOH溶液反应:______________。
③Cl2通入NaOH溶液中:___________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】
黄铜矿是主要的炼铜原料,CuFeS2是其中铜的主要存在形式。回答下列问题:
(1)CuFeS2中存在的化学键类型是_______。其组成的三种元素中电负性较强的是 _______。
(2)下列基态原子或离子的价层电子排布图正确的______。
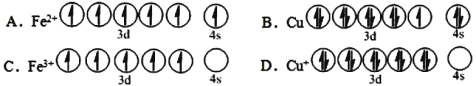
(3)在较低温度下CuFeS2与浓硫酸作用时,有少量臭鸡蛋气味的气体X产生。
①X分子的立体构型是____,中心原子杂化类型为____,属于_______(填“极性”或“非极性”)分子。
②X的沸点比水低的主要原因是___________。
(4)CuFeS2与氧气反应生成SO2,其结构式为![]() ,则SO2中共价键类型有_________。
,则SO2中共价键类型有_________。
(5)四方晶系CuFeS2晶胞结构如图所示。
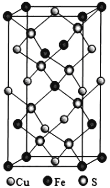
①Cu+的配位数为__________,
②已知:a=b=0.524 nm,c=1.032 nm,NA为阿伏加德罗常数的值,CuFeS2晶体的密度是________gcm3(列出计算式)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】为研究铜与浓硫酸的反应,某化学兴趣小组进行如下实验。
实验I:反应产物的定性探究,按如图装置(固定装置已略去)进行实验:
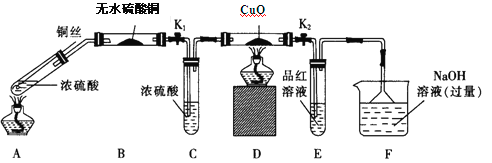
(1)F装置的烧杯中发生反应的离子方程式是_____________;B装置中的现象是__________。
(2)实验过程中,能证明浓硫酸中硫元素的氧化性强于氢元素的现象是_________。
(3)实验结束时,撤去所有酒精灯之前必须完成的实验操作是_________。
(4)实验结束后,证明A装置试管中反应所得产物是否含有铜离子的操作方法是_________。
实验Ⅱ:反应产物的定量探究
(5)在铜与浓硫酸反应的过程中,发现有黑色物质出现,且黑色物质为Cu2S。产生Cu2S的反应为aCu+bH2SO4=cCu2S+dCuSO4+eH2O,则a∶b=______
(6)为测定硫酸铜的产率,将该反应所得溶液中和后配制成250.00 mL溶液,取该溶液25.00 mL加入足量 KI溶液中振荡,以淀粉溶液为指示剂,用0.36 mol·L-1的Na2S2O3溶液滴定生成的I2,3次实验平均消耗该Na2S2O3溶液25.00 mL。若反应消耗铜的质量为6.4 g,则硫酸铜的产率为___。
(已知![]() )
)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】含硫化合物多为重要的化工原料。请回答下列问题:
I.多硫化物是含多硫离子(Sx2-)的化合物,可用作废水处理剂、硫化剂等。
(1)Na2S2的电子式为___。
(2)Na2S5(易溶于水)在酸性条件下可生成H2S和S,该反应的离子方程式为___。
(3)黄铁矿(FeS2)是工业上制硫酸的重要原料,在氧气中煅烧生成Fe2O3和SO2,其煅烧的化学方程式为___。
II.焦亚硫酸钠(Na2S2O5)是一种食品抗氧化剂,易溶于水。
(4)焦亚硫酸钠(Na2S2O5)中硫元素的化合价为___。
(5)向某些饮料中添加少量焦亚硫酸钠(Na2S2O5),可降低饮料中溶解氧的含量,发生反应的离子方程式为__。
(6)向饱和碳酸钠溶液中通入过量SO2可制得焦亚硫酸钠,发生反应的化学方程式为__。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知某有机物A的红外光谱和核磁共振氢谱图如下图所示,下列说法中不正确的是( )

A. 由红外光谱可知,该有机物中至少有三种不同的化学键
B. 由核磁共振氢谱图可知,该有机物分子中有三种不同的氢原子
C. 仅由其核磁共振氢谱图无法得知其分子中的氢原子总数
D. 若A的化学式为C2H6O,则其结构简式为CH3—O—CH3
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】厌氧氨化法是一种新型的氨氮去除技术,下列说法中正确的是( )
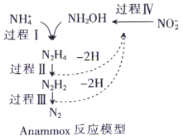
A.1molNH4+中所含的质子总数为10NA
B.1mol联氨(N2H4)中含有5mol共用电子对
C.NH2OH中既含有极性键也含有非极性键
D.该方法每处理1molNH4+,需要的NO2-为0.5mol
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com