
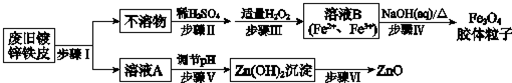
分析 根据实验流程图可知:废旧镀锌铁皮加入氢氧化钠溶液中反应,锌溶解生成偏锌酸钠和氢气,铁不溶解,过滤得到滤液A为Na2ZnO2,不溶物为Fe,溶液A调节pH使溶液中ZnO22-转化为Zn(OH)2沉淀,再经过抽滤、洗涤、干燥,灼烧得到ZnO;不溶物Fe中加入硫酸,反应生成硫酸亚铁,调节溶液PH=1~2,并加入适量过氧化氢,氧化部分亚铁离子为铁离子,得到含Fe2+、Fe3+的B溶液,再加入氢氧化钠溶液,加热分解生成四氧化三铁胶体粒子,
(1)步骤Ⅰ中所用的试剂是溶解锌分离;
(2)步骤Ⅲ是过氧化氢在酸性溶液中氧化亚铁离子为铁离子便于除去;
(3)步骤Ⅴ是溶液中Na2ZnO2和酸反应生成氢氧化锌沉淀;
(4)步骤Ⅵ的实验操作是氢氧化锌受热分解生成氧化锌和水;
解答 解:废旧镀锌铁皮加入氢氧化钠溶液中反应,锌溶解生成偏锌酸钠和氢气,铁不溶解,过滤得到滤液A为Na2ZnO2,调节溶液PH生成氢氧化锌沉淀,过滤、洗涤、灼烧得到氧化锌,不溶物为铁,溶于稀硫酸加入适量过氧化氢,调节溶液PH=1~2,部分氧化亚铁离子为铁离子,得到含Fe2+、Fe3+的B溶液,加热促进水解生成四氧化三铁胶体粒子,
(1)根据Zn及化合物的性质与Al及化合物的性质相似,Zn也能和氢氧化钠溶液反应,氢氧化钠溶液起到溶解镀锌层和去除油污作用,步骤Ⅰ所用的试剂是氢氧化钠溶液,
故答案为:氢氧化钠溶液;
(2)步骤Ⅲ是过氧化氢在酸性溶液中氧化亚铁离子为铁离子便于除去,反应的离子方程式为:2Fe2++2H++H2O2═2Fe3++2H2O,
故答案为:2Fe2++2H++H2O2═2Fe3++2H2O;
(3)步骤Ⅴ是溶液中Na2ZnO2和酸反应生成氢氧化锌沉淀,选项中的氢氧化钠溶液和氨水不能形成氢氧化锌沉淀,选盐酸,
故答案为:c;
(4)步骤Ⅵ的实验操作是氢氧化锌受热分解生成氧化锌和水,反应的化学方程式为:Zn(OH)2$\frac{\underline{\;\;△\;\;}}{\;}$ZnO+H2O,步骤Ⅵ的实验操作是灼烧(或加热),
故答案为:灼烧(或加热);
点评 本题以物质的制备为载体,考查实验基本操作和技能,物质的性质、氧化还原反应方程式的书写以及滴定实验等方面的综合知识,要求学生具有分析和解决问题的能力,题目难度中等.


科目:高中化学 来源: 题型:选择题
| A. | 为了抑制Fe2+的水解,用稀硝酸酸化 | |
| B. | 为了增强KMnO4溶液的氧化能力,用浓盐酸酸化 | |
| C. | 检验溶液中是否含有SO42-时,先用盐酸酸化 | |
| D. | 检验氯乙烷中的氯元素,水解后再用硫酸酸化 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| 实验编号 | 实验操作 | 实验现象 |
| ① | 滴入KSCN溶液 | 溶液变红色 |
| ② | 滴入AgNO3溶液 | 有黄色沉淀生成 |
| ③ | 滴入K3[Fe(CN)6]溶液 | 有蓝色沉淀生成 |
| ④ | 滴入淀粉溶液 | 溶液变蓝色 |
| A. | ①和② | B. | ②和④ | C. | ③和④ | D. | ①和③ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | Na+、Mg2+、SO42-、HCO3- | B. | Na+、Ba2+、Cl-、SO42- | ||
| C. | Cu2+、Ca2+、Cl-、NO3- | D. | Fe2+、K+、NO3-、Cl- |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| 成分 | 质量(g) | 摩尔质量(g/mol) |
| 蔗糖(C12H22O11) | 25.00 | 342 |
| 硫酸钾(K2SO4) | 0.25 | 174 |
| 高锰酸钾(KMnO4) | 0.25 | 158 |
| 阿司匹林(C9H8O4) | 0.17 | 180 |
| 硝酸银(AgNO3) | 0.02 | 170 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 氧化剂和还原剂混合不一定发生氧化还原反应 | |
| B. | 得电子越多的氧化剂,其氧化性就越强 | |
| C. | 阳离子只有氧化性,阴离子只有还原性 | |
| D. | 有单质参加且有单质生成的反应一定属于氧化还原反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com