
| A、大理石、石灰石、生石灰、CaCO3 |
| B、烧碱、纯碱、火碱、NaOH |
| C、熟石灰、消石灰、石灰乳、Ca(OH)2 |
| D、苏打、小苏打、纯碱、Na2CO3 |
科目:高中化学 来源: 题型:
| A、△H1>△H2>△H3 |
| B、△H1<△H3<△H2 |
| C、△H2>△H1>△H3 |
| D、△H1>△H3>△H2 |
查看答案和解析>>
科目:高中化学 来源: 题型:
A、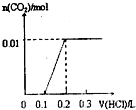 |
B、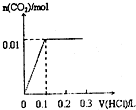 |
C、 |
D、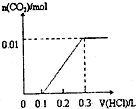 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、将少量二氧化硫通入次氯酸钠溶液中:SO2+H2O+ClO-=SO42-+Cl-+2H+ | ||||
| B、向含有Fe2O3悬浊液中通入HI气体:Fe2O3+6H+=2Fe3++3H2O | ||||
C、用惰性电极电解MgCl2溶液:2Cl-+2H2O
| ||||
| D、等物质的量的Ba(OH)2与(NH4)2Fe(SO4)2在溶液中反应:Ba2++2OH-+2NH4++SO42-=BaSO4↓+2NH3?H2O |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、钠与CuSO4溶液反应:2Na+Cu2+=Cu↓+2Na+ | ||||
| B、Na2S2O3溶液中加入稀硫酸:2S2O32-+4H+=SO42-+3S↓+2H2O | ||||
C、用铜做电极电解CuSO4溶液:2Cu2++2H2O
| ||||
| D、向FeCl3溶液中加入Mg(OH)2:3Mg(OH)2+2Fe3+=2Fe(OH)3+3Mg2+ |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、Fe(OH)3胶体粒子所作的布朗运动 |
| B、在电场作用下,Fe(OH)3胶体粒子在分散剂里作定向移动 |
| C、当光束通过Fe(OH)3胶体时,可以看到一条光亮的“通路” |
| D、向Fe(OH)3胶体中逐滴加入盐酸时会观察到先变浑浊再变澄清 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、属于氧化物 | B、属于硫酸盐 |
| C、属于钾盐 | D、属于电解质 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| 滴定次数 | 待测溶液体积(ml) | 标准盐酸体积(ml) | |
| 滴定前刻度(ml) | 滴定后刻度(ml) | ||
| 第一次 | 10.00 | 0.20 | 20.50 |
| 第二次 | 10.00 | 0.40 | 20.80 |
| 第三次 | 10.00 | 4.00 | 24.20 |
查看答案和解析>>
科目:高中化学 来源: 题型:

| 常温下状态 | 溶解性 | 稳定性 |
| 白色固体 | 易溶于水和乙醇,难溶于CCl4 | 在干燥空气中稳定,在湿空气中放出氨转化为NH4HC03,59时分解为NH3和CO2 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com