
【题目】钯(Pd)元素的原子序数为46,下列叙述错误的是( )
A. ![]() Pd和
Pd和 ![]() Pd互为同位素 B. Pd核外有46个电子
Pd互为同位素 B. Pd核外有46个电子
C. Pd核内有46个质子 D. ![]() Pd的原子核内有46个中子
Pd的原子核内有46个中子
 应用题作业本系列答案
应用题作业本系列答案科目:高中化学 来源: 题型:
【题目】下列关于细胞中化学元素和化合物说法错误的是
A. 活细胞中,含量最多的元素是H
B. 鸟嘌呤和胞嘧啶数量越多的DNA分子越稳定
C. 氨基酸、多肽链和蛋白质一般都含有氨基和羧基
D. 构成淀粉、纤维素和糖原的单体都相同
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某化学实验室产生的废液中含有Fe3+、Cu2+、Ba2+、Cl﹣四种离子,现设计下列方案对废液进行处理,以回收金属并制备氯化钡、氯化铁晶体. 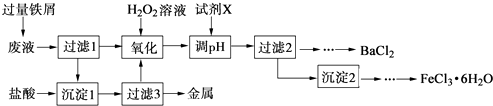
(1)沉淀1中含有的金属单质是 .
(2)氧化时加入H2O2溶液发生反应的离子方程式为 .
(3)下列物质中,可以作为试剂X的是 (填字母).
A.BaCl2
B.BaCO3
C.NaOH
D.Ba(OH)2
(4)检验沉淀2洗涤是否完全的方法是 .
(5)制备氯化铁晶体过程中需保持盐酸过量,其目的是 .
(6)由过滤2得到的滤液制备BaCl2的实验操作依次为、冷却结晶、、洗涤、干燥.
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某温度下,在体积为2L的密闭容器中充入1mol A和b mol B气体,发生如下反应:A(g)+B(g)2C(g),5min后反应达到平衡时n(A)为0.4mol.在反应过程中体系的温度持续升高,实验测得混合气体中C的含量与温度的关系如下图所示.下列叙述正确的是( ) 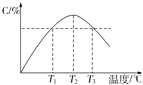
A.0~5 min,C物质的平均反应速率为0.04 molL﹣1min﹣1
B.图中温度T1时的正反应速率等于温度T3时的正反应速率
C.该反应温度T2时的平衡常数大于温度T3时的平衡常数
D.图中T2时,若只增大压强,则正、逆反应速率不改变
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】电离度是描述弱电解质电离程度的物理量,电离度=(已电离的电解质的物质的量/原来总的物质的量)×100%.现取20mL pH=3的 CH3COOH溶液,加入0.2molL﹣1的氨水,测得溶液导电性变化如图,则加入氨水前CH3COOH的电离度为( ) 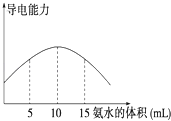
A.0.5%
B.1.5%
C.0.1%
D.1%
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】氨气是一种重要的化工产品,是生产铵盐、尿素等原料,工业合成氨的反应如下: N2(g)+3H2(g)2NH3(g)△H=一92.4KJmol﹣1
(1)已知H2(g)的燃烧热为285KJ/mol,写出NH3(g)在纯氧中燃烧生成无毒、无害物质的热化学方程式.
(2)25℃时,将a mol (NH4)2SO4溶于水,向该溶液中滴加V L稀氨水后溶液呈中性,则滴加氨水的过程中水的电离平衡将(填“正向”、“不”或“逆向”)移动,所滴加稀氨水的物质的量浓度为molL﹣1 . (25℃时,NH3H2O的电离平衡常数Kb≈2×10﹣5)
(3)工业上常通过如下反应合成尿素[CO(NH2)2]: CO2(g)+2NH3(g)CO(NH2)2(l)+H2O(g)△H<0,t℃时,向容积恒定为2L的密闭容器中加入0.10molCO2和0.40molNH3 . 反应中CO2( g)的物质的量随时间变化如表所示:
时间/min | 0 | 30 | 70 | 80 | 100 |
n(CO2)/mol | 0.10 | 0.060 | 0.040 | 0.040 | 0.040 |
①20min时,υ正(CO2 )80min时.υ逆(H2O)(填“>”、“=”或“<”).在t℃时,该反应额平衡常数表达式为K=;
②在100min时,保持其它条件不变,再向容器中充入0.050mo1CO2和0.20molNH3 , 重新建立平衡后CO2的转化率与原平衡相比将(填“增大”、“不变”或“减小”).
③上述可逆反应的平衡常数为(保留二位小数).
④根据表中数据在图甲中绘制出在t℃下NH3的转化率随时间变化的图象;保持其它条件不变;则(t+10)℃下正确的图象可能是(填图甲中的“A”或“B”). 
⑤图乙所示装置(阴、阳极均为惰性电极)可用于电解尿素〔CO(NH2)2〕的碱性溶液制取氢气.该装置中阳极的电极反应式为 , 若两极共收集到气体22.4L(标况),则消耗的尿素为g(忽略气体的溶解).
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知用硫酸酸化的草酸(H2C2O4)溶液能与KMnO4溶液反应.某化学小组研究发现,少量MnSO4可对该反应起催化作用.为进一步研究有关因素对该反应速率的影响,探究如下:
(1)常温下,探究不同的初始pH和草酸溶液浓度对反应速率的影响,设计如下实验,则A= , C= , E=
实验编号 | 温度 | 初始pH | 0.1mol/L草酸溶液体积/mL | 0.01mol/LKMnO4 | 蒸馏水体积/mL | 待测数据(混合液褪色时间/s) |
① | 常温 | 1 | 20 | 50 | 30 | t1 |
② | 常温 | A | B | C | 30 | t2 |
③ | 常温 | 2 | 40 | D | E | t3 |
(2)该反应的离子方程式 .
(3)若t1<t2 , 则根据实验①和②得到的结论是 .
(4)小组同学发现每组实验反应速率随时间的变化总是如图,其中t1~t2时间内速率变快的主要原因可能是: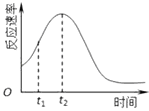
①;② .
(5)化学小组用滴定法测定KMnO4溶液物质的量浓度:取ag草酸晶体(H2C2O42H2O,摩尔质量126g/mol)溶于水配成250mL溶液,取25.00mL溶液置于锥形瓶中,加入适量稀H2SO4酸化,再用KMnO4溶液滴定至终点,重复滴定三次,平均消耗KMnO4溶液VmL.滴定到达终点的现象是:;实验中所需的定量仪器有(填仪器名称).该KMnO4溶液的物质的量浓度为mol/L.
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(题文)已知某反应中能量变化如图所示,所得结论错误的是( )

A. 该图像可以表示氯化铵与消石灰反应的能量变化
B. 该反应过程中,一定有其他形式的能量转化成化学能
C. 该反应过程中,形成新化学键释放的总能量小于断裂旧化学键吸收的总能量
D. 因为生成物的总能量高于反应物的总能量,所以该反应一定需要加热才可进行
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com