
科目:高中化学 来源: 题型:选择题
| 元素符号 | X | Y | Z | R | T |
| 原子半径(nm) | 0.160 | 0.111 | 0.104 | 0.143 | 0.066 |
| 主要化合价 | +2 | +2 | -2,+4,+6 | +3 | -2 |
| A. | 离子的还原性:T2->Z2- | |
| B. | 离子半径:Z2->X2+ | |
| C. | Y的原子序数大于X | |
| D. | X和Y的最高价氧化物的水化物的碱性:Y>X |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | BaSO4和BaCO3均难溶于水,均可用作“钡餐” | |
| B. | 轮船的外壳和铁锅等生锈主要发生了电化学腐蚀 | |
| C. | 钻石和水晶都是人们熟知的宝石,但其化学成分不同 | |
| D. | 硫酸铁和明矾都可用于净水 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| X | L | Z |
| Y | W |
| A. | Y的原子半径一定比L的大 | |
| B. | 若X、Y为非金属元素,则X、Y元素形成的单质晶体类型一定相同 | |
| C. | 若X、W能组成XW型分子,则其空间构型分子,则其空间构型一定为直线型 | |
| D. | 对应简单氢化物的沸点可能是X>Y、Z>W |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
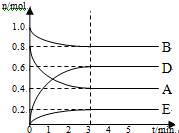 某温度T℃下,在某个固定容积为2.0L的密闭容器内,在时按右图所示发生反应:其中A、B、D为气体,E为固体.
某温度T℃下,在某个固定容积为2.0L的密闭容器内,在时按右图所示发生反应:其中A、B、D为气体,E为固体.查看答案和解析>>
科目:高中化学 来源: 题型:解答题
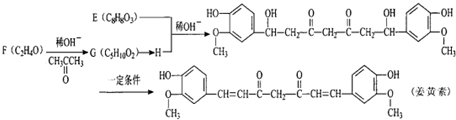
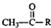 $\stackrel{稀OH-}{→}$
$\stackrel{稀OH-}{→}$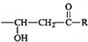
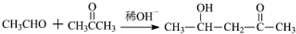 ,G→H的反应类型为氧化反应
,G→H的反应类型为氧化反应 ;将F滴人新制Cu(OH)2悬浊液,加热,观察到的现象是出现红色沉淀
;将F滴人新制Cu(OH)2悬浊液,加热,观察到的现象是出现红色沉淀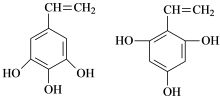
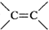
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com