
| A、用含氢氧化铝的药剂治疗胃酸过多 |
| B、用苏打中和发酵面团中的酸 |
| C、用醋酸清洗热水瓶内壁附着的水垢 |
| D、用二氧化硫熏蒸银耳 |


科目:高中化学 来源: 题型:
| A、称量时NaOH已经潮解 |
| B、定容时俯视容量瓶的标线 |
| C、向容量瓶中转移溶液时,容量瓶事先用蒸馏水洗涤过 |
| D、摇匀后发现液面低于标线,滴加蒸馏水至标线再摇匀 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、加入氯化钡溶液有白色沉淀产生,再加盐酸,沉淀不消失,则一定有SO42- |
| B、加入NaOH固体,产生的气体能使湿润红色石蕊试纸变蓝,则一定有NH4+ |
| C、先滴加氯水,再滴加KSCN溶液后显红色,则一定有Fe2+而没有Fe3+ |
| D、滴加硝酸银,生成白色沉淀,再滴加稀盐酸,沉淀不溶解,则含有Cl- |
查看答案和解析>>
科目:高中化学 来源: 题型:
| 被提纯的物质 [括号内物质是杂质] | 除杂试剂 | 除杂方法 | |
| A | CO(g)[CO2(g)] | NaOH溶液、浓H2SO4 | 洗气 |
| B | NH4Cl(aq)[Fe3+(aq)] | NaOH溶液 | 过滤 |
| C | Cl2(g)[HCl(g)] | 饱和食盐水、浓H2SO4 | 洗气 |
| D | Na2CO3(s)[NaHCO3(s)] | - | 加热 |
| A、A | B、B | C、C | D、D |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、浓硝酸存放在棕色细口瓶中 |
| B、氢氧化钠溶液盛装在用玻璃塞的试剂瓶中 |
| C、硫酸亚铁溶液存放在加有少量铁粉的试剂瓶中 |
| D、少量金属钠保存在煤油中 |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
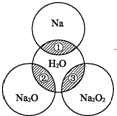 如图所示,两圆圈相交的阴影部分表示圆圈内的物质相互发生的反应.已知钠及其氧化物的物质的量均为0.1mol,水的质量为100g.下列说法正确的是( )
如图所示,两圆圈相交的阴影部分表示圆圈内的物质相互发生的反应.已知钠及其氧化物的物质的量均为0.1mol,水的质量为100g.下列说法正确的是( )| A、Na2O2晶体中阴阳离子数目之比为1:1 |
| B、反应③最多能产生0.05 mol O2 |
| C、反应①的离子方程式为Na+2H2O═Na++2OH-+H2↑ |
| D、①、②、③充分反应后所得溶液的质量分数从大到小的顺序为①>②>③ |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、NH4+、NO3-、Al3+、Cl- |
| B、Na+、SO32-、K+、Cl- |
| C、MnO4-、K+、SO42-、Na+ |
| D、K+、SO42-、HCO3-、Na+ |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、高温下,0.3 molFe与足量水蒸气反应,转移电子数目为0.8NA | ||||
| B、MnO2与浓盐酸共热,0.4 molHCl被氧化时,转移电子数目为0.4 NA | ||||
| C、5.6g铁片投入足量浓H2SO4中,转移电子数目为0.3 NA | ||||
D、5NH4NO3
|
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com