
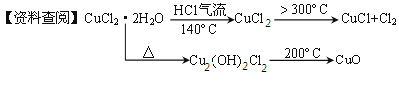
ЎҫМвДҝЎҝCuCl№г·әУҰУГУЪ»Ҝ№ӨәНУЎИҫөИРРТөЎЈДіСРҫҝРФС§П°РЎЧйДвИИ·ЦҪвCuCl2ЎӨ2H2OЦЖұёCuClЈ¬ІўҪшРРПа№ШМҪҫҝЎЈ
ЎҫКөСйМҪҫҝЎҝёГРЎЧйУГПВНјЛщКҫЧ°ЦГҪшРРКөСй(јРіЦТЗЖчВФ)ЎЈ

Зл»ШҙрПВБРОКМвЈә
(1)ТЗЖчXөДГыіЖКЗ__________ЎЈ
(2)КөСйІЩЧчөДПИәуЛіРтКЗўЩ Ўъ Ўъ Ўъ Ўъ ўЭЎЈ
ўЩјмІйЧ°ЦГөДЖшГЬРФәујУИлТ©Ж· ўЪПЁГрҫЖҫ«өЖЈ¬АдИҙ
ўЫФЪЎ°ЖшМеИлҝЪЎұҙҰНЁёЙФпHCl ўЬөгИјҫЖҫ«өЖЈ¬јУИИ
ўЭНЈЦ№НЁИлHClЈ¬И»әуНЁИлN2
(3)ФЪКөСй№эіМЦРЈ¬№ЫІмөҪBЦРОпЦКУЙ°ЧЙ«ұдОӘА¶Й«Ј¬CЦРКФЦҪөДСХЙ«ұд»ҜКЗ ЎЈ
(4)Ч°ЦГDЦР·ўЙъ·ҙУҰөДАлЧУ·ҪіМКҪКЗ ЎЈ
(5)·ҙУҰҪбКшәуЈ¬ИЎіцCuClІъЖ·ҪшРРКөСйЈ¬·ўПЦЖдЦРә¬УРЙЩБҝөДCuCl2»тCuOФУЦКЈ¬ёщҫЭЧКБПРЕПў·ЦОцЈә
ўЩИфФУЦККЗCuCl2Ј¬ФтІъЙъөДФӯТтКЗ ЎЈ
ўЪИфФУЦККЗCuOЈ¬ФтІъЙъөДФӯТтКЗ ЎЈ
(6)ИфТСЦӨКөФУЦКОӘCuOЈ¬ЗлРҙіцУЙCu2(OH)2Cl 2ЙъіЙCuOөД»ҜС§·ҪіМКҪ ЎЈ
Ўҫҙр°ёЎҝ
(1)ЗтРОёЙФп№ЬЈ»(2)ўЫЎъўЬЎъўЪЈ»(3)ПИұдәмәуНКЙ«Ј»
(4)Cl2+2OH-=Cl-+ClO-+2H2OЈ»H++OH-=H2OЈ»
(5)ўЩјУИИКұјдІ»Чг»тОВ¶ИЖ«өНЈ»ўЪHClЖшБчІ»ЧгЎЈ
(6)Cu2(OH)2Cl2![]() 2CuO+2HClЎьЈ»
2CuO+2HClЎьЈ»
ЎҫҪвОцЎҝ
КФМв·ЦОцЈә(1)УЙНјј°іЈјыөДТЗЖчҝЙЦӘЈ¬ТЗЖчXөДГыіЖОӘЗтРОёЙФп№ЬЈ¬№Кҙр°ёОӘЈәЗтРОёЙФп№ЬЈ»
(2)КөСйЦРУРЖшМеЙъіЙЈ¬ПИјмСйЧ°ЦГөДЖшГЬРФЈ¬ЗТИИ·ЦҪвCuCl22H2OЦЖұёCuClЈ¬·АЦ№CuClұ»Сх»ҜәНCu+Л®ҪвЛщТФұШРлТӘПИёПЧЯЧ°ЦГЦРөДСхЖшәНЛ®ХфЖшәуІЕјУИИЈ¬ЗТТӘФЪHClЖшБчЦРјУИИЦЖұёЈ¬·ҙУҰҪбКшәуПИПЁГрҫЖҫ«өЖЈ¬УҰёГТӘјМРшНЁИлөӘЖшЦұЦБЧ°ЦГАдЗРЈ¬ЛщТФІЩЧчЛіРтОӘЈәўЩ ЎъўЫЎъўЬЎъўЪЎъ ўЭЈ¬№Кҙр°ёОӘЈәўЫЎъўЬЎъўЪЈ»
(3)BЦРУР°ЧЙ«ұдОӘА¶Й«Ј¬ЛөГчУРЛ®ЙъіЙЈ¬ІъОпЦР»№УРCl2Ј¬ЛщТФCЦРКҜИпКФЦҪПИЦрҪҘұдОӘәмЙ«Ј¬әуНКЙ«Ј¬№Кҙр°ёОӘЈәКҜИпКФЦҪПИЦрҪҘұдОӘәмЙ«Ј¬әуНКЙ«Ј»
(4)DЦРКЗCl2әНNaOH·ҙУҰЙъіЙВИ»ҜДЖЎўҙОВИЛбДЖәНЛ®Ј¬әНВИ»ҜЗвУлЗвСх»ҜДЖөД·ҙУҰЈ¬·ҙУҰөДАлЧУ·ҪіМКҪОӘCl2+2OH-=Cl-+ClO-+H2OЈ»H++OH-=H2OЈ¬№Кҙр°ёОӘЈәCl2+2OH-=Cl-+ClO-+H2OЈ»H++OH-=H2OЈ»
(5)ўЩУЙ2CuCl2![]() 2CuCl+Cl2ЎьЈ¬ФУЦККЗCuCl2ЛөГчCuCl2Г»УР·ҙУҰНкИ«Ј¬·ЦҪвОВ¶ИІ»ёЯЈ¬№Кҙр°ёОӘЈәјУИИКұјдІ»Чг»тОВ¶ИЖ«өНЈ»ўЪФУЦККЗСх»ҜНӯЈ¬ЛөГчCuClұ»СхЖшСх»ҜІЕІъЙъБЛCuOЈ¬ЛөГчЧ°ЦГЦРУРСхЖшЈ¬ҝЙДЬКЗГ»УРФЪHClөД·ХО§ЦРјУИИ»тХЯОҙөИКФ№ЬАдИҙҫННЈЦ№НЁИлHClЖшМеЈ¬№Кҙр°ёОӘЈәНЁИлHClөДБҝІ»ЧгЎЈ
2CuCl+Cl2ЎьЈ¬ФУЦККЗCuCl2ЛөГчCuCl2Г»УР·ҙУҰНкИ«Ј¬·ЦҪвОВ¶ИІ»ёЯЈ¬№Кҙр°ёОӘЈәјУИИКұјдІ»Чг»тОВ¶ИЖ«өНЈ»ўЪФУЦККЗСх»ҜНӯЈ¬ЛөГчCuClұ»СхЖшСх»ҜІЕІъЙъБЛCuOЈ¬ЛөГчЧ°ЦГЦРУРСхЖшЈ¬ҝЙДЬКЗГ»УРФЪHClөД·ХО§ЦРјУИИ»тХЯОҙөИКФ№ЬАдИҙҫННЈЦ№НЁИлHClЖшМеЈ¬№Кҙр°ёОӘЈәНЁИлHClөДБҝІ»ЧгЎЈ
(6)ИфТСЦӨКөФУЦКОӘCuOЈ¬ФтУЙCu2(OH)2Cl 2ЙъіЙCuOөД»ҜС§·ҪіМКҪОӘCu2(OH)2Cl2![]() 2CuO+2HClЎьЈ¬№Кҙр°ёОӘЈәCu2(OH)2Cl2
2CuO+2HClЎьЈ¬№Кҙр°ёОӘЈәCu2(OH)2Cl2![]() 2CuO+2HClЎьЎЈ
2CuO+2HClЎьЎЈ



| Дкј¶ | ёЯЦРҝОіМ | Дкј¶ | іхЦРҝОіМ |
| ёЯТ» | ёЯТ»Гв·СҝОіМНЖјцЈЎ | іхТ» | іхТ»Гв·СҝОіМНЖјцЈЎ |
| ёЯ¶ю | ёЯ¶юГв·СҝОіМНЖјцЈЎ | іх¶ю | іх¶юГв·СҝОіМНЖјцЈЎ |
| ёЯИэ | ёЯИэГв·СҝОіМНЖјцЈЎ | іхИэ | іхИэГв·СҝОіМНЖјцЈЎ |
ҝЖДҝЈәёЯЦР»ҜС§ АҙФҙЈә МвРНЈә
ЎҫМвДҝЎҝҪьјёДкАҙЈ¬№ЪТФЎ°ВМЙ«ЎұөДРВёЕДоІ»¶ПІъЙъЈ¬ИзВМЙ«КіЖ·ЎўВМЙ«ІДБПЎўВМЙ«ДЬФҙЎўВМЙ«»ҜС§өИЈ¬ХвАпөДЎ°ВМЙ«ЎұКЗ¶ФИЛАаЙз»бҝЙіЦРш·ўХ№ХҪВФөДРОПуұнҙпЎЈЎ°ВМЙ«»ҜС§ЎұТӘЗуҙУҫӯјГЎў»·ұЈәНјјКхЙПЙијЖҝЙРРөД»ҜС§·ҙУҰЎЈҫЭҙЛЈ¬УЙөҘЦКГҫЦЖПхЛбГҫөДПВБРЛДёц·Ҫ°ёЦРЈ¬ДгИПОӘҝЙРР¶шЗТ·ыәПЎ°ВМЙ«»ҜС§ЎұТӘЗуөД·Ҫ°ёКЗ( )
A.Mg![]() Mg(NO3)2
Mg(NO3)2
B.Mg![]() MgCl2
MgCl2![]() Mg(OH)2
Mg(OH)2![]() Mg(NO3)2
Mg(NO3)2
C.Mg![]() MgO
MgO![]() Mg(NO3)2
Mg(NO3)2
D.Mg![]() MgSO4
MgSO4![]() Mg(NO3)2
Mg(NO3)2
Ійҝҙҙр°ёәНҪвОц>>
ҝЖДҝЈәёЯЦР»ҜС§ АҙФҙЈә МвРНЈә
ЎҫМвДҝЎҝПВБР·ҙУҰКфУЪОьИИ·ҙУҰөДКЗЈЁ Ј©
A.ДҫМҝөДИјЙХ
B.ЗвСх»Ҝұөҫ§МеУлВИ»Ҝп§ҫ§Ме»мәП
C.ГҫМхУлПЎБтЛбөД·ҙУҰ
D.ЙъКҜ»ТИЬУЪЛ®
Ійҝҙҙр°ёәНҪвОц>>
ҝЖДҝЈәёЯЦР»ҜС§ АҙФҙЈә МвРНЈә
ЎҫМвДҝЎҝҫц¶ЁЖшМеМе»эҙуРЎөДЦчТӘТтЛШКЗЈЁ Ј©
ўЩЖшМе·ЦЧУөДКэДҝ ўЪЖшМе·ЦЧУөДЦұҫ¶ ўЫЖшМе·ЦЧУјдөДҫаАл ўЬЖшМе·ЦЧУөДЦКБҝ
AЈ®ўЩўЪ BЈ®ўЪўЫ CЈ®ўЩўЫ DЈ®ўЫўЬ
Ійҝҙҙр°ёәНҪвОц>>
ҝЖДҝЈәёЯЦР»ҜС§ АҙФҙЈә МвРНЈә
ЎҫМвДҝЎҝПЦУРH2ЎўCO(Ме»эұИОӘ3ЎГ2)өД»мәПЖшМеa LЈ¬ФЪПаН¬МхјюПВЈ¬өұЖдНкИ«ИјЙХКұЛщРиO2Ме»эОӘ( )
AЈ®0.5 a L BЈ®a L CЈ® 2 a L DЈ®3 a L
Ійҝҙҙр°ёәНҪвОц>>
ҝЖДҝЈәёЯЦР»ҜС§ АҙФҙЈә МвРНЈә
ЎҫМвДҝЎҝЖҜ°Ч·ЫөДЦчТӘіЙ·ЦКЗЈЁ Ј©
AЈ®NaClO BЈ®CaCl2әН Ca(ClO)2 CЈ®NaClәНNaClO DЈ®Ca(ClO)2
Ійҝҙҙр°ёәНҪвОц>>
ҝЖДҝЈәёЯЦР»ҜС§ АҙФҙЈә МвРНЈә
ЎҫМвДҝЎҝПтГЬұХИЭЖчЦРідИлОпЦКAәНBЈ¬·ўЙъ·ҙУҰaAЈЁgЈ©+bBЈЁgЈ©![]() cCЈЁgЈ©ЎЈ·ҙУҰ№эіМЦРЈ¬ОпЦКAөДә¬БҝЈЁAЈҘЈ©әНCөДә¬БҝЈЁCЈҘЈ©ЛжОВ¶ИЈЁTЈ©өДұд»ҜЗъПЯИзНјЛщКҫЈ¬ПВБРЛө·ЁХэИ·өДКЗ
cCЈЁgЈ©ЎЈ·ҙУҰ№эіМЦРЈ¬ОпЦКAөДә¬БҝЈЁAЈҘЈ©әНCөДә¬БҝЈЁCЈҘЈ©ЛжОВ¶ИЈЁTЈ©өДұд»ҜЗъПЯИзНјЛщКҫЈ¬ПВБРЛө·ЁХэИ·өДКЗ

A. ёГ·ҙУҰФЪT1ЎўT3ОВ¶ИКұҙпөҪ№э»ҜС§ЖҪәв B. ёГ·ҙУҰФЪT2ОВ¶ИКұҙпөҪ№э»ҜС§ЖҪәв
C. ёГ·ҙУҰөДДж·ҙУҰКЗ·ЕИИ·ҙУҰ D. ЙэёЯОВ¶ИЈ¬ЖҪәв»бПтХэ·ҙУҰ·ҪПтТЖ¶Ҝ
Ійҝҙҙр°ёәНҪвОц>>
ҝЖДҝЈәёЯЦР»ҜС§ АҙФҙЈә МвРНЈә
ЎҫМвДҝЎҝЧцКөСйКұІ»РЎРДК№ЖӨ·фЙПХіБЛТ»Р©ёЯГМЛбјШЈ¬РОіЙөДәЪ°ЯәЬҫГІЕДЬПыіэЈ¬Из№ыУГІЭЛбЈЁТТ¶юЛбЈ©өДПЎИЬТәПҙөУЈ¬әЪ°ЯҝЙТФСёЛЩНЛИҘЈ¬ЖдАлЧУ·ҪіМКҪОӘ(ОҙЕдЖҪ)Јә
MnO4-+H2C2O4+H+ЎъCO2+Mn2++![]() Ј¬ПВБРУР№ШРрКцХэИ·өДКЗ
Ј¬ПВБРУР№ШРрКцХэИ·өДКЗ
AЈ®ёГ·ҙУҰөДСх»ҜјБОӘH2C2O4
BЈ®ёГАлЧУ·ҪіМКҪУТІа·ҪҝтДЪөДІъОпКЗOH-
CЈ®6mol H+ІОјУ·ҙУҰКұЈ¬өзЧУЧӘТЖ10mol
DЈ®ГҝЙъіЙ1mol CO2Ј¬өзЧУЧӘТЖөДКэДҝОӘ1mol
Ійҝҙҙр°ёәНҪвОц>>
ҝЖДҝЈәёЯЦР»ҜС§ АҙФҙЈә МвРНЈә
ЎҫМвДҝЎҝ 13C©ҒNMRЈЁәЛҙЕ№ІХсЈ©Ўў15N©ҒNMRҝЙУГУЪІв¶Ёө°°ЧЦКЎўәЛЛбөИЙъОпҙу·ЦЧУөДҝХјдҪб№№Ј¬ХвПоСРҫҝФш»с2002ДкЕөұҙ¶ы»ҜС§ҪұЈ®ПВГжУР№ШРрКцХэИ·өДКЗЈЁ Ј©
A.13CУл15NУРПаН¬өДЦРЧУКэ
B.13CУлC60»ҘОӘН¬ЛШТмРОМе
C.15N Ул14N »ҘОӘН¬О»ЛШ
D.232ThЧӘ»ҜіЙ233UКЗ»ҜС§ұд»Ҝ
Ійҝҙҙр°ёәНҪвОц>>
°Щ¶ИЦВРЕ - Б·П°ІбБРұн - КФМвБРұн
әюұұКЎ»ҘБӘНшОҘ·ЁәНІ»БјРЕПўҫЩұЁЖҪМЁ | НшЙПУРәҰРЕПўҫЩұЁЧЁЗш | өзРЕХ©ЖӯҫЩұЁЧЁЗш | ЙжАъК·РйОЮЦчТеУРәҰРЕПўҫЩұЁЧЁЗш | ЙжЖуЗЦИЁҫЩұЁЧЁЗш
ОҘ·ЁәНІ»БјРЕПўҫЩұЁөз»°Јә027-86699610 ҫЩұЁУКПдЈә58377363@163.com