
【题目】在两个密闭容器中,分别充有质量相同的甲、乙两种气体,若它们的温度和密度均相同,试根据甲、乙的摩尔质量![]() 关系,判断下列说法正确的是( )
关系,判断下列说法正确的是( )
A.若![]() ,则气体的压强:甲
,则气体的压强:甲![]() 乙
乙
B.若![]() ,则气体的摩尔体积:甲
,则气体的摩尔体积:甲![]() 乙
乙
C.若![]() ,则气体体积:甲
,则气体体积:甲![]() 乙
乙
D.若![]() ,则分子数:甲
,则分子数:甲![]() 乙
乙
科目:高中化学 来源: 题型:
【题目】从海水中可提取多种化工原料,下图是工业上对海水资源进行综合利用的流程图。试回答下列问题:

(1)若粗盐中含有杂质离子Ca2+、Mg2+、SO42-,精制时所用试剂为A.盐酸、B.BaCl2溶液、C.NaOH溶液、D.Na2CO3溶液。则加入试剂的顺序是________(填序号)。
(2)写出用海滩上的贝壳制Ca(OH)2的化学方程式:________________。
(3)电解熔融MgCl2可制取镁和Cl2,其中Cl2和Ca(OH)2反应可制得漂白粉。制漂白粉的化学方程式为________________。
(4)从经济效益角度考虑,该化工厂厂址应选在________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】将一包由Cu、![]() 和CuO组成的混合物均分成两份:一份混合物在加热条件下与
和CuO组成的混合物均分成两份:一份混合物在加热条件下与![]() 充分反应,将固体全部转化成铜粉时固体质量减少了
充分反应,将固体全部转化成铜粉时固体质量减少了![]() ;向另一份混合物中加入
;向另一份混合物中加入![]() 溶液恰好完全反应生成
溶液恰好完全反应生成![]() 和
和![]() 假设不产生其他还原产物
假设不产生其他还原产物![]() ,这些NO和
,这些NO和![]() 标准状况
标准状况![]() 混合并通入足量水中,气体全部被吸收生成
混合并通入足量水中,气体全部被吸收生成![]() 。则该硝酸的物质的量浓度为
。则该硝酸的物质的量浓度为![]()
![]()
A.![]() B.
B.![]() C.
C.![]() D.
D.![]()
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图所示,①和②为两个体积相同的固定容器,图中“![]() ”和“
”和“![]() ”分别表示氢原子和氧原子,则下列说法正确的是( )
”分别表示氢原子和氧原子,则下列说法正确的是( )
①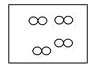 ②
②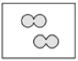
A.若①中的![]() 为4mol,则②中所含原子总数为
为4mol,则②中所含原子总数为![]() 个
个
B.①和②中气体的质量之比为1:8
C.![]() 、
、![]() 均能发生化合反应,但均不能发生置换反应
均能发生化合反应,但均不能发生置换反应
D.两容器的温度和压强均相同
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在浓CaCl2溶液中通入NH3和CO2,可以制得纳米级碳酸钙(粒子直径在1~10 nm之间)。下图所示A~E为实验室常见的仪器装置(部分固定夹持装置略去),请根据要求回答问题。

(1)实验室选用上图所示装置制取、收集干燥的NH3,接口的连接顺序是:a接_____(填小写字母代号,下同),_____接___,_____接h。
(2)向浓CaCl2溶液中通入NH3和CO2气体制纳米级碳酸钙时,应先通入的气体是____,试写出制纳米级碳酸钙的离子方程式:_____。
(3)在浓CaCl2溶液和NH3用量正确的情况下,CO2不足或过量都会导致纳米级碳酸钙产量下降,若CO2过量,溶液中大量存在的离子有(不考虑弱电解质的电离和盐类水解产生的少量离子):____。
(4)取反应后去除CaCO3的溶液分别做以下实验,下列实验判断合理的是_____(填字母代号)。
A.滴加少量Na2CO3溶液,若有沉淀生成,说明CO2一定不足
B.滴加少量盐酸,若有气泡产生,说明CO2一定过量
C.测量溶液pH,若pH小于7,说明CO2一定过量
D.滴加少量BaCl2溶液,若无沉淀生成,说明CO2一定没有过量
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】部分中学化学常见元素原子结构及性质如下表所示
元素 | 结构及性质 |
A | 元素A在第三周期中简单离子半径最小 |
B | B原子最外层电子数是内层电子数的0.6 |
C | 使用最广泛的金属元素C能形成两种氯化物,其相对分子质量之差为35.5 |
D | 元素D与B同主族,且大多数情况下D不显正化合价 |
E | 元素E在周期表中位于ⅠA族,有人认为将其排在ⅦA族也有一定道理 |
F | 元素F与B同周期,其最高价氧化物的水化物与A或B的最高价氧化物的水化物均能反应 |
(1)元素C在周期表中的位置是____元素;元素E形成的一种简单离子能支持“将元素E排在ⅦA族”这一观点,该离子的结构示意图为___。
(2)元素E与D可以按原子个数比2∶1、1∶1形成两种化合物X、Y,区别X、Y这两种物质的实验方法为 __。E与B形成的一种化合物Z与X、Y中的一种电子总数相同且能发生化学反应,写出该反应的化学方程式:___(用相应化学式表示)。
(3)请画出化合物F2B2的电子式:_____,该化合物中含有的化学键类型是___。
(4)元素A与元素F相比,金属性较强的是_________ (用元素符号表示),下列表述正确且能证明这一事实的是___(填字母代号)。
a.对应单质与酸反应时,每个A原子比每个F原子失电子多
b.对应单质与同浓度盐酸反应时,F比A剧烈得多
c.A的氧化物熔点比F的氧化物熔点高
d.F可将A从其盐溶液中置换出来
e.最高价氧化物对应的水化物的碱性F比A的强
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】回答下面问题:
(1)在①KNO3 ②K2CO3 ③(NH4)2SO4 三种盐溶液中,常温下呈酸性的是_____(填序号),显酸性的原因是_____(用化学用语表示)。
(2)将三氯化锑(SbCl3)固体溶于水,生成白色沉淀,且溶液 pH<7,则配制 SbCl3 溶液的正确方法是_____
(3)某温度下,向含有 AgCl 固体的 AgCl 饱和溶液中加入少量稀盐酸,则 c(Ag+)_____(填“增大”“减小”或“不变”,下同),Ksp_____。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】丰富多彩的生活材料:
(1)青奥会将于2014年8月在南京举行。青奥会建筑设施使用了大量节能材料,体现了“绿色青奥”的理念。
①用于青奥村工程的隔热保温材料聚氨酯属于___(填字母)。
a.有机高分子材料 b.无机非金属材料 c.金属材料
②青奥中心外墙的复合保温材料采用铝合金锁边。有关铝合金的性质正确的是___(填字母)。
a.强度小 b.耐腐蚀 c.密度大
③青奥会议中心双塔采用了玻璃幕墙设计。制造玻璃的主要原料为纯碱、石灰石和___(填字母)。
a.金刚砂 b.石英 c.水玻璃
(2)生活中处处有化学,化学己渗透到我们的“衣、食、住、行”之中。
①铝合金是生活中常见的材料,具有密度小、强度高的优良性能。其在空气中不易生锈的原因是___。
②玻璃和钢铁是常用的建筑材料。普通玻璃是由Na2SiO3、CaSiO3、___等物质组成的;钢铁制品不仅可发生化学腐蚀,在潮湿的空气中还能发生___腐蚀,生成的铁锈的主要成分是___(填化学式)。
(3)氮化硅是一种新型高温材料,可用于制造汽车发动机。请写出高纯硅和氮气在1300℃反应制备氮化硅的化学方程式:___。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】常温下,量取pH=2的两种二元酸H2A与H2B各1ml,分别加水稀释,测得pH与加水稀释倍数有如图所示关系,则下列有关叙述不正确的是

A. H2B为弱酸
B. NaHA水溶液中:c(Na+)+c(H+)=2c(A2-)+c(OH-)
C. 含等物质的量的NaHA、NaHB的混合溶液中:c(Na+)=c(A2-)+c(HB-)+c(B2-)+c(H2B)
D. pH=10的NaHB溶液中:c(Na+)>c(HB-)>c(B2-)>c(OH-)>c(H2B)
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com