
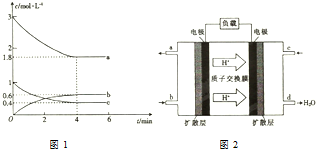
 甲醇是一种低碳能源,在全球能源危机和环境污染的背景下具有良好的发展前景,在催化剂作用下可用H2(g)+CO(g)$\stackrel{催化剂}{?}$CH3OH(g),三种物质的物质的量浓度随时间变化的关系如图1所示.
甲醇是一种低碳能源,在全球能源危机和环境污染的背景下具有良好的发展前景,在催化剂作用下可用H2(g)+CO(g)$\stackrel{催化剂}{?}$CH3OH(g),三种物质的物质的量浓度随时间变化的关系如图1所示.分析 (1)根据2H2(g)+CO(g)$\stackrel{催化剂}{?}$CH3OH反应,H2浓度变化在减小并且是CO的2倍判断;
(2)可以加快反应速率的措施为加压或者升温等;
(3)根据CH3OH的平均反应速率=$\frac{△c}{△t}$计算;
(4)在甲醇燃料电池中,燃料甲醇作负极,发生失电子的氧化反应,氧气作正极,发生得电子的还原反应,根据电极反应以及电子守恒来计算消耗的氧气的体积.
解答 解:(1)由2H2(g)+CO(g)$\stackrel{催化剂}{?}$CH3OH反应,H2浓度变化在减小并且是CO的2倍,所以代表H2浓度变化的曲线为a,故答案为:a;
(2)可以加快反应速率的措施为加压或者升温,故答案为:加压或者升温;
(3)根据图象CH3OH为生成物,即代表CH3OH浓度变化的曲线为b,则0-4 min内,CH3OH的平均反应速率=$\frac{△c}{△t}$=$\frac{0.6mol/L}{4min}$=0.15mol/(L•min),故答案为:0.15mol/(L•min);
(4)①在甲醇燃料电池中,燃料甲醇作负极,氧气作正极,电解质中的阳离子移向正极,所以c口通入的物质为氧气,该电极为正极,故答案为:O2;正极;
②当6.4g即0.2mol甲醇完全反应生成CO2时,根据总反应:2CH3OH+3O2=2CO2+4H2O,消耗氧气0.3mol,即标准状况下体积为0.3×22.4=6.72L,故答案为:6.72.
点评 本题是一道关于化学平衡图象的分析与反应速率的计算以及燃料电池的工作原理知识的考题,要求学生具有分析和解决问题的能力,难度不大.


 口算能手系列答案
口算能手系列答案科目:高中化学 来源: 题型:选择题
| A. | 使甲基橙变红色的溶液:Mg2+、K+、SO42-、NO3- | |
| B. | 常温下,c(H+)/c(OH-)=1010的溶液中:Na+、NH4+、ClO-、I- | |
| C. | 水电离出的c(H+)=10-12mol•L-1的溶液:K+、Na+、CO32-、Br- | |
| D. | 含有0.1mol•LHCO3-的溶液:Na+、Fe3+、NO3-、SCN- |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
 .
.
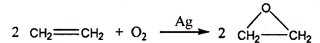

查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | ①②③⑤ | B. | ①③④ | C. | ①③⑤ | D. | ①②③④⑤ |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
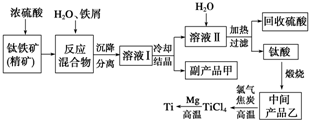 金属钛(Ti)因其硬度大、熔点高、常温时耐酸碱腐蚀等性质被广泛用在高新科技材料和航天领域中.
金属钛(Ti)因其硬度大、熔点高、常温时耐酸碱腐蚀等性质被广泛用在高新科技材料和航天领域中.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| ① | ② | ③ |
| 将铁钉放入硫酸铜溶液中 | 向硫酸亚铁溶液中滴入几滴浓硝酸 | 将铁钉放入氯化铁溶液中 |
| A. | 实验①和③中的铁钉只作还原剂 | |
| B. | 实验③中反应的离子方程式为Fe+Fe3+═2Fe2+ | |
| C. | 实验②中Fe2+既显氧化性又显还原性 | |
| D. | 上述实验证明氧化性:Fe3+>Fe2+>Cu2+ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | ①③②⑤ | B. | ①④②⑤ | C. | ①③②⑥ | D. | ①⑥⑤ |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com