
【题目】在国庆70周年庆典上,空中飞过的歼击机编队让我们热血沸腾,其中有中国自主研制的最先进的歼20隐形超音速飞机。当超音速飞机在平流层飞行时,尾气中的NO会破坏臭氧层,,或许通过测定局部的臭氧浓度变化可使飞机不再“隐形”。因此科学家正在研究利用催化技术将尾气中的NO和CO转变成CO2和N2,化学方程式如下:2NO(g)+2CO(g) ![]() 2CO2(g)+N2(g) △H<0。请回答下列问题:
2CO2(g)+N2(g) △H<0。请回答下列问题:
(1)该反应的平衡常数表达式为___________________________。
(2)假设在闭容器发生上述反应,达到平衡后采取下列选项的措施既能加快反应速率又能提高NO转化率的是_____________。
A.选用更有效的催化剂同时增加CO的量 B.升高反应体系的温度
C.及时加入碱石灰 D.缩小容器的体积
(3)研究表明:在使用等质量催化剂时,增大催化剂比表面积可提高化学反应速率。为了分别验证温度、催化剂比表面积对化学反应速率的影响规律,某同学将等物质的量的NO和CO充入容积为2L的恒容密闭容器中,设计了三组实验,部分实验数据已经填在下面实验设计表中。
实验编号 | T/℃ | NO初始浓度/mol·L-1 | NO平衡浓度/mol·L-1 | 催化剂的比表面积/m2·g-1 |
Ⅰ | 280 | 0.3 | 0.1 | 82 |
Ⅱ | T1 | c1 | c2 | 124 |
Ⅲ | 350 | c3 | c4 | 124 |
①在上述表格的实验条件数据中,T1=____________,c3=_____________。
②平衡时若保持温度T1℃不变,再向容器中充入CO和CO2各0.2mol,则平衡将_________移动(填“向左”“向右”或“不”)

③在给出的坐标图中,画出了上表中的I、Ⅱ、Ⅲ实验条件下建立平衡过程中,混合气体里NO浓度随时间变化的趋势曲线图,请说出B曲线对应的实验编号__________(填Ⅱ、Ⅲ)。

(4)在恒温恒容的密闭容器中通入n(NO):n(CO)=1:3的混合气体,发生上述反应,下列图像正确且能说明反应在进行到t1时刻一定达到平衡状态的是__________(选填字母)。
【答案】K=![]() A、D 280 0.3 向右 Ⅲ c、d
A、D 280 0.3 向右 Ⅲ c、d
【解析】
(1)根据平衡常数的公式结合题给的反应写出平衡常数表达式;
(2)措能加快反应速率的外界条件:增大浓度、升高温度、增大气体的压强、使用催化剂等;提高NO转化率的方法:增大压强,降低温度、增大一氧化碳浓度等;据以上分析解答。
(3)①根据控制变量法,在进行比较时,其他量不变,让一个量发生变化进行分析;
②由三段式计算出平衡常数K;根据浓度商与K的关系确定反应进行的方向。
③催化剂不影响平衡的移动,改变反应的速率;
(4)根据反应达到平衡状态时,正逆反应速率相等,各组分的浓度保持不变及由此衍生出的其它物理量进行分析。
(1)该反应的平衡常数表达式为K=![]() 。
。
(2)A.选用更有效的催化剂能加快反应速率,增大反应物的浓度,平衡正向移动,另一反应物的转化率提高,A项正确;
B.反应是个放热反应,升高体系的温度,平衡逆向移动,NO的转化率降低,B项错误;
C.碱石灰吸收二氧化碳,使产物二氧化碳浓度减小,并不能加快反应速率,C项错误;
D.缩小容器的体积,增大了压强,使反应速率加快,由于该反应正向是一个气体分子总数减小的反应,加压平衡正向移动,使一氧化NO转化率提高,D项正确;
答案选AD。
(3)①根据控制变量法,第Ⅰ组和第Ⅱ组比表面积不同,那温度就是相同的,所以T1是280℃,各组投放物料是一样的,故c3仍是0.3 mol·L-1。
②由三段式计算出平衡常数k:
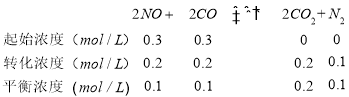
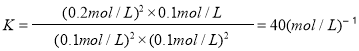 ,再向容器中充入CO和CO2各0.2mol,瞬间各物质的浓度:c(NO)=0.1 mol·L-1、C(CO)=0.2 mol·L-1、c(CO2)=0.3 mol·L-1、c(N2) =0.1mol·L-1。浓度商
,再向容器中充入CO和CO2各0.2mol,瞬间各物质的浓度:c(NO)=0.1 mol·L-1、C(CO)=0.2 mol·L-1、c(CO2)=0.3 mol·L-1、c(N2) =0.1mol·L-1。浓度商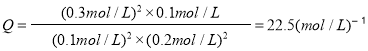
Q<K,故平衡正向移动。
③催化剂表面积的改变并不能影响到达平衡时平衡浓度,能够影响平衡移动的,在该题中是温度,B曲线到达平衡时的浓度和另外两条不一样,所以B曲线对应的是350℃即Ⅲ组的实验。
(4)a.平衡常数只受温度影响而改变,只要温度没变,无论是否达到平衡,平衡常数都不会改变,故t1时刻不能判断是否达平衡,a项错误;
b.t1时刻CO2和NO物质的量相等,但t1时刻之后CO2、NO物质的量还在改变,故t1时刻没有达到平衡状态,b项错误;
c.起始通入n(NO):n(CO)=1:3,二者反应按1:1进行转化,随反应进行比例关系发生变化,t1时刻起n(NO):n(CO)不变了,则说明已达平衡,故c项正确;
d.转化率不变了,说明已达到平衡,d项正确;
答案选c、d。


 新思维假期作业暑假吉林大学出版社系列答案
新思维假期作业暑假吉林大学出版社系列答案科目:高中化学 来源: 题型:
【题目】从工业废钒中回收金属钒既避免污染环境又有利于资源综合利用。某工业废钒的主要成分为V2O5、VOSO4和SiO2等,下图是从废钒中回收钒的一种工艺流程:

(1)为了提高“酸浸”效率,可以采取的措施有________(填两种).
(2)“还原”工序中反应的离子方程式为________.
(3)“沉钒”得到NH4VO3沉淀,需对沉淀进行洗涤,检验沉淀完全洗净的方法是________.
(4)写出流程中铝热反应的化学方程式________.
(5)电解精炼时,以熔融NaCl、CaCl2和VCl2为电解液(其中VCl2以分子形式存在).粗钒应与电源的________极(填“正”或“负”)相连,阴极的电极反应式为________.
(6)为预估“还原”工序加入H2C2O4的量,需测定“酸浸”液中VO2+的浓度.每次取25.00mL“酸浸”液于锥形瓶用a mol/L(NH4)2Fe(SO4)2标准溶液和苯代邻氨基苯甲酸为指示剂进行滴定(其中VO2+ VO2+),若三次滴定消耗标准液的体积平均为bmL,则VO2+的浓度为________g/L(用含a、b的代数式表示)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】
铜矿( CuFeS2)是炼铜的最主要矿物。火法冶炼黄钢矿的过程中,其中一步反应是:2Cu2O+Cu2S![]() 6Cu+SO2。回答下列问题。
6Cu+SO2。回答下列问题。
(1)Cu+价电子的电子排布图为___________,Cu2O与Cu2S比较,熔点较高的是___________,原因为______________________。
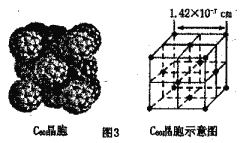
(2)SO2与SO3的键角相比,键角更小的是___________。某种硫的氧化物冷却到289.8K时凝固得到一种螺旋状单链结构的固体,其结构片段如图1所示。此固态物质中S原子的杂化轨道类型是___________;该物质的化学式为___________。
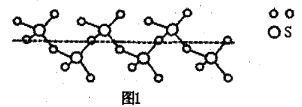
(3)离子化合物CaC2的晶体结构如图2所示。写出该物质的电子式___________。从钙离子看该晶体属于___________堆积,一个晶胞含有的π键平均有___________个。

(4)根据图3可知,与每个C60分子距离最近且相等的C60分子有___________个,其距离为___________cm(列出计算式即可)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】K2Cr2O7溶液中存在平衡:Cr2O72-(橙色)+H2O![]() 2CrO42-(黄色)+2H+,用K2Cr2O7溶液进行下列实验:
2CrO42-(黄色)+2H+,用K2Cr2O7溶液进行下列实验:
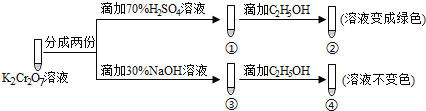
结合实验,下列说法错误的是( )
A.①中溶液橙色加深,③中溶液变黄B.对比②和④可知K2Cr2O7酸性溶液氧化性强
C.②中C2H5OH使Cr2O72-被氧化D.若向④中加入70%H2SO4溶液至过量,溶液可变为绿色
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列判断正确的是
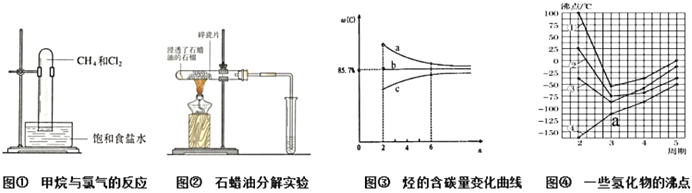
A. 图①:当CH4与Cl2体积比为1:2,维持足够长反应时间,CH4可全部变成CCl4
B. 图②:碎瓷片的作用与蒸馏实验中的碎瓷片作用不同
C. 图③:烷烃、烯烃、炔烃的单一物质及同类混合物含碳量随C原子数的变化曲线分别为a、b、c
D. 图④:点a代表的物质是PH3
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】有机物W用作调香剂、高分子材料合成的中间体等,制备W的一种合成路线如下。

请回答下列问题:
(1)F的化学名称是________,⑤的反应类型是________。
(2)E中含有的官能团是________(写名称),D聚合生成高分子化合物的结构简式为________。
(3)将反应③得到的产物与O2在催化剂、加热的条件下反应可得D,写出反应④的化学方程式________。
(4)④、⑤两步能否颠倒?________(填“能”或“否”)理由是________。
(5)与A具有含有相同官能团的芳香化合物的同分异构体还有________种(不含立体异构),其中核磁共振氢谱为六组峰,且峰面积之比为1:1:2:2:2:2的结构简式为________。
(6)参照有机物W的上述合成路线,以M和CH3Cl为原料制备F的合成路线(无机试剂任选)________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】相同温度下,容积均恒为2L的甲、乙、丙3个密闭容器中发生反应:
2SO2(g)+O2(g)![]() 2SO3(g) △H=-197kJ·mol-l。实验测得起始、平衡时的有关数据如下表:
2SO3(g) △H=-197kJ·mol-l。实验测得起始、平衡时的有关数据如下表:
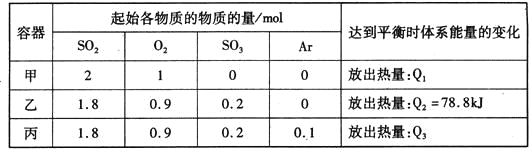
下列叙述正确的是
A. Q1>Q3>Q2=78.8kJ
B. 三个容器中反应的平衡常数均为K=2
C. 甲中反应达到平衡时,若升高温度,则SO2的转化率将大于50%
D. 若乙容器中的反应经tmin达到平衡,则0~tmin内,v(O2)=![]() mol/(L·min)
mol/(L·min)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】二氧化硫是硫的重要化合物,在生产、生活中有广泛应用,是大气主要污染物之一,具有一定的还原性,探究SO2气体还原Fe3+、I2,可以使用的药品和装置如图所示:
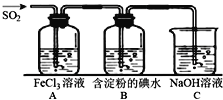
(1)写出由铜和浓硫酸制取SO2的化学方程式_____________________。
(2)装置A中的现象是__________。若要从A中的FeCl3溶液中提取晶体,必须进行的实验操作步骤:蒸发、冷却结晶、过滤、自然干燥,在过滤操作中有用到的玻璃仪器有_______(填编号)。
A酒精灯 B烧瓶 C漏斗 D烧杯 E玻璃棒 F坩埚
(3)根据以上现象,该小组同学认为SO2与FeCl3发生氧化还原反应。
①写出SO2与FeCl3溶液反应的离子方程式___________________;
②请设计实验方案检验有Fe2+生成__________________________;
(4)B中蓝色溶液褪色,表明I-的还原性比SO2__________(填“强”或“弱”)。
(5)若C中所得溶液只有一种溶质且pH>7,则溶液中各离子浓度大小顺序为_________。
(6)工业上通过煅烧黄铁矿产生SO2来进一步得到硫酸,已知煅烧1g FeS2产生7.1kJ热量,写出煅烧FeS2的热化学反应方程式____________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】“人文奥运”的一个重要体现是:坚决反对运动员服用兴奋剂。某种兴奋剂的结构简式如图所示,有关该物质的说法正确的是( )

A.滴入KMnO4(H+)溶液,观察紫色褪去,能证明结构中存在碳碳双键
B.该分子中的所有碳原子可能共平面
C.遇FeCl3溶液显紫色,因为该物质与苯酚属于同系物
D.1 mol该物质与浓溴水和H2反应最多消耗Br2和H2分别为3mol、7 mol
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com