
| A、离子积是1×10-15 |
| B、以液氨为溶剂的溶液中C(NH4+)一定等于 C(NH2-) |
| C、若液氨中放人NaNH2,其离于积不变 |
| D、此液氨中放人NH4C1,其离子积数值增加 |


 中考利剑中考试卷汇编系列答案
中考利剑中考试卷汇编系列答案 教育世家状元卷系列答案
教育世家状元卷系列答案 黄冈课堂作业本系列答案
黄冈课堂作业本系列答案科目:高中化学 来源: 题型:
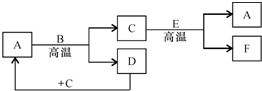 如图所示:已知A和E为金属单质,B是化合物且常温下为液态,F为两性化合物.
如图所示:已知A和E为金属单质,B是化合物且常温下为液态,F为两性化合物.查看答案和解析>>
科目:高中化学 来源: 题型:
| A、阴极产物是氢气 |
| B、阳极产物是氧气 |
| C、阴极产物是铝和氧气 |
| D、阳极产物只有氯气 |
查看答案和解析>>
科目:高中化学 来源: 题型:
 将锌片和铜片用导线相连后一同插入稀硫酸中,导线上便有电流通过.
将锌片和铜片用导线相连后一同插入稀硫酸中,导线上便有电流通过.查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、反应后溶液中不存在任何沉淀,所以反应前后Cu2+的浓度不变 |
| B、沉淀溶解后,生成深蓝色溶液是由于存在配合离子[Cu(NH3)4]2+ |
| C、向反应后的溶液中加入乙醇,将析出深蓝色的晶体CuSO4?5H2O |
| D、在[Cu(NH3)4]2+离子中,既存在离子键,又存在共价键 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| 1 |
| 2 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com