
短周期主族元素X、Y、Z、W的原子序数依次增大,元素X的原子半径最小,Y元素和X元素在一定条件下能形成YX,Z和W的原子序数相差8,W原子的电子总数是其电子层数的5倍。下列叙述正确的是( )
A.Y可用于制造高性能可充电电池
B.WX3的沸点高于ZX3
C.Z的最高价含氧酸的酸性强于W的最高价含氧酸的酸性
D.原子半径的大小顺序:rW>rZ>rY>rX
AC
【解析】短周期主族元素X、Y、Z、W的原子序数依次增大.Z和W的原子序数相差8,Z不可能是H元素,故Z、W处于同主族,Z处于第二周期、W处于第三周期,W原子的电子总数是其电子层数的5倍,故核外电子总数为15,W为磷元素,则Z为氮元素;元素X的原子半径最小,X只能处于第一周期,故X为氢元素;Y原子序数小于氮元素,Y元素和氢元素在一定条件下能形成YX,故Y表现+1价,H表现-1价,故Y为Li元素,A.金属Li可用于制造高性能可充电电池,A正确;B.NH3分子之间存在氢键,沸点:NH3>PH3,B错误;C.非金属性N>P,酸性:HNO3>H3PO4,C正确;D.Li原子半径最大、H原子半径最小,N、P同主族,半径P>N,原子半径Li>P>N>H,即rY>rW>rZ>rX,D错误;
考点:原子结构与元素周期率的关系


科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
| X | A | ||
| Y | C | B |
| A、原子半径由小到大的顺序为:A<B<C<Y |
| B、A、B的氢化物的沸点由低到高的顺序为:HA<HB |
| C、X、Y最高价氧化物对应的水化物的酸性由弱到强的顺序为:H2YO3<H2XO3 |
| D、B、C简单离子的还原性由弱到强的顺序为:B-<C 2- |
查看答案和解析>>
科目:高中化学 来源: 题型:
| Y | W | |
| X | Z |
| A、原子半径最大的是X |
| B、电负性最大的是W |
| C、Y、Z原子序数差为8 |
| D、氢化物最稳定的是Z |
查看答案和解析>>
科目:高中化学 来源: 题型:
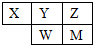 短周期主族元素X、Y、Z、W、M在元素周期表中的位置如图,W最高价氧化物对应的水化物为强酸,下列说法正确的是( )
短周期主族元素X、Y、Z、W、M在元素周期表中的位置如图,W最高价氧化物对应的水化物为强酸,下列说法正确的是( )| A、原子半径:Y<Z<M | B、M最高价氧化物对应的水化物一定是强酸 | C、Z与M对应的氢化物的沸点:M>Z | D、一定条件下,M、Y对应的单质都能与W的氢化物发生置换反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com