
| A. | 凡是放热反应都是自发的,吸热反应都是非自发的 | |
| B. | 化学反应的方向与反应的熵变无关 | |
| C. | 室温下,CaCO3(s)=CaO(s)+CO2(g)不能自发进行,说明该反应△H<0 | |
| D. | 同一物质:固体→液体→气体的变化是焓增和熵增的过程 |
分析 A、放热反应有利于反应的自发进行;
B、熵增加的反应有利于反应的自发进行;
C、根据反应可知△S>0,室温下不能自发进行,说明该反应的△H>0;
D、同一物质:固体→液体→气体的变化时吸收能量焓增和混乱程度变大熵增的过程.
解答 解:A、放热反应有利于反应的自发进行,但是不一定所有的放热反应都是自发反应,故A错误;
B、熵增大的反应有利于反应的自发进行,所以化学反应的方向与反应的熵变有关,故B错误;
C、CaCO3(s)═CaO(s)+CO2(g)气体的量增大,△S>0,因为室温下不能自发进行,说明该反应的△H>0,故C错误;
D、同一物质:固体→液体→气体的变化时吸收能量焓增和混乱程度变大熵增的过程,故D正确;
故选D.
点评 本题考查学生影响化学反应方向的因素是:焓变和熵变,注意化学反应能否自发进行的判据是看△H-T△S是否小于零,必须综合考虑体系的焓变和熵变.


科目:高中化学 来源: 题型:解答题
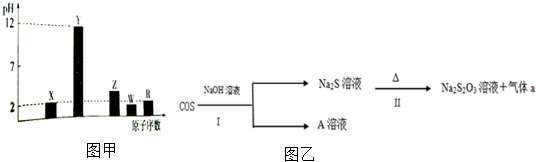
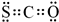 .
.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 在化学反应过程中,吸热反应需不断从外界获得能量,放热反应不需从外界获得能量 | |
| B. | 由C(石墨,S)═C(金刚石,S)△H=+1.9kJ•mol-1,可知金刚石比石墨稳定 | |
| C. | 已知常温常压下:HCl(aq)+NaOH(aq)=NaCl(aq)+H2O(l)△H=-57.3 kJ•mol-1,则有:H2SO4(aq)+Ba(OH)2(aq)=BaSO4(s)+2H2O(l)△H=-114.6 kJ•mol-1 | |
| D. | 已知:S(s)+O2(g)=SO2(g)△H1=-Q1 kJ•mol-1,S(g)+O2(g)=SO2(g)△H2=-Q2kJ•mol-1,则Q1<Q2 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
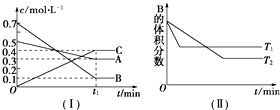 T℃时,A气体与B气体反应生成C气体,反应过程中A、B、C浓度变化如图(Ⅰ)所示,若保持其他条件不变,温度分别为T1和T2时,B的体积分数与时间的关系如图(Ⅱ)所示.根据以上条件,回答下列问题:
T℃时,A气体与B气体反应生成C气体,反应过程中A、B、C浓度变化如图(Ⅰ)所示,若保持其他条件不变,温度分别为T1和T2时,B的体积分数与时间的关系如图(Ⅱ)所示.根据以上条件,回答下列问题:查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 2KOH(aq)+H2SO4(aq)═K2SO4(aq)+2H2O(1)△H=-114.6 kJ•mol-1此时中和热△H=-114.6 kJ•mol-1 | |
| B. | NaOH(aq)+HCl(aq)═NaCl(aq)+H2O(1)△H=+57.3 kJ•mol-1 | |
| C. | H2SO4和NaOH反应的中和热△H=-57.3 kJ•mol-1 | |
| D. | 稀醋酸与稀NaOH溶液反应生成1 mol水,放出57.3 kJ 热量 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 胶体粒子带电荷并且在一定条件下能稳定存在 | |
| B. | 胶体粒子不能穿过半透膜,能通过滤纸空隙 | |
| C. | 胶体的分散质粒子直径在1nm~100nm之间 | |
| D. | 胶体粒子能够发生布朗运动而且能产生丁达尔现象 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | NH4+ K+ NO3- Cl- | B. | NO3- CO32- K+ Na+ | ||
| C. | K+ Na+ Cl- SO42- | D. | Mg2+ Cu2+ SO42- Cl- |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com