
科目:高中化学 来源: 题型:推断题
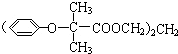 ,可用于降低血液中的胆固醇,该物质合成线路如图所示:
,可用于降低血液中的胆固醇,该物质合成线路如图所示: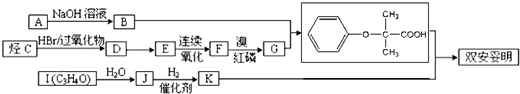
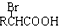 $\stackrel{苯酸钠}{→}$
$\stackrel{苯酸钠}{→}$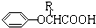
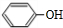 .
.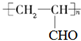
 +K→双安妥明”的化学方程式为
+K→双安妥明”的化学方程式为 .
.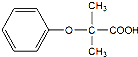 的同分异构体有6种(不考虑立体异构)
的同分异构体有6种(不考虑立体异构)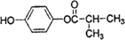 (写结构简式).
(写结构简式).查看答案和解析>>
科目:高中化学 来源: 题型:填空题
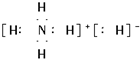 .
.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 32g氧气含有2NA个氧原子 | |
| B. | 32g臭氧含有2NA个氧原子 | |
| C. | 32g氧气和臭氧的混合气体中含有2NA个氧原子 | |
| D. | 32g氧气和臭氧的混合气体含有NA个氧原子 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
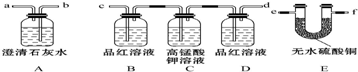
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
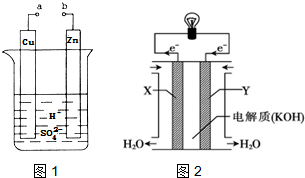
查看答案和解析>>
科目:高中化学 来源: 题型:推断题
 .
.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| R | ||
| X | Y | Z |
| A. | Y的氢化物比R的氢化物稳定 | |
| B. | 原子半径大小顺序是Z>Y>X | |
| C. | Y、R形成化合物的化合物YR2能使KMnO4溶液褪色 | |
| D. | X、Z可形成化合物XZ3,且该化合物属离子化合物 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com