
下列各项判断中正确的是
[ ]
A.某元素其中一种核素相对原子质量为m,则该元素的相对原子质量为m
B.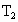 、
、 互为同位素
互为同位素
C.中子的质量大于质子的质量
D.同一元素的不同核素之间互称为同位素
 轻松暑假总复习系列答案
轻松暑假总复习系列答案科目:高中化学 来源: 题型:阅读理解
| ||
| ||
查看答案和解析>>
科目:高中化学 来源: 题型:
| 第一组 | He-268.8 | (a)-249.5 | Ar-185.8 | Kr-151.7 |
| 第二组 | F2 -187.0 | Cl2 -33.6 | (b) 58.7 | I2 184.0 |
| 第三组 | (c) 19.4 | HCl-84.0 | HBr-67.0 | HI-35.3 |
| 第四组 | H2O 100.0 | H2S-60.2 | (d) 42.0 | H2Te-1.8 |
| A、abc的化学式分别为Ne2、Br2、HF |
| B、第三组与第四组相比较,化合物的稳定顺序为:HBr>d |
| C、第三组物质溶于水后,溶液的酸性:c>HCl>HBr>HI |
| D、第四组物质中H2O的沸点最高,是因为H2O分子内存在氢键 |
查看答案和解析>>
科目:高中化学 来源: 题型:013
下列各项判断中正确的是
[ ]
A.某元素其中一种核素相对原子质量为m,则该元素的相对原子质量为m
B. 、
、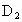 互为同位素
互为同位素
C.中子的质量大于质子的质量
D.同一元素的不同核素之间互称为同位素
查看答案和解析>>
科目:高中化学 来源: 题型:
根据元素周期律及晶体结构与性质判断,下列各项叙述中正确的组合是( )
①同一主族元素,原子半径越大,非金属单质的熔点一定越高
②同一周期元素的原子,半径越大越容易失去电子
③同一主族元素的氢化物,相对分子质量越大,它的沸点一定越高
④若X是原子晶体,Y是分子晶体,则熔点:X>Y
⑤若A2+2D―=2A―+D2,则还原性:D―>A―
⑥若R2―和M+的电子层结构相同,则原子序数:R>M
⑦若弱酸HA的酸性强于弱酸HB,则同浓度钠盐溶液的碱性:NaA<NaB
⑧VIA族元素的氢化物中稳定性最好的,其沸点也最高
A.①③⑤⑦ B.②④⑥⑧ C.①②③④⑥⑦⑧ D.①②④⑤⑦⑧
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com