
【题目】全钒液流储能电池是利用不同价态离子对的氧化还原反应来实现化学能和电能相互转化的装置,其原理如图所示。下列说法错误的是( )

A.放电过程中右槽溶液颜色逐渐由绿色变为紫色
B.放电过程中氢离子的作用之一是参与正极反应
C.充电过程中左槽溶液逐渐由蓝变黄
D.充电时若转移的电子数为3.01×1023个,左槽溶液中n(H+)的变化量为0.5mol
【答案】A
【解析】
A.根据图示电源的正负极连接方式可得,放电时,右侧电极是负极,发生氧化反应,V2+转化为V3+,溶液由紫色变为绿色,故A错误;
B.根据A项分析,放电时,右侧电极是负极,发生氧化反应,负极反应为:V2+-e-=V3+,左侧为正极,发生还原反应,正极反应为:VO2++2H++e-= VO2++H2O,负极区溶液中的氢离子通过交换膜进入正极区,所以氢离子的作用是参与正极反应和平衡电荷,故B正确;
C.根据A项分析,放电时,右侧电极是负极,发生氧化反应,则充电时,右侧电极是阴极,发生还原反应;放电时,左侧为正极,发生还原反应,充电时,左槽为阳极,发生氧化反应,阳极反应为:VO2++H2O- e-= VO2++2H+,溶液逐渐由蓝变黄,故C正确;
D.根据C项分析,充电时,左槽为阳极,发生氧化反应,阳极反应为:VO2++H2O- e-= VO2++2H+,根据电极反应,转移1mol电子,生成2mol H+,若转移的电子数为3.01×1023个,即转移0.5mol电子,左槽溶液中生成1mol H+,由于H+的作用是平衡电荷,同时有0.5mol H+从左槽移到右槽,所以,左槽溶液中氢离子的物质的量实际增多了0.5mol,故D正确;
答案选A。


科目:高中化学 来源: 题型:
【题目】研究表明CO与N2O在Fe+作用下发生反应的能量变化及反应历程如图所示,两步反应分別为:①N2O+Fe+=N2+FeO (慢):②FeO++CO=CO2+Fe+ (快)。下列说法正确的是

A. 反应①是氧化还原反应,反应②是非氧化还原反应
B. 两步反应均为放热反应,总反应的化学反应速率由反应②决定
C. Fe+使反应的活化能减小,FeO+是中间产物
D. 若转移lmol电子,则消耗II.2LN2O
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】现有易溶强电解质的混合溶液10L,其中可能含存![]() 、
、![]() 、
、![]() 、
、![]() 、
、![]() 、
、![]() 、
、![]() 、
、![]() 中的几种,向其中通入
中的几种,向其中通入![]() 气体,产生沉淀的量与通入
气体,产生沉淀的量与通入![]() 的量之间的关系如图所示,下列说法正确的是( )
的量之间的关系如图所示,下列说法正确的是( )
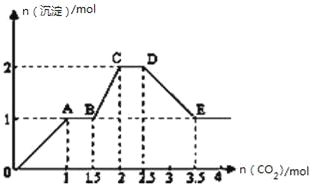
A.该溶液中能确定存在的离子是![]() 、
、![]() 、
、![]()
B.肯定不存在的离子是![]() 、
、![]()
C.若不能确定的离子中至少还存在一种阳离子,则该离子的最小浓度为0.2mol/L
D.OA段反应的离子方程式:2AlO2-+CO2+3H2O=2Al(OH)3↓+CO32-
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】联氨(N2H4)和次磷酸钠(NaH2PO2)都具有强还原性.都有着广泛的用途。
(1)已知:①N2H4(l)+O2(g)=N2(g)+2H2O(g) △H=-621.5 kJ●mol-1
②N2O4(l)-=N2(g)+2O2(g) △H2=+204.3 kJ●mol-1
则火箭燃料的燃烧反应为2N2H4(l)+N2O4(l)=3N2(g)+4H2O(g) △H=_____.
(2)已知反应N2H4(g)+ 2Cl2(g)![]() N2(g)+4HCl(g),T°C时,向V L恒容密闭容器中加入2 mol N2H4(g)和4 mol Cl2(g) ,测得Cl2和HCl的浓度随时间的关系如图所示。
N2(g)+4HCl(g),T°C时,向V L恒容密闭容器中加入2 mol N2H4(g)和4 mol Cl2(g) ,测得Cl2和HCl的浓度随时间的关系如图所示。
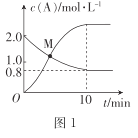
①0~ 10 min内,用N2(g)表示的平均反应速率v(N2)=_______。
②M点时,N2H4的转化率为______(精确到0.1)%。
③T °C时,达到平衡后再向该容器中加入1.2 mol N2H4(g)、0.4 mol Cl2(g)、0. 8 mol N2 (g)、1.2 mol HCl(g) ,此时平衡______(填“正向移动”“逆向移动”或“不移动”)。
(3)①在惰性气体中,将黄磷(P4)与石灰乳和碳酸钠溶液一同加入高速乳化反应器中制得NaH2PO2,同时还产生磷化氢(PH3)气体,该反应的化学方程式为________________。
②次磷酸(H3PO2)是一元酸,常温下.1.0 mol●L-1的NaH2PO2溶液pH为8,则次磷酸的Ka=___________。
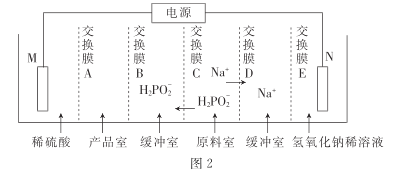
③用次磷酸钠通过电渗析法制备次磷酸.装置如图2所示。交换膜A属于____(填“阳离子”或“阴离子”)交换膜,电极N的电极反应式为______,当电路中流过3.8528×105库仑电量时.制得次磷酸的物质的量为_____ (一个电子的电量为 1.6×10- 19库仑,NA数值约为6. 02× 1023)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在盛有饱和硫酸钠溶液的烧杯中,保持温度不变,用惰性电极电解一定时间后( )
A. 溶液的pH值将增大B. 钠离子数和硫酸根离子数的比值将变小
C. 溶液的浓度逐渐增大,有一定量晶体析出D. 溶液的浓度不变,有晶体析出
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列各装置中都盛有0.1 mol·L-1 的NaCl溶液,放置一定时间后,锌片的腐蚀速率由快到慢的顺序是:( )

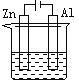

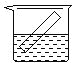
① ② ③ ④
A. ③①④②B. ①②④③C. ①②③④D. ②①④③
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某二元弱酸(简写为H2B)溶液,按下式发生一级和二级电离:
H2B![]() H++HB-
H++HB-
HB-![]() H++B2-
H++B2-
已知相同浓度时的电离度a(H2B)>>a(HB-),现有下列四种溶液:
①0.01molL-1的H2B溶液
②0.01molL-1的NaHB溶液
③0.02molL-1的HCl溶液与0.04molL-1的NaHB溶液等体积混合后的溶液
④0.02molLL-1的NaOH溶液与0.02molL-1的NaHB溶液等体积混合后的溶液
下列说法错误的是( )
A.溶液④一定显碱性B.c(H2B)最大的是③
C.c(B2-)最小的是①D.c(H+)最大的是③
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】电化学在日常生活中用途广泛,如图①是镁、次氯酸钠燃料电池的示意图,电池总反应式为:Mg+ClO-+H2O=Cl-+Mg(OH)2↓。如图②是电解法除去工业废水中的Cr2O72-,下列说法正确的是( )
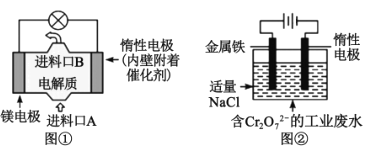
A.图①中镁电极发生的反应是:ClO-+H2O+2e-=Cl-+2OH-
B.图②最终得到Fe(OH)3和Cr(OH)3,则阳极上的电极反应式为:Fe-3e-=Fe3+
C.图②中每转移0.2mol电子,阴极逸出2.24LH2
D.若图①中7.2gMg溶解产生的电量用于图②废水处理,理论得到Fe(OH)3的物质的量为0.3mol
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知:①H2(g)+![]() O2(g)=H2O(g) ΔH1=akJ·mol1
O2(g)=H2O(g) ΔH1=akJ·mol1
②2H2(g)+O2(g)=2H2O(g) ΔH2=bkJ·mol1
③H2(g)+![]() O2(g)=H2O(l) ΔH3=ckJ·mol1
O2(g)=H2O(l) ΔH3=ckJ·mol1
④2H2(g)+O2(g)=2H2O(l) ΔH4=d kJ·mol1
下列关系式中正确的是
A.a<c<0B.b>d>0C.2a=b<0D.2c=d>0
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com