
”¾ĢāÄæ”æĻĀĮŠÓŠ¹ŲČČ»Æѧ·½³ĢŹ½µÄŠšŹöÖŠ£¬ÕżČ·µÄŹĒ £Ø £©
A.ŗ¬20.0gNaOHµÄĻ”ČÜŅŗÓė×ćĮæµÄĻ”ĮņĖįĶźČ«ÖŠŗĶ£¬·Å³ö28.7kJµÄČČĮ棬Ōņ±ķŹ¾ÖŠŗĶČȵÄČČ»Æѧ·½³ĢŹ½ĪŖ:2NaOH(aq)+H2SO4(aq)=Na2SO4(aq)+2H2O(l) H=-114.6kJ/mol
B.ŅŃÖŖČČ»Æѧ·½³ĢŹ½£ŗ SO2(g)+![]() O2(g)
O2(g) ![]() SO3(g) H=-98.32kJ/mol£¬ŌŚČŻĘ÷ÖŠ³äČė2mol SO2ŗĶ1mol O2³ä·Ö·“Ó¦£¬×īÖշųöµÄČČĮæĪŖ196.64kJ
SO3(g) H=-98.32kJ/mol£¬ŌŚČŻĘ÷ÖŠ³äČė2mol SO2ŗĶ1mol O2³ä·Ö·“Ó¦£¬×īÖշųöµÄČČĮæĪŖ196.64kJ
C.ŅŃÖŖ2H2(g)+O2(g) =2H2O(g)H=-483.6kJ/mol£¬ŌņH2µÄČ¼ÉÕČČĪŖ241.8kJ/mol
D.ÓĆĻ”°±Ė®ÓėĻ”ŃĪĖį½ųŠŠÖŠŗĶČČµÄ²ā¶ØŹµŃ飬¼ĘĖćµĆµ½µÄÖŠŗĶČȵÄHĘ«“ó
”¾“š°ø”æD
”¾½āĪö”æ
A.øł¾ŻÖŠŗĶČȵÄøÅÄīæÉÖŖ£¬ÖŠŗĶČȵÄČČ»Æѧ·½³ĢŹ½Ó¦øĆĪŖ:NaOH(aq)+1/2H2SO4(aq)=1/2Na2SO4(aq)+H2O(l) H=-57.3kJ/mol£¬¹ŹA“ķĪó£»
B. ¶žŃõ»ÆĮņµÄ“ß»ÆŃõ»ÆŹĒæÉÄę·“Ó¦£¬½«2mol SO2ŗĶ1mol O2³äČėŅ»ĆܱÕČŻĘ÷ÖŠ·“Ó¦£¬·Å³öµÄČČĮæŠ”ÓŚ196.64kJ£¬¹ŹB“ķĪó£»
C. Č¼ÉÕČȵĶØŅåĪŖ1molæÉČ¼ĪļĶźČ«Č¼ÉÕÉś³ÉĪȶØŃõ»ÆĪļŹ±·Å³öµÄČČĮ棬ӦøĆÉś³ÉŅŗĢ¬Ė®²ÅæÉÅŠ¶Ļ£¬¹ŹC“ķĪó£»
D.ŅņĪŖŅ»Ė®ŗĻ°±ĪŖŅ»ŌŖČõ¼ī£¬µēĄėŅŖĪüČČ£¬Ōģ³ÉĖł²āÖŠŗĶČČĘ«“󣬹ŹDÕżČ·£»
“š°ø£ŗD



| Äź¼¶ | øßÖŠæĪ³Ģ | Äź¼¶ | ³õÖŠæĪ³Ģ |
| øßŅ» | øßŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” | ³õŅ» | ³õŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” |
| ø߶ž | ø߶žĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õ¶ž | ³õ¶žĆā·ŃæĪ³ĢĶĘ¼ö£” |
| øßČż | øßČżĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õČż | ³õČżĆā·ŃæĪ³ĢĶĘ¼ö£” |
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æøł¾ŻĻĀĮŠ½į¹¹Ź¾ŅāĶ¼£¬ÅŠ¶ĻĻĀĮŠĖµ·ØÖŠÕżČ·µÄŹĒ

A. ŌŚNaCl¾§ĢåÖŠ£¬¾ąNa+×ī½üµÄ¶ąøöCl-¹¹³ÉÕżĖÄĆęĢå
B. ŌŚCaF2¾§ĢåÖŠ£¬Ca2+µÄÅäĪ»ŹżĪŖ4
C. ŌŚ½šøÕŹÆ¾§ĢåÖŠ£¬Ģ¼Ō×ÓÓėĢ¼Ģ¼¼üŹżÖ®±ČĪŖ1£ŗ2
D. øĆĘųĢ¬ĶÅ“Ų·Ö×ӵķÖ×ÓŹ½ĪŖEF»ņFE
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æ20ŹĄ¼Ķ50Äź“śæĘѧ¼ŅĢį³ö¼Ū²ćµē×Ó¶Ō»„³āÄ£ŠĶ(¼ņ³ĘVSEPRÄ£ŠĶ)£¬ÓĆÓŚŌ¤²ā¼ņµ„·Ö×ÓĮ¢Ģå½į¹¹”£ĘäŅŖµćæÉŅŌøÅĄØĪŖ£ŗ
¢ń”¢ÓĆAXnEm±ķŹ¾Ö»ŗ¬Ņ»øöÖŠŠÄŌ×ӵķÖ×Ó×é³É£¬AĪŖÖŠŠÄŌ×Ó£¬XĪŖÓėÖŠŠÄŌ×ÓĻą½įŗĻµÄŌ×Ó£¬EĪŖÖŠŠÄŌ×Ó×īĶā²ćĪ“²ĪÓė³É¼üµÄµē×Ó¶Ō(³ĘĪŖ¹Ā¶Ōµē×Ó)£¬(n£«m)³ĘĪŖ¼Ū²ćµē×Ó¶ŌŹż”£·Ö×ÓÖŠµÄ¼Ū²ćµē×Ó¶Ō×ÜŹĒ»„ĻąÅųā£¬¾łŌČµÄ·Ö²¼ŌŚÖŠŠÄŌ×ÓÖÜĪ§µÄæռ䣻
¢ņ”¢·Ö×ÓµÄĮ¢Ģå¹¹ŠĶŹĒÖø·Ö×ÓÖŠµÄŌ×ÓŌŚæÕ¼äµÄÅŲ¼£¬²»°üĄØÖŠŠÄŌ×ÓĪ“³É¼üµÄ¹Ā¶Ōµē×Ó£»
¢ó”¢·Ö×ÓÖŠ¼Ū²ćµē×Ó¶ŌÖ®¼äµÄ³āĮ¦Ö÷ŅŖĖ³ŠņĪŖ£ŗi”¢¹Ā¶Ōµē×ÓÖ®¼äµÄ³āĮ¦£¾¹Ā¶Ōµē×Ó¶ŌÓė¹²ÓƵē×Ó¶ŌÖ®¼äµÄ³āĮ¦£¾¹²ÓƵē×Ó¶ŌÖ®¼äµÄ³āĮ¦£»ii”¢Ė«¼üÓėĖ«¼üÖ®¼äµÄ³āĮ¦£¾Ė«¼üÓėµ„¼üÖ®¼äµÄ³āĮ¦£¾µ„¼üÓėµ„¼üÖ®¼äµÄ³āĮ¦£»iii”¢XŌ×ӵƵē×ÓÄÜĮ¦Ō½Čõ£¬A£XŠĪ³ÉµÄ¹²ÓƵē×Ó¶ŌÖ®¼äµÄ³āĮ¦Ō½Ē棻iv”¢ĘäĖū”£Ēė׊ĻøŌĶĮÉĻŹö²ÄĮĻ£¬»Ų“šĻĀĮŠĪŹĢā£ŗ
(1)øł¾ŻŅŖµćIæÉŅŌ»³öAXnEmµÄVSEPRĄķĻėÄ£ŠĶ£¬ĒėĢīŠ“ĻĀ±ķ£ŗ
n£«m | 2 | ________ |
VSEPRĄķĻėÄ£ŠĶ | ________ | ÕżĖÄĆęĢå |
¼Ū²ćµē×Ó¶ŌÖ®¼äµÄĄķĻė¼ü½Ē | ________ | 109”ć28”ä |
(2)ĒėÓĆVSEPRÄ£ŠĶ½āŹĶCO2ĪŖÖ±ĻߊĶ·Ö×ÓµÄŌŅņ_________________________________£»
(3)H2O·Ö×ÓµÄĮ¢Ģå¹¹ŠĶĪŖ£ŗ___________________£¬ĒėÄćŌ¤²āĖ®·Ö×ÓÖŠ”ĻH£O£HµÄ“óŠ”·¶Ī§²¢½āŹĶŌŅņ______________________________________________________________£»
(4)SO2Cl2ŗĶSO2F2¶¼ŹōAX4E0ŠĶ·Ö×Ó£¬S£½OÖ®¼äŅŌĖ«¼ü½įŗĻ£¬S£Cl”¢S£FÖ®¼äŅŌµ„¼ü½įŗĻ”£ĒėÄćŌ¤²ā SO2Cl2ŗĶSO2F2·Ö×ÓµÄĮ¢Ģå¹¹ŠĶ£ŗ_____________________________£¬ SO2Cl2·Ö×ÓÖŠ”ĻCl£S£Cl________________(Ń”Ģī”°£¼”±”¢”°£¾”±»ņ”°£½”±)SO2F2·Ö×ÓÖŠ”ĻF£S£F”£
(5)ÓĆ¼Ū²ćµē×Ó¶Ō»„³āĄķĀŪ(VSEPR)ÅŠ¶ĻĻĀĮŠ·Ö×Ó»ņĄė×ÓµÄæռ乹ŠĶ
·Ö×Ó»ņ Ąė×Ó | PbCl2 | XeF4 | SnCl62- | PF3Cl2 | HgCl42- | ClO4-- |
æÕ¼ä ¹¹ŠĶ | _____ | _____ | _____ | _____ | _____ | _____ |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æĮ×»ÆĒā£Ø![]() £©”¢ŃõĮņ»ÆĢ¼£ØCOS£©¾łæÉ×÷“¢Įøŗ¦³ęɱ¼Į”£Ēė»Ų“šĻĀĮŠĪŹĢā£ŗ
£©”¢ŃõĮņ»ÆĢ¼£ØCOS£©¾łæÉ×÷“¢Įøŗ¦³ęɱ¼Į”£Ēė»Ų“šĻĀĮŠĪŹĢā£ŗ
£Ø1£©Į×Ō×ÓµÄŗĖĶāµē×ÓÅŲ¼Ź½______________£¬ŗĖĶāÓŠ______ÖÖ²»Ķ¬ÄÜĮæµÄµē×Ó£»Ęä×īĶā²ćÓŠ____ÖÖŌĖ¶ÆדĢ¬²»Ķ¬µÄµē×Ó£¬ÕāŠ©µē×ÓÕ¼¾ŻµÄ¹ģµĄŹżĪŖ____øö”£
£Ø2£©ŃõĮņ»ÆĢ¼ÖŠ£¬ŌŖĖŲµÄ·Ē½šŹōŠŌ×īĒæµÄŌŖĖŲŌŚÖÜĘŚ±ķÖŠµÄĪ»ÖĆŹĒ______£»ŅŃÖŖCOSÓė![]() µÄ½į¹¹ĻąĖĘ£¬ŹŌŠ“³öCOSµÄµē×ÓŹ½______________£¬COSŹōÓŚ_____·Ö×Ó£ØĢī”°¼«ŠŌ”±»ņ”°·Ē¼«ŠŌ”±£©”£
µÄ½į¹¹ĻąĖĘ£¬ŹŌŠ“³öCOSµÄµē×ÓŹ½______________£¬COSŹōÓŚ_____·Ö×Ó£ØĢī”°¼«ŠŌ”±»ņ”°·Ē¼«ŠŌ”±£©”£
ŃõĮņ»ÆĢ¼Ė®½ā¼°²æ·ÖÓ¦ÓĆĮ÷³ĢČēĻĀ£Ø²æ·Ö²śĪļŅŃĀŌČ„£©£ŗ
COS![]() H2S
H2S![]() Na2S
Na2S![]() MČÜŅŗ+H2
MČÜŅŗ+H2
£Ø3£©Š“³ö·“Ó¦¢ņµÄĄė×Ó·½³ĢŹ½£ŗ_____________________£»
£Ø4£©ĮņĖį¹¤ŅµÉś²śÖŠ½Ó“„ŹŅÄŚ·¢ÉśµÄ·“Ó¦·½³ĢŹ½ĪŖ___________£»ŌŚŹµ¼ŹÉś²śÖŠ£¬²Ł×÷ĪĀ¶ČŃ”¶Ø400~500”ę”¢Ń¹ĒæĶس£²ÉÓĆ³£Ń¹µÄŌŅņ·Ö±šŹĒ____________”£
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æŌŚ“߻ƼĮ“ęŌŚĻĀ£¬![]() æÉÓĆĄ“Ļū³żNOµÄĪŪČ¾£¬Éś³ÉĮ½ÖÖ¶Ō»·¾³ĪŽŗ¦µÄĪļÖŹ”£Š“³ö·“Ó¦µÄ»Æѧ·½³ĢŹ½_______£¬øĆ·“Ó¦ÖŠŃõ»Æ²śĪļÓė»¹Ō²śĪļµÄĪļÖŹµÄĮæÖ®±ČŹĒ______”£
æÉÓĆĄ“Ļū³żNOµÄĪŪČ¾£¬Éś³ÉĮ½ÖÖ¶Ō»·¾³ĪŽŗ¦µÄĪļÖŹ”£Š“³ö·“Ó¦µÄ»Æѧ·½³ĢŹ½_______£¬øĆ·“Ó¦ÖŠŃõ»Æ²śĪļÓė»¹Ō²śĪļµÄĪļÖŹµÄĮæÖ®±ČŹĒ______”£
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æÓŠ¹Ųŗ¬µŖ»ÆŗĻĪļµÄŠŌÖŹŹµŃ锣

¢ń.Ä³ŃŠ¾æŠŌѧĻ°Š”×éĄūÓĆČēĶ¼×°ÖĆŃŠ¾æĻõĖįµÄŠŌÖŹ”£
ŹµŃéŅ»£ŗ¼×Ķ¬Ń§ÓĆČēĶ¼×°ÖĆĄ“Ö¤ŹµĻ”ĻõĖįÓėĶ·“Ӧɜ³ÉNO
£Ø1£©“ÓAÖŠĻņUŠĪ¹Ü֊עĀśĻ”ĻõĖįŗ󣬷¢ÉśµÄĻÖĻóŹĒ___”£
£Ø2£©ŅŌĻĀŹÕ¼ÆNOĘųĢåµÄø÷ÖÖ×°ÖĆÖŠ£¬ŗĻĄķµÄŹĒ___”£(ĢīŠņŗÅ£¬¶ąŃ”²»øų·Ö)

£Ø3£©ŌŚ100mL»ģŗĻČÜŅŗÖŠ£¬HNO3ŗĶH2SO4µÄĪļÖŹµÄĮæÅØ¶Č·Ö±šŹĒ0.4mol/L£¬0.1mol/L£¬ĻņøĆ»ģŗĻŅŗÖŠ¼ÓČė1.92gĶ·Ū£¬¼ÓČČ“ż³ä·Ö·“Ó¦ŗó£¬ĖłµĆČÜŅŗÖŠCu2£«µÄĪļÖŹµÄĮæÅØ¶ČŹĒ__”£
ŹµŃ鶞£ŗŅŅ×éĶ¬Ń§ĄūÓĆÉĻŹö×°ÖĆĶź³ÉÅØĻõĖįÓėĶµÄ·“Ó¦
£Ø4£©ŅŅ×éĶ¬Ń§·¢ĻÖŹµŃéŹŅĄļÓŠ¼øĘæÅØĻõĖį³Ź»ĘÉ«£¬ĒėÓĆ»Æѧ·½³ĢŹ½ŗĶ¼ņµ„µÄĪÄ×ÖĖµĆ÷½āŹĶÕāÖÖĻÖĻó£ŗ ___”£
¢ņ.ijĶ¬Ń§ÓĆČēĶ¼ŹµŃé×°ÖĆ(ĘäÖŠ¼īŹÆ»ŅĪŖ¹ĢĢåĒāŃõ»ÆÄĘŗĶÉśŹÆ»ŅµÄ»ģŗĻĪļ)ÖĘČ”°±Ęų”£Ēė»Ų“šĻĀĮŠĪŹĢā£ŗ

£Ø5£©Š“³öÖĘČ”°±ĘųµÄ»Æѧ·½³ĢŹ½£ŗ___”£
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æĄūÓĆČēĶ¼ĖłŹ¾×°ÖĆ£¬µ±X”¢YŃ”ÓĆ²»Ķ¬²ÄĮĻŹ±£¬æɽ«µē½āŌĄķ¹ć·ŗÓ¦ÓĆÓŚ¹¤ŅµÉś²ś”£ĻĀĮŠĖµ·ØÖŠÕżČ·µÄŹĒ
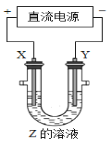
A. ĀČ¼ī¹¤ŅµÖŠ£¬X”¢Y¾łĪŖŹÆÄ«£¬Yø½½üÄܵƵ½ĒāŃõ»ÆÄĘ
B. ĶµÄ¾«Į¶ÖŠ£¬XŹĒ“æĶ£¬YŹĒ“ÖĶ£¬ZŹĒCuSO4
C. µē¶Ę¹¤ŅµÖŠ£¬XŹĒ“ż¶Ę½šŹō£¬YŹĒ¶Ę²ć½šŹō
D. Ķā¼ÓµēĮ÷µÄŅõ¼«±£»¤·ØÖŠ£¬XŹĒ“ż±£»¤½šŹō
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æŅ»¶ØĪĀ¶ČĻĀ£¬ŌŚČżøöĢå»ż¾łĪŖ1.0 L µÄŗćČŻĆܱÕČŻĘ÷ÖŠ·¢Éś·“Ó¦£ŗ2A(g)![]() B(g)+C(g) ¦¤H
B(g)+C(g) ¦¤H
ČŻĘ÷ ±ąŗÅ | ĪĀ¶Č(”ę) | ĘšŹ¼ĪļÖŹµÄĮæ(mol) | Ę½ŗāĪļÖŹµÄĮæ(mol) | |
A(g) | B(g) | C(g) | ||
¢ń | 387 | 0. 20 | 0. 080 | 0. 080 |
¢ņ | 387 | 0. 40 | ||
¢ó | 207 | 0. 20 | 0. 090 | 0. 090 |
ĻĀĮŠĖµ·Ø²»ÕżČ·µÄŹĒ
A. øĆ·“Ó¦µÄÕż·“Ó¦ĪŖ¦¤H<0
B. 207”ę£¬K=4
C. “ļµ½Ę½ŗāŹ±£¬ČŻĘ÷¢ńÖŠµÄAĢå»ż·ÖŹżÓėČŻĘ÷¢ņÖŠµÄĻąĶ¬
D. ČŻĘ÷¢ńÖŠ·“Ó¦µ½“ļĘ½ŗāĖłŠčŹ±¼ä±ČČŻĘ÷¢óÖŠµÄ¶Ģ
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æĮņ»ĘŌŚæÕĘųÖŠČ¼ÉÕÉś³ÉĘųĢå¼×£¬¼×ČÜÓŚĖ®µĆČÜŅŗŅŅ£¬ĻņŅŅČÜŅŗÖŠµĪ¼ÓäåĖ®£¬äåĖ®ĶŹÉ«£¬ŅŅ±ä³É±ū”£ŌŚ±ūĄļ¼ÓČėNa2SÉś³ÉĘųĢ嶔£¬°Ń¶”ĶØČėŅŅµĆµ½³ĮµķĪģ”£¼×”¢ŅŅ”¢±ū”¢¶””¢Īģ¾łŗ¬ÓŠĮņŌŖĖŲ£¬ŌņĖüĆĒÕżČ·µÄĖ³ŠņŹĒ
A. SO3ӢH2SO4ӢH2SO3ӢH2SӢSB. SO2ӢH2SO3ӢH2SO4ӢSO2ӢSO3
C. SO3 ӢH2SO4ӢH2SO3ӢSO2ӢNa2S2O3D. SO2ӢH2SO3ӢH2SO4ӢH2SӢS
²éæ““š°øŗĶ½āĪö>>
°Ł¶ČÖĀŠÅ - Į·Ļ°²įĮŠ±ķ - ŹŌĢāĮŠ±ķ
ŗž±±Ź”»„ĮŖĶųĪ„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±ØĘ½ĢØ | ĶųÉĻÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | µēŠÅÕ©Ę¾Ł±Ø×ØĒų | É꥜Ź·ŠéĪŽÖ÷ŅåÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | ÉęĘóĒÖČؾŁ±Ø×ØĒų
Ī„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±Øµē»°£ŗ027-86699610 ¾Ł±ØÓŹĻä£ŗ58377363@163.com