
| A. | 在酯水解试验中,可以通过观察酯层消失的时间差异,来判断乙酸乙酯在不同条件下水解速率的差别 | |
| B. | 探究“温度影响硫代硫酸钠与稀硫酸反应速率的因素”的实验中,需要用到的计量仪器只需量筒、温度计 | |
| C. | 在溴富集过程中,可在分液漏斗中加入4mL溴水,再向其中加入10mL四氯化碳,振荡,静置、分液,得下层液体 | |
| D. | 实验室制备乙烯常用硫酸铜溶液洗气 |
分析 A.乙酸乙酯不溶于水,通过乙酸乙酯的油层厚度来确定乙酸乙酯的水解程度;
B.该实验所需的计量仪器有量筒、温度计和秒表;
C.溴水与四氯化碳比例应为溴水较多;
D.乙烯中不含硫化氢.
解答 解:A.由于乙酸乙酯不溶于水,所以乙酸乙酯在水中形成油层,可以通过观察油层的消失时间判断乙酸乙酯的水解程度,故A正确;
B.该实验需要量取溶液的体积、称量反应体系的温度和记录溶液变浑浊的时间,故所需的计量仪器有量筒、温度计和秒表,故B错误;
C.溴的萃取实验中,溴水体积较大,四氯化碳体积较小,故C错误;
D.乙烯中不含硫化氢,不需要用硫化氢洗气,故D错误.
故选A.
点评 本题考查化学实验方案的评价,为高频考点,涉及物质性质的探究、混合物分离提纯等,把握物质的性质、反应原理、实验技能为解答的关键,侧重分析与实验能力的考查,注意实验的评价性分析,题目难度不大.


 励耘书业暑假衔接宁波出版社系列答案
励耘书业暑假衔接宁波出版社系列答案科目:高中化学 来源: 题型:解答题
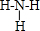 ,D2C含有的化学键类型为离子键;
,D2C含有的化学键类型为离子键;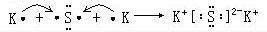 ;
;查看答案和解析>>
科目:高中化学 来源: 题型:选择题
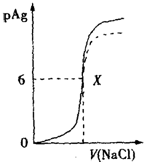 已知:pAg=-lg[c(Ag+)],Ksp(AgCl)=1.8×10-10,且Ksp(AgCl)>Ksp(AgI).如图是向10mL AgNO3溶液中逐渐加入0.1mol/L的NaCl溶液时,溶液的pAg随着加入NaCl溶液的体积(单位mL)变化的图象(实线).根据图象所得下列结论正确的是( )
已知:pAg=-lg[c(Ag+)],Ksp(AgCl)=1.8×10-10,且Ksp(AgCl)>Ksp(AgI).如图是向10mL AgNO3溶液中逐渐加入0.1mol/L的NaCl溶液时,溶液的pAg随着加入NaCl溶液的体积(单位mL)变化的图象(实线).根据图象所得下列结论正确的是( )| A. | 原AgNO3溶液的物质的量浓度为0.1 mol•L-1 | |
| B. | 图中X点的坐标为(10,6) | |
| C. | 图中X点对应溶液中Ag+与Cl-的浓度不相同 | |
| D. | 若把0.1 mol•L-1的NaCl溶液换成0.1 mol•L-1的NaI溶液,则图象在终点后变为虚线部分 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| 选项 | 陈述Ⅰ | 陈述Ⅱ |
| A | CaSO3是难溶物 | 向CaCl2溶液中通入SO2产生白色沉淀 |
| B | 明矾能水解生成Al(OH)3胶体 | 实验室用明矾与水反应制Al(OH)3 |
| C | SiO2是酸性氧化物 | SiO2与任何酸均不反应 |
| D | Zn具有还原性和导电性 | 可用作锌锰干电池的负极材料 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
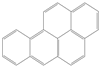 柴静在《穹顶之下》中介绍到雾霾中含有较大量的一种突变原和致癌物质--苯并[a]芘(Benzo-a-pyrene)(BAP).苯并芘是一种五环多环芳香烃类(结构如图所示),存在于汽车废气(尤其是柴油引擎)、烟草与木材燃烧产生的烟,以及炭烤食物中.关于苯并[a]芘的下列说法中正确的是( )
柴静在《穹顶之下》中介绍到雾霾中含有较大量的一种突变原和致癌物质--苯并[a]芘(Benzo-a-pyrene)(BAP).苯并芘是一种五环多环芳香烃类(结构如图所示),存在于汽车废气(尤其是柴油引擎)、烟草与木材燃烧产生的烟,以及炭烤食物中.关于苯并[a]芘的下列说法中正确的是( )| A. | BAP导电性优良,因其有共轭双键结构 | |
| B. | 五环多环芳香烃类都是BAP的同分异构体 | |
| C. | BAP有10种一硝基取代物 | |
| D. | BAP的分子式为C20H12 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 反应中硫酸作氧化剂 | |
| B. | NH4CuSO3中硫元素被氧化 | |
| C. | 刺激性气味的气体是氨气 | |
| D. | 1 mol NH4CuSO3完全反应转移0.5 mol电子 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
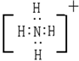 ;
;查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 酸、碱、盐都是电解质 | |
| B. | H2O与D2O互称同素异形体 | |
| C. | 石油的分馏和裂化均属于化学变化 | |
| D. | 只含共价键的物质,一定是共价化合物 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题

 ,GHOOC(CH2)4COOH;
,GHOOC(CH2)4COOH;查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com