
 某实验小组设计如下流程,模拟将汽车尾气中的氮氧化物(主要为NO和NO2的混合物)转化为工业用盐亚硝酸钠(NaNO2),并对亚硝酸钠进行多角度探究:汽车尾气$→_{操作①}^{20%NaOH}$溶液$\stackrel{操作②}{→}$固体$→_{③}^{操作}$NaNO2
某实验小组设计如下流程,模拟将汽车尾气中的氮氧化物(主要为NO和NO2的混合物)转化为工业用盐亚硝酸钠(NaNO2),并对亚硝酸钠进行多角度探究:汽车尾气$→_{操作①}^{20%NaOH}$溶液$\stackrel{操作②}{→}$固体$→_{③}^{操作}$NaNO2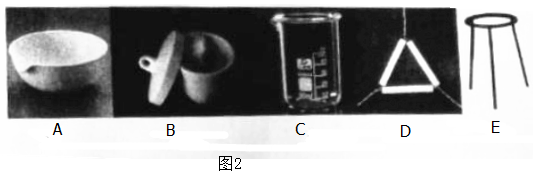
分析 Ⅰ.(1)根据配制溶质质量分数为20%的氯化钠溶液的步骤为:计算、称量、溶解、装瓶,结合每一步骤需要的仪器;
(2)导气管a可以平衡压强;
(3)操作③是高温分解固体,选择坩埚中加热分解硝酸钠,加热过程中需要用玻璃棒搅拌;
Ⅱ.(4)说明 NO2-有氧化性,则N元素的化合价降低,在酸性条件下,与还原剂KI反应即可;
(5)酸性KMnO4溶液氧化亚硝酸根离子为硝酸根离子,高锰酸根离子被还原为锰离子,结合原子守恒和电荷守恒可写出该反应的离子方程式;结合反应 的离子方程式定量关系计算反应的亚硝酸钠得到混合物中质量分数.
解答 解:I.(1)用固体氯化钠和水配制溶质质量分数为20%的氯化钠溶液的步骤为:计算、称量、量取、溶解、装瓶;
称量时用药匙取氯化钠固体,用托盘天平称量氯化钠固体;用量筒量、胶头滴管取所需水的体积;用烧杯溶解氯化钠,并用玻璃棒搅拌,所以需要的玻璃仪器有量筒、胶头滴管、烧杯、玻璃棒,配制20%NaOH溶液,除烧杯、玻璃棒外,还需要的玻璃仪器有量筒、胶头滴管,
故答案为:量筒、胶头滴管;
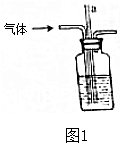
(2)操作中,实验小组同学将气体通入盛有NaOH溶液的烧杯,改用图1装置,玻璃管a的作用是保持容器内压强稳定,
故答案为:保持容器内压强稳定;
(3)操作③是高温分解硝酸钠固体,选择坩埚、泥三角、三脚架,
故答案为:BDE;
II.(4)说明 NO2-有氧化性,则N元素的化合价降低,在酸性条件下,与还原剂KI反应,所以选择的试剂为KI-淀粉溶液、稀硫酸,观察到溶液变蓝现象,证明其具有氧化性,
故答案为:取样,滴加稀硫酸和KI-淀粉溶液,若溶液变蓝,则证明 NO2-有氧化性;
(5 ) 酸性KMnO4溶液氧化亚硝酸根离子为硝酸根离子,高锰酸根离子被还原为锰离子,该反应的离子方程式为:5NO2-+2MnO4-+6H+=5NO3-+2Mn2++3H2O;当加入最后一滴KMnO4溶液时,溶液由无色变为紫色,且半分钟内不褪色;
结合反应的离子方程式定量关系计算反应的亚硝酸钠,
2MnO4-+5NO2-+6H+=2Mn2++5NO3-+3H2O
2 5
0.020L×0.1000mol•L-1 n
n=0.005mol
100.00ml溶液中NaNO2物质的量为0.005mol×4=0.02mol
得到混合物中质量分数=$\frac{0.02mol×69g/mol}{1.5g}$×100%=92%;
故答案为:5NO2-+2MnO4-+6H+=5NO3-+2Mn2++3H2O;当加入最后一滴KMnO4溶液时,溶液由无色变为紫色,且半分钟内不褪色;92%.
点评 考查了物质性质和物质组成实验验证分析判断,滴定实验计算应用,物质检验的方法,掌握基础是关键,题目难度中等.


 智趣暑假温故知新系列答案
智趣暑假温故知新系列答案科目:高中化学 来源: 题型:选择题
| A. | 为检验SO42-需要滴加稀硝酸酸化的BaCl2溶液并观察是否有白色沉淀生成 | |
| B. | 把光洁无锈的铁丝放在煤气灯外焰灼烧至与原来的火焰颜色相同时,蘸取K2CO3溶液并灼烧,透过蓝色钴玻璃可观察到火焰为淡紫色 | |
| C. | 向盛有足量苯酚溶液的试管中滴加少量稀溴水,可观察到白色沉淀生成 | |
| D. | 实验室制备乙炔时,常用NaOH溶液除去产生的H2S、PH3等杂质 |
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 原子半径:d>c>b>a | B. | 4种元素中b的金属性最强 | ||
| C. | c的氧化物的水化物是强碱 | D. | d单质的氧化性比a单质的氧化性强 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| W | X | |||
| Y | Z |
| A. | 氢化物沸点:W<Z | B. | 氧化物对应水化物的酸性:Y>W | ||
| C. | 化合物熔点:Y2X3<YZ3 | D. | 简单离子的半径:Y<X |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 若改为加入A物质可加快反应速率 | |
| B. | 达新平衡后B的转化率减小,A的转化率增大 | |
| C. | 达新平衡后A与B的转化率均增大 | |
| D. | 达新平衡后B的转化率不变,A的转化率增大 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 蒸馏 | B. | 升华 | C. | 干馏 | D. | 萃取 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
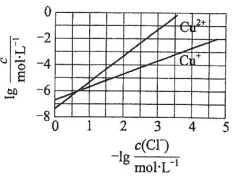 在湿法炼锌的电解循环溶液中,较高浓度的Cl-会腐蚀阳极板而增大电解能耗.可向溶液中同时加入Cu和CuSO4,生成CuCl沉淀从而除去Cl-.根据溶液中平衡时相关离子浓度的关系图,下列说法错误的是( )
在湿法炼锌的电解循环溶液中,较高浓度的Cl-会腐蚀阳极板而增大电解能耗.可向溶液中同时加入Cu和CuSO4,生成CuCl沉淀从而除去Cl-.根据溶液中平衡时相关离子浓度的关系图,下列说法错误的是( )| A. | Ksp(CuCl)的数量级为10-7 | |
| B. | 除Cl-反应为Cu+Cu2++2Cl-=2CuCl | |
| C. | 加入Cu越多,Cu+浓度越高,除Cl-效果越好 | |
| D. | 2Cu+=Cu2++Cu平衡常数很大,反应趋于完全 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题

查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com