
下列反应的离子方程式中正确的是 ( )
A.将Fe(OH)2投入稀HNO3中:Fe(OH)2+2H+=Fe2++2H2O
B.在Ba(OH)2溶液中滴入少量的KHCO3溶液:Ba2++2OH-+2HCO3-=BaCO3↓+CO32-+2H2O
C.在NaClO溶液中通入少量的SO2:ClO-+SO2+H2O=SO42-+Cl-+2H+
D.在硫酸氢钠溶液中滴加少量纯碱溶液:2H++CO32-=CO2↑+H2O
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源:2016-2017学年河北省高二12月月考化学卷(解析版) 题型:选择题
下列有关说法不正确的是( )
A.沿海城市建筑时直接从海洋里取用海沙,可以大大降低成本
B.“地沟油”禁止使用,但处理后可以制生物柴油和肥皂
C.乙醇溶液、双氧水均可用于杀菌消毒,但原理不同
D.维生素C和铁粉是常用的抗氧化剂
查看答案和解析>>
科目:高中化学 来源:2017届浙江省“七彩阳光”新高考研究联盟高三上考试化学试卷(解析版) 题型:选择题
下列说法正确的是
A.硬脂酸丙酯在碱性条件下的水解反应叫皂化反应
B.淀粉和纤维素在一定条件下水解均可得到葡萄糖
C.鸡蛋清的溶液中加入硫酸铵溶液,可使鸡蛋清凝聚而失去生理活性
D.蛋白质是只含有C、H、O、N四种元素的高分子化合物
查看答案和解析>>
科目:高中化学 来源:2017届湖南省怀化市高三上学期期中质检化学试卷(解析版) 题型:填空题
CO2是目前最主要的温室气体,减小CO2的排放并用来制造有价值的化学用品是目前的研究目标。
(1)利用CO2与CH4生产合成气(CO、H2):
已知:CH4(g)+2O2(g) CO2(g)+2H2O(g) ΔH=-890.3 KJ·mol-1
CO2(g)+2H2O(g) ΔH=-890.3 KJ·mol-1
CO(g)+H2O(g) CO2(g)+H2(g) ΔH=+2.8 KJ·mol-1
CO2(g)+H2(g) ΔH=+2.8 KJ·mol-1
2CO(g)+O2(g) 2CO2(g) ΔH=-566.0 KJ·mol-1
2CO2(g) ΔH=-566.0 KJ·mol-1
反应CO2(g)+CH4(g) 2CO(g)+2H2(g) ΔH= ____________。
2CO(g)+2H2(g) ΔH= ____________。
②250℃时,以镍合金为催化剂,向体积为4 L的密闭容器中通入6 mol CO2、6 mol CH4,开始发生如下反应:CO2(g)+CH4(g) 2CO(g)+2H2(g)。经过一段时间达到平衡,平衡体系中各组分体积分数(某一成分物质的量占总气体物质的量的百分数)如下表:
2CO(g)+2H2(g)。经过一段时间达到平衡,平衡体系中各组分体积分数(某一成分物质的量占总气体物质的量的百分数)如下表:
物质 | CH4 | CO2 | CO | H2 |
体积分数 | 0.1 | 0.1 | 0.4 | 0.4 |
此温度下该反应的平衡常数K=________________。
(2)以二氧化钛表面覆盖Cu2Al2O4为催化剂,可以将CO2和CH4直接转化成乙酸。在不同温度下催化剂的催化效率与乙酸的生成速率如下图所示。250~300℃时,乙酸的生成速率减小的可能原因是____________________。

(3) 如以氢氧化钾水溶液作电解质进行电解,CO2在铜电极上可转化为甲烷,该电极反应方程式为_____________________。
(4)将2mol CO2和6molH2容积相同而温度不同的Ⅰ、Ⅱ两个恒容密闭容器中开始发生反应:CO2(g)+3H2(g)  CH3OH(g)+H2O(g),测得CH3OH的物质的量随时间的变化如下图1所示。
CH3OH(g)+H2O(g),测得CH3OH的物质的量随时间的变化如下图1所示。


①曲线Ⅰ、Ⅱ对应的平衡常数大小关系为KⅠ_______KⅡ(填“>”“=”或“<”),可知该 反应是一个_______(填“放热”或“吸热”)反应。
②下列事实说明该反应已达到平衡状态的是_________________:
A.容器内气体压强保持不变
B.容器内气体的密度保持不变
C.CO2的体积分数保持不变
D.CO2的消耗速率与CH3OH的生成速率相等
E.容器内混合气体的平均相对分子质量保持不变
(5)利用光能和光催化剂,可将CO2和H2O(g)转化为CH4和O2。紫外光照射时,在不同催化剂(Ⅰ、Ⅱ、Ⅲ)作用下,CH4产量随光照时间的变化如上图2所示。在0~15小时内,CH4的平均生成速率Ⅰ、Ⅱ和Ⅲ从大到小的顺序为_____________(填序号)。
查看答案和解析>>
科目:高中化学 来源:2017届湖南省怀化市高三上学期期中质检化学试卷(解析版) 题型:选择题
在一密闭容器中反应aA(g) bB(g)达平衡后,测得c(B)为1mol/L。如保持温度不变,将容器体积变为原来的2倍,重新达到新的平衡时,c(B)变为0.6mol/L,则下列说法不正确的是( )
bB(g)达平衡后,测得c(B)为1mol/L。如保持温度不变,将容器体积变为原来的2倍,重新达到新的平衡时,c(B)变为0.6mol/L,则下列说法不正确的是( )
A.平衡向正反应方向移动 B.物质A的转化率增大
C物质B的质量分数增大 D.a>b
查看答案和解析>>
科目:高中化学 来源:2017届湖南省怀化市高三上学期期中质检化学试卷(解析版) 题型:选择题
下列有关实验的说法中正确的是 ( )
A. “左码右物”称量药品时称量结果一定偏小
B. 用pH试纸无法测出氯水的pH
C. 可用碱式滴定管量取15.65ml 0.10mol/LKMnO4溶液
D. 量取8.2ml浓硫酸时,仰视量筒刻度所得浓硫酸体积偏小
查看答案和解析>>
科目:高中化学 来源:2017届黑龙江哈尔滨六中高三上学期期末化学卷(解析版) 题型:推断题
【化学—选修5:有机化学基础】沐舒坦(结构简式为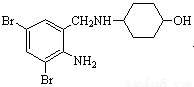 ,不考虑立体异构)是临床上使用广泛的。下图所示的其多条合成路线中的一条(反应试剂和反应条件均未标出)
,不考虑立体异构)是临床上使用广泛的。下图所示的其多条合成路线中的一条(反应试剂和反应条件均未标出)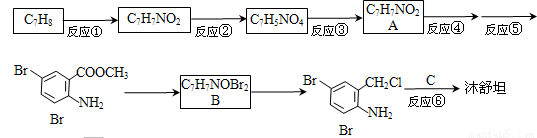
已知:
完成下列填空:
(1)写出反应①所用试剂和反应条件 ,反应⑥的化学反应方程式 。
(2)写出反应类型
反应③ 反应⑤
(3)写出结构简式
A B
(4)反应⑥中除加入反应试剂C外,还需要加入K2CO3,其目的是为了 ;
(5)写出两种C的能发生水解反应,且只含3种不同化学环境氢原子的同分异构体的结构简式 、
(6)反应②,反应③的顺序不能颠倒,其原因是 。
查看答案和解析>>
科目:高中化学 来源:2017届河北省高三上第五次调研化学卷(解析版) 题型:选择题
下图是CO2电催化还原为CH4的工作原理示意图。下列说法不正确的是( )

A.该过程是电能转化为化学能的过程
B.铜电极的电极反应式为CO2+8H++8e-=CH4+2H2O
C.一段时间后,① 池中n(KHCO3)不变
D.一段时间后,② 池中溶液的pH一定减小
查看答案和解析>>
科目:高中化学 来源:2016-2017学年江苏省高二12月模拟二化学卷(解析版) 题型:选择题
将5.10g镁铝合金加入120mL 4.0 mol•L-1的盐酸中,待合金完全溶解后,得到溶液X。下列说法一定正确的是
A.合金完全溶解后产生H2的物质的量为0.24mol
B.合金中镁与铝的物质的量之比小于1
C.若向溶液X中加入270mL 2.0 mol•L-1NaOH溶液,充分反应,所得沉淀为Mg(OH)2
D.若向溶液X中加入足量的氨水,充分反应,所得沉淀经过过滤、洗涤后充分灼烧,则残留固体质量大于8.50g
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com