
向1 L的密闭容器中加入1 mol X、0.3 mol Z和一定量的Y三种气体。一定条件下发生反应,各物质的浓度随时间变化如图一所示。图二为t2时刻后改变反应条件,平衡体系中反应速率随时间变化的情况,且四个阶段都各改变一种不同的条件。下列说法不正确的是
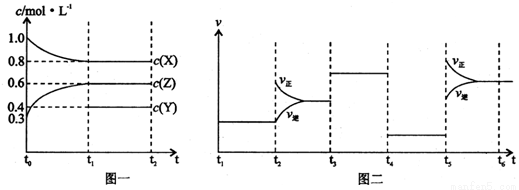
A.Y的起始物质的量为0.5 mol
B.该反应的化学方程式为:2X(g)+Y(g)  3Z(g) ∆H<0
3Z(g) ∆H<0
C.若t0=0,t1=10 s,则t0~t1 阶段的平均反应速率为v(Z)=0.03 mol/(L·s)
阶段的平均反应速率为v(Z)=0.03 mol/(L·s)
D.反应物X的转化率t6点比t3点高
 名师点睛字词句段篇系列答案
名师点睛字词句段篇系列答案科目:高中化学 来源:2016-2017学年广西省高一上模拟考试化学卷(解析版) 题型:选择题
下列离子能大量共存的是
A.使 无色酚酞试液呈红色的溶液中:Na+、K+、SO
无色酚酞试液呈红色的溶液中:Na+、K+、SO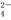 、CO
、CO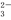
B.无色透明的溶液中:Cu2+、K+、SO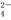 、NO
、NO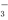
C.含有大量Ba(NO3)2的溶液中:Mg2 +、NH
+、NH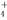 、SO
、SO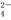 、Cl-
、Cl-
D.使紫色石蕊试液呈红色的溶液中:Na+、K+、CO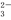 、NO
、NO
查看答案和解析>>
科目:高中化学 来源:2016-2017学年广西省高二上模拟考试化学卷(解析版) 题型:选择题
标准状况下,将V L A气体(摩尔质量为M g·mol-1)溶于0.1 L水中,所得溶液密度为ρ g·cm-3,则此溶液的物质的量浓度(mol·L-1)为
A.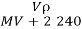
B.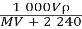
C.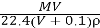
D.100VρM(MV+2240)
查看答案和解析>>
科目:高中化学 来源:2017届四川省绵阳市高三第二次诊断性考试化学试卷(解析版) 题型:选择题
常温下,用0.1000 mol/L的盐酸滴定20.00 mL未知浓度的Na2CO3溶液,溶液的pH与所加盐酸的体积关系如图所示。下列有关叙述正确的是
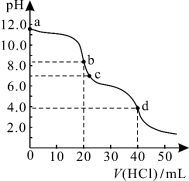
A.a点溶液呈碱性的原因用离子方程式表示为:CO +2H2O
+2H2O H2CO3+2OH-
H2CO3+2OH-
B.c点处的溶液中c(Na+)-c(Cl-)=c(HCO )+2c(CO
)+2c(CO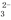 )
)
C.滴定过程中使用甲基橙作为指示剂比酚酞更准确
D.d点处溶液中水电离出的c(H+)大于b点处
查看答案和解析>>
科目:高中化学 来源:2017届天津市五区县高三上学期期末考试化学试卷(解析版) 题型:填空题
磷尾矿难溶于水,主要含Ca5(PO4)3F和CaCO3·MgCO3。某研究小组提出了用磷尾矿制备CaCO3、Mg(OH)2、P4和CO的方案,其工艺流程图如下:
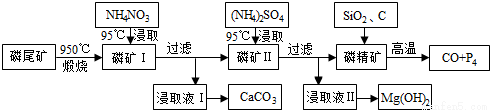
请回答下列问题:
(1)磷精矿[Ca5(PO4)3F]分解温度_______________(填“高于”、“低于” )950℃;
(2)NH4NO3溶液能从磷矿I中浸取出Ca2+的原因是________________,第一次浸取液用NH4NO3而不用的(NH4)2SO4原因是__________________________。
(3)磷精矿与SiO2、C发生反应时被还原的物质是_______________。
(4)其产物CO在工业上有重要的综合应用,现以CO、H2O、熔融Na2O组成的电池装置如图所示。
写出石墨Ⅰ电极上发生反应的电极反应式_______________,Na+向________(填写“石墨Ⅰ”或“石墨Ⅱ”)移动。
(5)CO也可由甲酸(HCOOH)制取,甲酸是易溶于水的一元弱酸。
①常温下关于1 L 0.1 mol·L-1  HCOONa溶液,下列关系不正确的是____________。
HCOONa溶液,下列关系不正确的是____________。
a.c(H+)·c(OH-)=1×10-14
b.c(H+)+c(HCOOH)=c(OH-)
c.c(Na+)=c(HCOOH)+c(HCOO -)
-)
d.c(Na+)>c(H+)>c(HCOO-)>c(OH-)
②向1 L 0.1 mol·L-1 HCOONa溶液中加水稀释后,c(HCOOH)·c(OH-)的数值________(填写“增大”“减 小”或“不变”)。
小”或“不变”)。
查看答案和解析>>
科目:高中化学 来源:2017届天津市五区县高三上学期期末考试化学试卷(解析版) 题型:选择题
向Na2CO3溶液中滴加盐酸,反应过程中能量变化如下图所示,下列说法正确的是
A.反应HCO3-(aq)+H+(aq)=CO2(g)+H2O(l) 为放热反应
B.CO32-(aq)+2H+(aq)=CO2(g)+H2O(l) ∆H=(∆H1+∆H2+∆H3)
C.∆H1>∆H2 ∆H2<∆H3
D.H2CO3(aq)=CO2(g)+H2O(l),若使用催化剂,则∆H3变小
查看答案和解析>>
科目:高中化学 来源:2017届天津市五区县高三上学期期末考试化学试卷(解析版) 题型:选择题
下列有关物质的性质与用途说法不正确的是
A.FeCl3易溶于水,可用作净水剂
B.硅是半导体材料,纯净的硅是光纤制品的基本原料
C.浓硫酸能干燥氯气,说明浓硫酸具有吸水性
D.氨易液化,液氨气化吸收大量的热,所以液氨常用作制冷剂
查看答案和解析>>
科目:高中化学 来源:2016-2017学年广东省惠州市高二上学期高二质量检测化学试卷(解析版) 题型:实验题
活性氧化锌是一种多功能性的新型材料.某小组以粗氧化锌(含铁、铜的氧化物)为原料模拟工业生产活性氧化锌,步骤如下:
已知各相关氢氧化物沉淀pH范围如下表所示:
Zn(OH)2 | Fe(OH)2 | Fe(OH)3 | Cu(OH)2 | |
开始沉淀pH | 5.4 | 7.0 | 2.3 | 4.7 |
完全沉淀pH | 8.0 | 9.0 | 4.1 | 6.7 |
步骤II中,在酸性溶液中加入KMnO4的作用是将Fe2+ 氧化成Fe3+,离子方程式为 ;
(2)用ZnO调节pH,以除去含铁杂质。检验沉淀是否完全的实验操作是 ;调节pH的适宜范围是 。
(3)步骤III中加入Zn粉的作用是① ,②进一步调节溶液PH值。
(4)用如下方法测定所得活性氧化锌的纯度(假设杂质不参与反应):
取1.000g活性氧化锌,用15.00mL 1.00mol/L硫酸溶液完全溶解,滴入几滴指示剂,再用0.50mol/L的标准氢氧化钠溶液滴定剩余硫酸,到达终点时消耗氢氧化钠溶液12.00mL,通过计算可以得到活性氧化锌的纯度,由表中Zn(OH)2PH变化可知,滴入的最理想的指示剂是 (填“酚酞”、“甲基橙”或“石蕊试剂”)。
查看答案和解析>>
科目:高中化学 来源:2016-2017黑龙江牡丹江第一高级中学高一上期末化学卷(解析版) 题型:选择题
在Na+的物质的量浓度为0.5mol•L-1的某澄清溶液中,还可能含有如下离子:K+、Mg2+、Ba2+、NO3-、CO32-、SO42-。取100mL该溶液进行如下实验(气体体积在标准状况下测定):
I.向该溶液中加入足量稀盐酸,在标准状况下放出0.56L气体(不考虑气体溶解);
II.向I中所得的滤液中滴加足量BaCl2溶液产生白色沉淀2.33g;
下列说法正确的是( )
A.一定不存在的离子是Mg2+、Ba2+,不能确定是否含有K+、NO3-
B.一定存在的离子是CO32-、SO42-,CO32-的物质的量浓度为0.25mol•L-1,SO42-的物质的量浓度为0.1mol•L-1
C.一定存在的离子是CO32-、SO42-、K+,其中K+浓度≥0.2mol•L-1
D.一定存在的离子是CO32-、SO42-、K+,其中K+浓度为0.2mol•L-1
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com