
ijԭ�Ͼ��ⶨ��Ҫ����A��B��C��D��E����ǰ������Ԫ�أ���ԭ��������������Ԫ��A��B��C��D��E��ԭ�ӽṹ����Ϣ���£�
Ԫ�� | Ԫ�����ʻ�ԭ�ӽṹ |
A | ���ڱ���ԭ�Ӱ뾶��С |
B | ԭ�Ӻ��������ֲ�ͬ��������ԭ�ӹ���Ҹ�����������ĵ�������ͬ |
C | �����p�������� |
D | λ�ڶ����ڣ���ԭ�ӵĺ���ɶԵ�������δ�ɶԵ�������3�� |
E | λ��ds����ԭ�ӵ�������������A����ͬ |
��ش��������⣨��A��B��C��D��E����Ӧ��Ԫ�ط�������)��
��1��B��C��D��һ��������С����Ϊ______________��
��2��E�Ķ������ӵĵ����Ų�ʽΪ______________��
��3��A2B2D4��һ���л����ᣬ��������������÷�����B���ӻ���ʽΪ____________��1 mol A2B2D4�����к��ЦҼ���ĿΪ____________��
��4���뻯����BD��Ϊ�ȵ�����������ӻ�ѧʽΪ__________����дһ��)��
��5��B2A6��C2A4�����о�����18�����ӣ����ǵķе����ϴ���Ҫԭ����__________________��
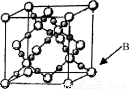
��6��BD2�ڸ��¸�ѹ�����γɾ���ľ�������ͼ��ʾ��һ���þ����к�________��Dԭ�ӡ�

| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ��2015-2016ѧ���ຣʡ��һ��ѧ��ѧ�Ծ��������棩 ���ͣ�ѡ����
�����£�ij��ɫ������Һ�У����и��������ܹ������������
A��H����Na����Cl����CO32�� B��Ba2����Na����SO42����Cl��
C��MnO4- ��K+ ��I- ��H+ D��Mg2+ ��Cl-��NO3- ��H+
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2016�콭��ʡ������ѧ�ڵ�һ���¿���ѧ�Ծ��������棩 ���ͣ�ѡ����
�����������������п����������Һ�ֱ����������Ȼ�����Һ��Ӧ�������ɵ����ᱵ������������Ϊ1��2��3����������������Һ�����ʵ���Ũ�ȱ�Ϊ
A��1��2��3 B��1��6��9 C��1��3��3 D��1��3��6
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2016������ʡ�����и����ڳ����Ի�ѧ�Ծ��������棩 ���ͣ�ѡ����
CO2��H2�Ļ������5 g,��150 ��ʱ���������������,�õ�����ȼ,����ͬ״�����ٽ���Ӧ�����û������ͨ�뵽������Na2O2��,���Na2O2�������ص�����Ϊ3.4 g,��ԭ���������CO2���������Ϊ
A��25% B��75% C��88% D��32%
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2016�콭��ʡ��У�����ϵ�һ��������ѧ�Ծ��������棩 ���ͣ������
��10�֣���ҵ�ϳɰ����Ʊ�����һ�������������������ͼ��ʾ��
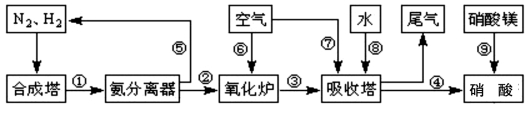
��1����ҵ����ʱ����ȡ������һ����ӦΪ��CO+H2O��g) CO2+H2
CO2+H2
T��ʱ����1L�ܱ������г���0.2mol CO��0.3molˮ��������Ӧ����ƽ�����ϵ��c��H2)��0.12mol/L��
�¶��´˷�Ӧ��ƽ�ⳣ��K��_____�������������
��2���ϳ����з�����ӦN2��g)+3H2��g) 2NH3��g)����H<0���±�Ϊ��ͬ�¶��¸÷�Ӧ��ƽ�ⳣ�����ɴ˿���֪������T1____300K���>������<����=������
2NH3��g)����H<0���±�Ϊ��ͬ�¶��¸÷�Ӧ��ƽ�ⳣ�����ɴ˿���֪������T1____300K���>������<����=������
T/�� | T1 | 300 | T2 |
K | 1.00��107 | 2.45��105 | 1.88��103 |
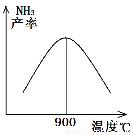
��3��N2��H2������������145��Ϳ�ʼ��Ӧ����ͬ�¶���NH3�IJ�����ͼ��ʾ���¶ȸ���900��ʱ��NH3�����½���ԭ���� ��
��4�����᳧��β��ֱ���ŷŽ���Ⱦ������Ŀǰ��ѧ��̽������ȼ�������еļ���Ƚ��������ﻹԭΪ������ˮ���䷴Ӧ����Ϊ��
CH4��g)+4NO2��g)��4NO��g)+CO2��g)+2H2O��g)�� ��H=��574kJ��mol��1
CH4��g)+4NO��g)��2N2��g)+CO2��g)+2H2O��g)�� ��H=��1160kJ��mol��1
�����ֱ�ӽ�NO2��ԭΪN2���Ȼ�ѧ����ʽΪ�� ��
��5�������ڴ�����ȼ�գ�����һ�ֵ��ʺ�ˮ����ѧ�����ô�ԭ������Ƴɰ���-����ȼ�ϵ�أ����ڼ���������ͨ�백�������ĵ缫��ӦʽΪ ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2016�콭��ʡ������ѧ�ڿ�ѧ���Ի�ѧ�Ծ��������棩 ���ͣ�ѡ����
�����й����ʵķ���������ȷ����
�ٻ���ʯ̿�ᡢ�������֡�ˮ������ˮ�� �ڻ����CaCl2���ռ�۱���ϩ��HD
�۵���ʣ������������������ᡢ���ᱵ ��ͬϵ�CH2O2��C2H4O2��C3H6O2��C4H8O2
��ͬ�������壺C60��C70�����ʯ��ʯī
A���٢ۢ� B���ۢ� C���ڢۢ� D���ڢ�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2016�����ʡƽ���и�����ѧ�ڵ�һ��ģ�⿼�Ի�ѧ�Ծ��������棩 ���ͣ�ѡ����
�����й�ʵ�����������ȷ����
A�����ձ�����ƿ��Һ�����ʼ���ʱ��û�е�ʯ����
B���ƾ���Ũ�����Ϲ�����170 �棬���Ƶ���ϡ
C����������ƽ��������ҩƷʱ��ҩƷ����������
D�����δ֪��Һ�еμ��Ȼ�����Һ�а�ɫ�������ɣ�֤��ԭ��Һ��һ���������������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2016��ɽ��ʡ������ѧ�ڿ�ѧ���Ի�ѧ�Ծ��������棩 ���ͣ�ѡ����
ҩ�ﱴŵ����������ˮ����Ͷ�������������һ�������·�Ӧ�Ƶã�

�����й�������ȷ����
A����ŵ�������������ֺ���������
B������FeCl3 ��Һ��������ˮ����Ͷ�����������
C������ˮ����Ͷ����������Ӿ�����NaHCO3 ��Һ��Ӧ
D����ŵ��������NaOH ��Һ���ȣ�������������ˮ�����ƺͶ�������������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2016�����ʡ������ѧ�ڵ�һ���ʼ컯ѧ�Ծ��������棩 ���ͣ������
��10�֣�������أ�K2FeO4����һ�����͡���Ч�������ɫˮ����������C12��O3��ClO2��KMnO4�����Ը�ǿ��������Ⱦ����ҵ�������Ƶø������ƣ�Ȼ���ڵ����£������������Һ�м���KOH�����ͣ�ʹ�������������
��1��ʪ���Ʊ��������ƣ�Na 2FeO4���ķ�Ӧ��ϵ��������:Fe��OH��3��ClO����OH-��FeO42����Cl����H2O��
��д������ƽʪ���Ʊ��������Ƶ����ӷ���ʽ�� ��
�ڵ����£��ڸ���������Һ�м���KOH�����Ϳ�����������أ�K2FeO4��������ܵ�ԭ���� ��
��2���ɷ��Ʊ��������Ƶ���Ҫ��ӦΪ��2FeSO4+6Na2O2��2Na 2FeO4+2 Na 2O+2 Na 2SO4+O2��
�÷�Ӧ�еĻ�ԭ���� ������������ ��ÿ����l mol Na 2FeO4ת�� mol���ӡ�
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com