
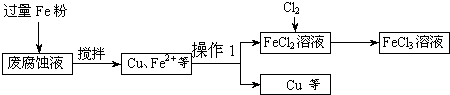
������12�֣�ӡˢ��·�ķϸ�ʴҺ���д���CuCl2��FeCl2��FeCl3�������ŷŽ����»�����Ⱦ����Դ���˷ѡ��ɴӸ÷�Һ�л���ͭ���������Ļ�����ȫ��ת��ΪFeCl3��Һ����Ϊ��ʴҺԭ��ѭ��ʹ�á����ij�ϸ�ʴҺ�к�CuCl2 1.5mol/L����FeCl2 3.0mol/L����FeCl3 1.0mol/L����HCl 3.0mol/L��ȡ�ϸ�ʴҺ200mL������������ʵ���ҽ���ʵ�飺
![]()

�ش��������⣺
��1������������õ�ͭ���к������ʣ����������Լ���
���ѧʽ����
��2�� ʵ���ҿ��ù���KClO3��ŨHCl��Ӧ�Ʊ�Cl2���˷�Ӧ��Cl2��������������ǻ�ԭ�����Ӧ�Ļ�ѧ����ʽΪ ��
![]() �� ��ͼ��ʵ�����Ʊ�Cl2��ͨ��FeCl2��Һ�л��FeCl3��Һ�IJ���װ�á�
�� ��ͼ��ʵ�����Ʊ�Cl2��ͨ��FeCl2��Һ�л��FeCl3��Һ�IJ���װ�á�
![]()


![]()
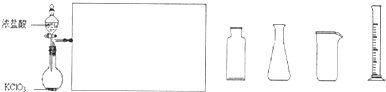
![]() ����ͼ��ѡ������������������װ�ü�ͼ�����ӱ�Ҫ�����ӡ��������ܡ���Ƥ�ܡ��̶�װ�ò��û�������������������װ�Լ���
����ͼ��ѡ������������������װ�ü�ͼ�����ӱ�Ҫ�����ӡ��������ܡ���Ƥ�ܡ��̶�װ�ò��û�������������������װ�Լ���
![]()


![]() �� ʵ���У���������������ٶȣ�ʹ���ܿ��ݳ�������ÿ��1~2�����Ա㱻FeCl2��Һ��ȫ���ա��������������ٶȵIJ����ǣ� ��
�� ʵ���У���������������ٶȣ�ʹ���ܿ��ݳ�������ÿ��1~2�����Ա㱻FeCl2��Һ��ȫ���ա��������������ٶȵIJ����ǣ� ��
![]() �� ���������̲��������ȡFe�۵�����Ӧ������ g����ȷ��0.1g������ͨ��Cl2�����ʵ��������� mol��������ƿ�е�KClO3������Ӧ������ g����ȷ��0.1g����
�� ���������̲��������ȡFe�۵�����Ӧ������ g����ȷ��0.1g������ͨ��Cl2�����ʵ��������� mol��������ƿ�е�KClO3������Ӧ������ g����ȷ��0.1g����
��1��HCl����H2SO4�� ��2�֣�
![]() ����д����Һ�����ֲ��۷֡������ֱ�ʾ���÷֡���CuCl2��CuSO4Ҳ�÷֣�
����д����Һ�����ֲ��۷֡������ֱ�ʾ���÷֡���CuCl2��CuSO4Ҳ�÷֣�
![]() ��2��KClO3��6HCl��Ũ����3Cl2����KCl +3 H2O��2�֣�
��2��KClO3��6HCl��Ũ����3Cl2����KCl +3 H2O��2�֣�
![]() ������ƽ���÷֡�©д��������1�֡���ע����Ũ�����۷֣�
������ƽ���÷֡�©д��������1�֡���ע����Ũ�����۷֣�
![]() ��3��
��3��
![]()


![]() ��3�֣�
��3�֣�
![]() �����������װ�ò��۷֣�ϴ��ƿ������ƿ���۷֣�������Ƥ�ܲ��۷֡��������ӿ�1�֣��������Լ�ÿ����1�֣�װ����ȫ��տ�1�֣�
�����������װ�ò��۷֣�ϴ��ƿ������ƿ���۷֣�������Ƥ�ܲ��۷֡��������ӿ�1�֣��������Լ�ÿ����1�֣�װ����ȫ��տ�1�֣�
![]() ��4������������Һ©���Ļ���������Һ����µ��ٶȣ�2�֣�
��4������������Һ©���Ļ���������Һ����µ��ٶȣ�2�֣�
![]() �����������Һ©���Ļ�����ʹŨ���Ỻ�����¡������������۷֡���
�����������Һ©���Ļ�����ʹŨ���Ỻ�����¡������������۷֡���
![]() ��5��39.2 0.75 30.6����30.7�� ����1�֣���3�֣�
��5��39.2 0.75 30.6����30.7�� ����1�֣���3�֣�
![]() �����㲻ȷ��С��λ������ȷ���÷֣�
�����㲻ȷ��С��λ������ȷ���÷֣�


 �Ķ��쳵ϵ�д�
�Ķ��쳵ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| ||
| ||
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ��Ķ�����
| ||
| ||
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2012��ɽ��ʡΫ���и�����ѧ����ĩ���Ի�ѧ�Ծ� ���ͣ�ʵ����
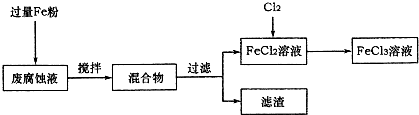
(16��)ӡˢ��·�ķϸ�ʴҺ���д���CuCl2��FeCl2��FeCl3�������ŷŽ����»�����Ⱦ����Դ���˷ѣ��ɴӸ÷�Һ�л���ͭ���������Ļ�����ȫ��ת��ΪFeCl3��Һ����Ϊ��ʴҺԭ��ѭ��ʹ�á�
(1)���ij�ϸ�ʴҺ�к�CuCl2 1.5 mol��L-1��FeCl23.O mol��L-1��FeCl3 1.0 mol��L-1��HCl3.0 mol��L-1��ȡ�ϸ�ʴҺ200mL������������ʵ���ҽ���ʵ�飺
�ش��������⣺
�ϸ�ʴҺ�м���������ۺ�����Ӧ�����ӷ���ʽΪ ��
�ڼ���ϸ�ʴҺ�к���Fe3+��ʵ������� ��
�����������У������ˡ��õ��IJ����������ձ����������� ��
���������õ���ͭ�����������Լ��� ��
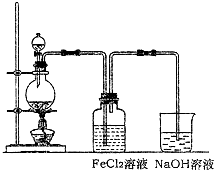
(2)ij��ѧ��ȤС��������ͼװ����ȡ������ͨ�뵽FeCl2��Һ�л��FeCl3��Һ��
��ʵ�鿪ʼǰ��ijͬѧ��ʵ��װ�ý����������Լ�飬������ ��
��Ũ������������̷�Ӧ�Ļ�ѧ����ʽΪ ��
�ձ���NaOH��Һ�������� ��
�۲ο�(1)�����ݣ����������̲��������ȡFe�۵�����Ӧ������ g��
��ͨ��Cl2�����ʵ���Ӧ������ mol.
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2011-2012ѧ������ʡ��ƽ�и�����ѧ����ĩ��ϰ��ѧ�Ծ� ���ͣ������
������12�֣�������M��һ���������ಡҩ����м��壬��AΪԭ�ϵĹ�ҵ�ϳ�·������ͼ��ʾ��

��֪��RONa+ R��X��ROR��+ NaX
�����������������գ�
��1��д����Ӧ���͡���Ӧ�� ��Ӧ��
��2��д���ṹ��ʽ��A C
��3��д�� ����λ�칹���������ˮ�����㶹�صĽṹ��ʽ
��
����λ�칹���������ˮ�����㶹�صĽṹ��ʽ
��
��4����C����D����һ����Ӧ���� ����Ӧ������ ��
��5��д����D����M�Ļ�ѧ��Ӧ����ʽ ��
��6��AҲ���Ʊ�������( )��ԭ�ϣ�д������A����ȫת��Ϊ�������ķ�����
)��ԭ�ϣ�д������A����ȫת��Ϊ�������ķ�����
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com