
| A. | IA族与 VIIA族元素间可形成共价化合物或离子化合物 | |
| B. | 最高第二周期元素从左到右,正价从+1递增到+7 | |
| C. | 同主族元素的简单阴离子还原性越强,非金属性越强 | |
| D. | 同周期金属元素的化合价越高,其原子失电子能力越强 |
分析 A.ⅠA族为H和碱金属,ⅦA族元素为非金属元素;
B.第二周期元素中,O、F没有正价;
C.同主族元素的简单阴离子还原性越强对应元素的非金属性越弱,难易规律;
D.同周期金属元素的化合价越高,越难失去电子.
解答 解:A.ⅠA族为H和碱金属,ⅦA族元素为非金属元素,H与卤族元素形成共价化合物,碱金属元素与卤族元素形成离子化合物,故A正确;
B.第二周期元素中,O、F没有正价,则第二周期元素从左到右,最高正价从+1递增到+5,故B错误;
C.同主族元素的简单阴离子还原性越强,非金属性越弱,故C错误;
D.同周期金属元素的化合价越高,越难失去电子,如第三周期中,Na比Al容易失去电子,故D错误;
故选A.
点评 本题考查元素周期表和元素周期律的应用,注意同周期、同主族元素的性质变化规律是解答本题的关键,注意利用实例分析问题,题目难度中等.


科目:高中化学 来源: 题型:填空题
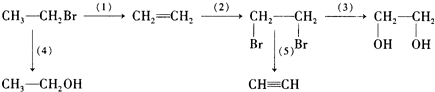
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| 序号 | X | Y | Z | W |  |
| A | NaOH | Na2CO3 | NaHCO3 | NaCl | |
| B | Cl2 | Ca(ClO)2 | HClO | HCl | |
| C | Si | SiO2 | Na2SiO3 | H2SiO3 | |
| D | FeCl3 | FeCl2 | Fe(OH)2 | Fe(OH)3 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | XYZW的原子半径依次减小 | |
| B. | W与X形成的化合物中只含离子键 | |
| C. | W的最高价氧化物对应的水化物一定为强酸 | |
| D. | 若W与Y的原子序数相差5,则二者形成化合物的化学式一定为Y2W3 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | ③ | B. | ④ | C. | ②⑤ | D. | ① |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
 .
.查看答案和解析>>
科目:高中化学 来源: 题型:解答题
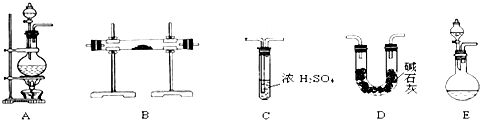
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com