
| A. | 酸与醇反应一定能生成酯,且酯化反应是可逆反应 | |
| B. | CO2通入饱和苯酚钠溶液,用分液法可以得到苯酚 | |
| C. | 有机物 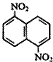 的n溴代物的同分异构体的数目与m溴代物的同分异构体的数目相等,则m、n一定满足的关系式m+n=6 的n溴代物的同分异构体的数目与m溴代物的同分异构体的数目相等,则m、n一定满足的关系式m+n=6 | |
| D. | 等物质的量的烃或烃的含氧衍生物A和B完全燃烧时,消耗氧气的量相等.则A和B的分子量相差可能为18n或44n(n为正整数) |
分析 A.乙醇与浓HBr反应生成溴乙烷和水;
B.CO2通入饱和苯酚钠溶液,反应生成苯酚,为强酸制取弱酸的反应;
C.苯环上有6种H,如1氯代物与5氯代物的同分异构体的数目相等;
D.等物质的量的有机物消耗相等的物质的量的氧气有以下几种情况:①分子间相差n个CO2;②分子间相差n个H2O;③分子间1个C相当于4个H,即少n个C要多4n个H;④互为同分异构体.
解答 解:A.乙醇与浓HBr反应生成溴乙烷和水,不生成酯,而醇与有机酸反应生成酯和水,为可逆反应,故A错误;
B.CO2通入饱和苯酚钠溶液,反应生成苯酚,为强酸制取弱酸的反应,苯酚为不溶于水的液体,则用分液法可以得到苯酚,故B正确;
C.苯环上有6种H,如1氯代物与5氯代物的同分异构体的数目相等,则n溴代物的同分异构体的数目与m溴代物的同分异构体的数目相等,则m、n一定满足的关系式m+n=6,故C正确;
D.当A与B的分子组成只相差n个“CO2”时,消耗氧气的量相等,即A和B的相对分子质量的差值为44n,当A与B分子组成只相差n个“H2O”时,消耗氧气的量相等,即A和B的相对分子质量的差值为18n,由于分子间1个C相当于4个H,即少n个C要多4n个H时,消耗氧气的量相等,A和B的相对分子质量的差值12n-4n=8n;当A与B互为同分异构体时,分子式相同,消耗氧气的量相等,则A和B的相对分子质量的差值为0,故D正确;
故选A.
点评 本题考查有机物的结构与性质,为高频考点,把握官能团与性质的关系、反应中官能团的变化为解答的关键,侧重分析与应用能力的考查,注意选项D为解答的难点,题目难度不大.


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:选择题

| A. | 实验室中灼烧操作通常在坩埚中进行 | |
| B. | 若X为烧碱,则Z为氨气,沉淀a为红棕色,可作颜料 | |
| C. | 若X为盐酸,则Z为CO2,溶液丙只含NaCl和Na2CO3 | |
| D. | 上述过程中所发生的反应有分解反应、复分解反应、氧化还原反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 向0.1mol/LpH=2的HF溶液加水稀释,$\frac{c({H}^{+})}{c(HF)}$增大 | |
| B. | 向0.2 mol/L NaHCO3溶液中加入等体积0.1 mol/L NaOH溶液c(HCO3-)>c(CO32-)>c(OH-)>c(H+) | |
| C. | 向0.1mol/L NaHSO3溶液中通入NH3至中性(溶液体积视为不变),则 c(NH4+)+c(H2SO3)═c(SO32-) | |
| D. | 现有常温下水电离出的c(H+)均为1×10-11 mol/L且体积相同的三种溶液:①HCl溶液②CH3COOH溶液③NaOH溶液,分别与足量铝粉反应,生成氢气的量③最少 |
查看答案和解析>>
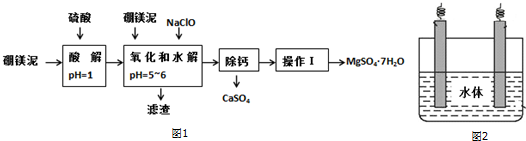
科目:高中化学 来源: 题型:解答题
| 氢氧化物 | 开始沉淀时的pH | 完全沉淀时的pH |
| Mg(OH)2 | 9.3 | 10.8 |
| Fe(OH)2 | 7.6 | 9.6 |
| Fe(OH)3 | 2.7 | 3.7 |
| Al(OH)3 | 3.7 | 4.7 |
| 温度(℃) | 40 | 50 | 60 | 70 |
| MgSO4 | 30.9 | 33.4 | 35.6 | 36.9 |
| CaSO4 | 0.210 | 0.207 | 0.201 | 0.193 |
查看答案和解析>>
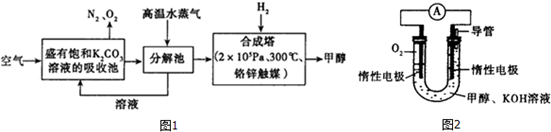
科目:高中化学 来源: 题型:解答题
| 实验组 | 温度/℃ | 起始量/mol | 平衡量/mol | 达到平衡所需要的时间/min | ||
| CO | H2O | H2 | CO | |||
| 1 | 650 | 4 | 2 | 1.6 | 2.4 | 6 |
| 2 | 900 | 2 | 1 | 0.4 | 1.6 | 3 |
| 3 | 900 | a | b | c | d | t |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | ①②⑥ | B. | ③④⑥ | C. | ②③⑤ | D. | ①④⑤ |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com