
X为短周期元素组成的单质,有下列转化关系:X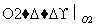 XnOm
XnOm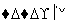 盐,下列相关叙述正确的是( )
盐,下列相关叙述正确的是( )
A.①②一定都是氧化还原反应
B.①②都不是氧化还原反应
C.XnOm一定是酸性氧化物
D.XnOm是金属氧化物或非金属氧化物
 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:
氧化镁在医药、建筑等行业应用广泛。硫酸镁还原热解制备高纯氧化镁是一种新的探索。以菱镁矿(主要成分为MgCO3,含少量FeCO3)为原料制备高纯氧化镁的实验流程如下:
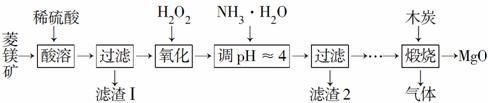
(1)MgCO3与稀硫酸反应的离子方程式为___________________ _____________________________________________________________________________________________________________________________。
(2)加入H2O2氧化时,发生反应的化学方程式为________________________________________________________________________________________________________________________________________________。
(3)滤渣2的成分是____________________________________________ _________________________(填化学式)。
(4)煅烧过程存在以下反应:
2MgSO4+C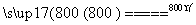 2MgO+2SO2↑+CO2↑
2MgO+2SO2↑+CO2↑
MgSO4+C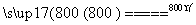 MgO+SO2↑+CO↑
MgO+SO2↑+CO↑
MgSO4+3C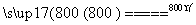 MgO+S↑+3CO↑
MgO+S↑+3CO↑
利用如图装置对煅烧产生的气体进行分步吸收或收集。
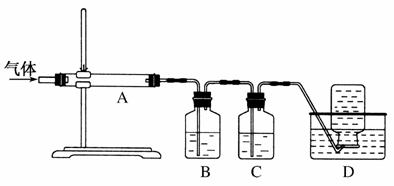
①D中收集的气体是________(填化学式)。
②B中盛放的溶液可以是________(填字母)。
a.NaOH溶液 b.Na2CO3溶液
c.稀硝酸 d.KMnO4溶液
③A中得到的淡黄色固体能与热的NaOH溶液反应,产物中元素的最高价态为+4,写出该反应的离子方程式:
___________________________________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
(1) 鉴别NaCl和Na2CO3溶液的试剂是 ,离子方程式为 。
(2) 除去混入Na2CO3溶液中少量NaHCO3杂质的试剂是 ,离子方程式为
。
(3) 除去Fe粉中少量Al粉杂质的试剂是 ,离子方程式为 。
查看答案和解析>>
科目:高中化学 来源: 题型:
A-D是中学化学实验中常见的几种温度计装置示意图,正确的是:
A.酒精和浓硫酸混合加热制乙烯 B.石油分馏实验
C.苯跟溴的取代反应 D.电石跟水反应制乙炔
| A | B | C | D |
|
|
|
|
|
查看答案和解析>>
科目:高中化学 来源: 题型:
为探究苯与溴的取代反应,甲用右图装置I进行如下实验:
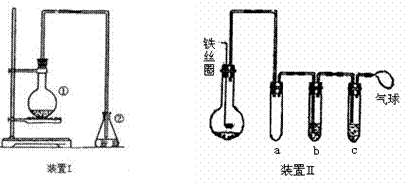 |
将一定量的苯和溴放在烧瓶中,同时加入少量铁屑做催化剂,3-5分钟后发现滴有AgNO3的锥形瓶中有浅黄色沉淀生成,即证明苯与溴发生了取代反应。
(1)装置I中①的化学方程式为_________________________________。
(2)①中长导管的作用是____________________________________。
(3)要想得到纯净的产物,可用稀NaOH溶液,蒸馏水洗涤。洗涤分离粗产品应使用的最主要仪器是____________。检验产物已纯净的方法是 ____________________。
(4)乙同学设计右图所示装置Ⅱ,并用下列某些试剂完成该实验。可选用的试剂是:苯、液溴;浓硫酸;氢氧化钠溶液;硝酸银溶液;四氯化碳。
a的作用是_____________________________。 能证明苯和液溴发生的是取代反应,而不是加成反应,那试管b中应加入 ,试管c中应加入 。
(5)比较两套装置,装置Ⅱ的两个优点是①___________________②____________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
X、Y、Z、W有如图所示的转化关系,则X、Y可能是( )
①C、CO ②AlCl3、Al(OH)3 ③N2、NO ④S、SO2 ⑤NaOH、Na2CO3
A.①②⑤ B.②③⑤
C.③④ D.①②④
查看答案和解析>>
科目:高中化学 来源: 题型:
铅蓄电池是典型的可充电电池,它的正负极极板是惰性材料,
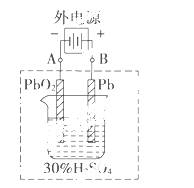
请回答下列问题(不考虑氢、氧的氧化还原):
(1)电解液中H2SO4的浓度将变______________________;
当外电路通过1 mol电子时,理论上负极板的质量增加__________g。
(2)在完全放电耗尽PbO2和Pb时,若按上图连接,电解一段时间后,则在A电极上生成________,B电极上生成____________,此时铅蓄电池的正负极的极性将________。
查看答案和解析>>
科目:高中化学 来源: 题型:
糕点包装中常见的脱氧剂组成为还原性铁粉、氯化钠、炭粉等,其脱氧原理与钢铁的吸氧腐蚀相同。下列分析正确的是
A.脱氧过程是吸热反应 ,可降低温度,延长糕点保质期
,可降低温度,延长糕点保质期
B.脱氧过程中铁作原电池正极,电极反应为: Fe-3e→Fe3+
Fe-3e→Fe3+
C.脱氧过程中碳做原电池负极,电极反应为:2H2O+O2+4e→4OH-
D.含有1.12g铁粉的脱氧剂,理论上最多能吸收氧气336mL(标准状况)
查看答案和解析>>
科目:高中化学 来源: 题型:
下列各组热化学方程式中,化学反应的ΔH前者大于后者的是( )
①C(s)+O2(g)===CO2(g) ΔH1
C(s)+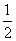 O2(g)===CO(g) ΔH2
O2(g)===CO(g) ΔH2
②S(s)+O2(g)===SO2(g) ΔH3
S(g)+O2(g)===SO2(g) ΔH4
③H2(g)+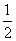 O2(g)===H2O(l) ΔH5
O2(g)===H2O(l) ΔH5
2H2(g)+O2(g)===2H2O(l) ΔH6
④CaCO3(s)===CaO(s)+CO2(g) ΔH7
CaO(s)+H2O(l)===Ca(OH2)(s) ΔH8
A.① B.④
C.②③④ D.①②③
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com