
【题目】偏二甲肼与N2O4是常用的火箭推进剂,二者发生如下化学反应:(CH3)2NNH2(l)+2N2O4(l)=2CO2(g)+3N2(g)+4H2O(g)(Ⅰ)![]()
(1)反应(Ⅰ)中氧化剂是___。
(2)火箭残骸中常现红棕色气体,原因为:N2O4(g)![]() 2NO2(g) ΔH(Ⅱ)
2NO2(g) ΔH(Ⅱ)
当温度升高时,气体颜色变深,则反应(Ⅱ)中ΔH___0(填“>”或“<”),保持温度和体积不变向上述平衡体系中再充入一定量的N2O4,混合气体的颜色__(填“变深”或“变浅”)。
【答案】N2O4 > 变深
【解析】
(1)根据化合价的变化分析,化合价降低的做氧化剂被还原;
(2)当温度升高时,气体颜色变深,说明平衡正向进行,正反应为吸热反应,ΔH >0;保持温度和体积不变向上述平衡体系中再充入一定量的N2O4,相当于成比例增大反应物,据此回答。
(1)反应(Ⅰ)中,N2O4(l)中N元素化合价从+4得到电子变成0价,得电子发生还原反应,N2O4(l)是氧化剂;
答案为N2O4。
(2)N2O4(g)2NO2(g) (Ⅱ),当温度升高时,气体颜色变深,说明平衡正向移动,正反应为吸热反应,则ΔH >0;保持温度和体积不变向上述平衡体系中再充入一定量的N2O4,相当于成比例增大反应物,即增大压强平衡向气体体积减小的方向移动即逆反应方向,虽然NO2的体积分数减小,但二氧化氮的浓度仍然增大,则混合气体的颜色变深;
答案为>;变深。


科目:高中化学 来源: 题型:
【题目】在150℃时使NH4HCO3分解,将所产生的气体依次通过Na2O2和浓H2SO4,则Na2O2增重ag,浓H2SO4增重bg;若将上述气体先通过浓H2SO4,则使酸液增重dg,再通过Na2O2,则使之增重cg。设气体皆完全被吸收,a、b、c、d质量由大到小的排列顺序正确的是
A.d a c bB.b c a dC.a c b dD.d c b a
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】根据下面的反应路线及所给信息填空。
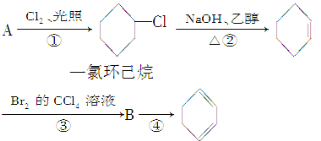
(1)A的结构简式是______,名称是______。
(2)①的反应类型是______,②的反应类型是______。
(3)反应④的化学方程式是__________________________________
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某工厂用NaCl为原料制备高氯酸,实验按流程如下所示:
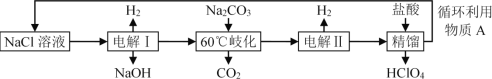
下列说法不正确的是( )
A.电解Ⅰ分别用不锈钢网和石墨作电极,石墨电极上有黄绿色气体生成
B.“60℃歧化”的反应为:3Cl2+3CO32-=5Cl+ClO3-+3CO2
C.电解Ⅱ中阳极反应式为:ClO3-+2OH-2e=ClO4-+H2O
D.循环利用物质A的成分是NaCl、NaClO4
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列各组物质中,属于同分异构体的是( )
A.![]() 和
和![]()
B.H2N-CH2-COOH 和 H3C-CH2-NO2
C.CH3-CH2-CH2-COOH 和 H3C-CH2-CH2-CH2-COOH
D.H3C-CH2-O-CH2-CH3 和![]()
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】实验室利用呋喃甲醛为原料制备呋喃甲醇与呋喃甲酸。
Ⅰ、制备原理:
2![]() +NaOH
+NaOH![]() +
+![]()
![]() +HCl
+HCl![]() +NaCl
+NaCl
Ⅱ、实验步骤
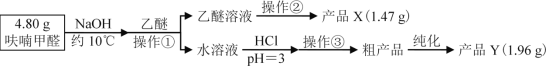
Ⅲ、相关信息
呋喃甲醛 | 呋喃甲醇 | 呋喃甲酸 | 乙醚 | |
熔点/℃ | -36.5 | -29 | 133 | -116.3 |
沸点/℃ | 161.7 | 170 | 231 | 34.5 |
水溶性 | 微溶 | 微溶 | 可溶 | 不溶 |
相对分子质量 | 96 | 98 | 112 | 74 |
Ⅳ、实验装置
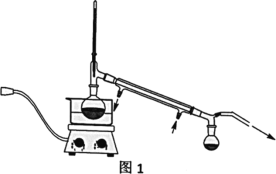
V、分析与思考,回答下列问题:
(1)操作①名称___;产品Y为___。
(2)操作②的装置如图1所示,收集产品X时温度计的读数应控制在90℃左右,其原因是___。
(3)操作①所得水溶液,加盐酸须控制pH为2~3,pH<3的理由是___;控制溶液pH时,应选择的指示剂是__。
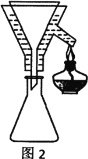
(4)粗产品Y纯化过程用图2装置进行热过滤,具体操作:向铜漏斗中加热水→___→拆装置。涉及操作顺序最合理的选项。
A.加热漏斗支管→放入短颈漏斗→放入滤纸→放接液烧杯→倒入热的待滤液
B.放入短颈漏斗→放接液烧杯→加热漏斗支管→放入滤纸→倒入热的待滤液
C.放入短颈漏斗→放入滤纸→加热漏斗支管→放接液烧杯→倒入热的待滤液
D.放入短颈漏斗→放入滤纸→放接液烧杯→倒入热的待滤液→加热漏斗支管
(5)共消耗30mL萃取剂乙醚,从萃取效果角度思考,下列4种萃取方式最合理的是__。
A.30mL、0mL、0mL B.10mL、10mL、10mL
C.15mL、10mL、5 mL D.5mL、10mL、15mL
(6)计算产品Y的产率ω(Y)=___。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】KMnO4溶液常用做氧化还原反应滴定的标准液,由于KMnO4的强氧化性,它的溶液易被空气中或水中某些少量还原性物质还原,生成难溶性物质MnO(OH)2,因此精确配制KMnO4标准溶液的操作是:
(1)称取稍多于所需量的KMnO4固体溶于水,将溶液加热并保持微沸lh;
(2)用微孔玻璃漏斗过滤除去难溶的MnO(OH)2;
(3)过滤得到的KMnO4溶液贮存于棕色试剂瓶放在暗处:
(4)利用氧化还原滴定方法,在70℃-80℃条件下用基准试剂(纯度高、稳定性好的物质)溶液测定其浓度。
回答下列问题:
(1)为什么要称取稍多于所需的KMnO4固体?__
(2)为什么不用普通滤纸过滤器过滤?___
(3)如何保证在70℃~80℃条件下进行滴定操作:___
(4)下列物质中,可以用于测定KMnO4溶液浓度的基准试剂是__
A.H2C2O4·2H2O B.FeSO4·7H2O C.浓盐酸 D.Na2SO3
(5)若准确称取Wg草酸晶体(H2C2O4·2H2O)溶于水配成500mL水溶液,取25.00mL置于锥形瓶中,用高锰酸钾溶液滴定至终点,消耗高锰酸钾溶液VmL。6H++2MnO4-+5H2C2O4·2H2O=2Mn2++10CO2↑+18H2O,问:
①滴定时,高锰酸钾溶液应装在__;
②滴定终点标志是___;
③KMnO4溶液的物质的量浓度为___;
④若滴定前平视,滴定后俯视,则测得的浓度值将__(填“偏高”或偏低)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】工业废弃物的资源化回收再利用,可以更大限度的发挥原材料的价值。下图是工业生产纳米磁性氧化铁的流程:

下列说法不正确的是
A. 用Na2CO3溶液浸泡是为了除去废铁屑表面的铁锈
B. 若生产中不通入N2,暴露在空气中生产,将不能得到高纯度产品
C. 加适量的H2O2是为了将部分Fe2+氧化为Fe3+ ,涉及反应:H2O2+2Fe2++2H+=2Fe3++2H2O
D. 溶液A中Fe2+和Fe3+的浓度比为1:2
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】研究非元素及其化合物的性质具有重要意义。含硫物质燃烧会产生大量烟气,主要成分是SO2、CO2、N2、O2 。某研究性学习小组在实验室利用下列装置制备模拟烟气,并测定烟气中SO2的体积分数。
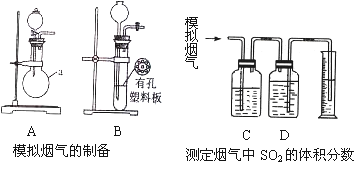
(一)模拟烟气的制备
(1)用A装置制SO2,化学反应方程式为___________________________。
(2)用B装置制CO2,使用该装置优点的是___________________________。
(3)将制得的气体与空气充分混合,获得模拟烟气用于后续实验。
(二)测定烟气中SO2的体积分数
(4)将部分模拟烟气缓慢通过C、D装置,其中C、D中盛有的药品分别是______、__________。(填序号)
①KMnO4溶液 ②饱和NaHSO3溶液 ③饱和Na2CO3溶液 ④饱和NaHCO3溶液
(5)若模拟烟气的流速为amL/min,若t1分钟后,测得量筒内液体体积为VmL,则SO2的体积分数____________________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com