
���� ��1���ٸ�������һ�����ʵ���Ũ�ȵ���Һ�IJ����ǣ����㡢�������ܽ⡢��Һ��ϴ�ӡ����ݡ�ҡ����ѡ��ʹ�õ�������
�ڸ��ݲ���������;��������
�۸���c=$\frac{n}{V}$��ͨ���жϲ������������ʵ����ʵ���n����Һ���V��Ӱ����������
��2�������Ը��������Һ��FeSO4��Һ����������Fe2+��MnO4-֮���������ԭ��Ӧ��Ӧ���������������������ӷ���ʽ��
�ڸ��ݷ�Ӧ��֪������������KMnO4��Һ���ⶨFeSO4��Һ��Fe2+�����ʵ���Ũ�ȵļ����ϵʽΪ��C��Fe2+��•V��Fe2+��=5C��MnO4-��•V��MnO4-�����ݴ˷���
��� �⣺��1���ٸ�������һ�����ʵ���Ũ�ȵ���Һ�IJ����Ǽ��㡢�������ܽ⡢��Һ��ϴ�ӡ����ݡ�ҡ�ȿ�֪��Ҫ�������У���ƽ��ҩ�ס��ձ�������������ͷ�ιܺ�250 mL ������ƿ��
�ʴ�Ϊ��250 mL ������ƿ��
�����ܽ������ع���ʱ���������������ǽ��裻����Һʱ����������������������
�ʴ�Ϊ�������������
��A����ˮ����ʱ���ӿ̶��ߣ��ᵼ����Һ���ƫС����Ũ��ƫ�ߣ���A��ѡ��
B��ֻҪ�����ʱ��Һ����̶������м��ɣ�����ˮ�����Ⱦ��еĻ��Ǻ�������ģ���Ũ����Ӱ�죬��B��ѡ��
C���ߵ�ҡ�Ⱥ��ְ�Һ����ڿ̶����������ģ��ּ�ˮ���ϻᵼ����Һ�����ƫ����Ũ��ƫС����Cѡ��
��ѡC��
��2�����ڷ�Ӧ�У�Fe2+����ԭ����������Ϊ+3�ۣ�������Fe3+��1molFe2+ʧ1mol���ӣ�MnO4-������������Ԫ�ر���ԭΪ+2�ۣ�������Mn2+��1molMnO4-��5mol���ӣ����ݵ�ʧ�������������ƽ�ɵã�5Fe2++MnO4-+8H+�TMn2++5Fe3++4H2O��
�ʴ�Ϊ��5Fe2++MnO4-+8H+�TMn2++5Fe3++4H2O��
�ڸ��ݷ�Ӧ��֪��������0.10000mol/L������KMnO4��Һ���ⶨFeSO4��Һ��Fe2+�����ʵ���Ũ�ȵļ����ϵʽΪ��C��Fe2+��•V��Fe2+��=5C��MnO4-��•V��MnO4-������֪Ҫ�����C��Fe2+����ֻ��֪����ȡ��FeSO4��Һ������Ͳ�����ĵ���KMnO4��Һ��������ɴ���ʽ�Ӽ����C��Fe2+����
�ʴ�Ϊ�����ĵ���KMnO4��Һ�������
���� ���⿼����һ�����ʵ���Ũ����Һ�����ƺ�������ԭ�ζ�������ʵ���ԭ���ǽ���Ĺؼ����ۺ��Խ�ǿ��ע��ʵ��Ļ�������������ע�����


 ͬ��ѧ��һ�ζ���ϵ�д�
ͬ��ѧ��һ�ζ���ϵ�д� �����ܾ�ϵ�д�
�����ܾ�ϵ�д� ���ƿ�����ϵ�д�
���ƿ�����ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
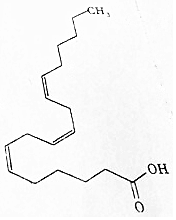 ��-������������������Ҫ������֬���ᣬ������ǿ�����������������������������˯�ߵ����ã���ṹ��ʽ��ͼ��ʾ���������˵���в���ȷ���ǣ�������
��-������������������Ҫ������֬���ᣬ������ǿ�����������������������������˯�ߵ����ã���ṹ��ʽ��ͼ��ʾ���������˵���в���ȷ���ǣ�������| A�� | ��-������ķ���ʽΪC18H30O2 | |
| B�� | ��-��������ʹ���Ը��������Һ��ɫ | |
| C�� | ��-��������һ���������ܷ���������Ӧ��ȡ����Ӧ | |
| D�� | 1mol��-�������������4molBr2�����ӳɷ�Ӧ |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | SO2��g��+NaOH��aq���TNaHSO3��aq����H=-��2a-b��kJ/mol | |
| B�� | SO2��g��+NaOH��aq���TNaHSO3��aq����H=-��4b-a��kJ/mol | |
| C�� | SO2��g��+NaOH��aq���TNaHSO3��aq����H=-��a-4b��kJ/mol | |
| D�� | SO2��g��+NaOH��aq���TNaHSO3��aq����H=-��4a-b��kJ/mol |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ʵ����
| ʵ���� | T/�� | ����ʯ��� | HNO3Ũ��/mol•L-1 |
| �� | ���� | ϸ���� | 2.00 |
| �� | ���� | ϸ���� | 1.00 |
| �� | 35�� | �ֿ��� | 2.00 |
| �� | 35�� | ϸ���� | 2.00 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
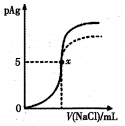 ��֪��pAg=-lg[c��Ag+��]��Ksp��AgCl��=1��l0-10��Ksp��AgI��=l��l0-17����ͼ����l0mLAgNO3��Һ�м���0��lmol/LNaCI��Һʱ����Һ��pAg���ż���NaCl��Һ������仯��ͼ��ʵ�ߣ�������ͼ���������н�����ȷ���ǣ�������
��֪��pAg=-lg[c��Ag+��]��Ksp��AgCl��=1��l0-10��Ksp��AgI��=l��l0-17����ͼ����l0mLAgNO3��Һ�м���0��lmol/LNaCI��Һʱ����Һ��pAg���ż���NaCl��Һ������仯��ͼ��ʵ�ߣ�������ͼ���������н�����ȷ���ǣ�������| A�� | ԭAgNO3��Һ�����ʵ���Ũ��Ϊ0��l mol/L | |
| B�� | ͼ��x���ʾ��Һ��c��Ag+��=c��Cl-�� | |
| C�� | ͼ��x�������Ϊ��10��5�� | |
| D�� | ��NaCl��Һ����0.1 mol/L��MaCl��Һ����ͼ�����յ���Ϊ���߲��� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ��Ӧ��MnO2�������� | |
| B�� | ���������뻹ԭ�������ʵ���֮��Ϊ1��3 | |
| C�� | KClO3�ڷ�Ӧ��ʧȥ���� | |
| D�� | ��Ӧ��ÿ����l mol K2MnO4���������õ�2 mol���� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| ����� | �Լ� | ���뷽�� | |
| A | �������ӣ� | ��ˮ | ���� |
| B | ���飨��ϩ�� | ���Ը��������Һ | ϴ�� |
| C | �������������ᣩ | ����Na2CO3��Һ | ��Һ |
| D | �屽���嵥�ʣ� | �� | ��ȡ |
| A�� | A | B�� | B | C�� | C | D�� | D |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
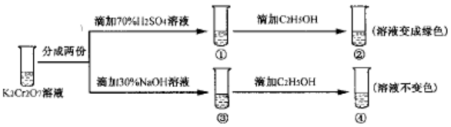
| A�� | ������Һ��ƣ�������Һ��ɫ���� | |
| B�� | �������淴Ӧ��ƽ�ⳣ�����٣��� | |
| C�� | K2Cr2O7��Һ�������������������¸�ǿ | |
| D�� | ������м���70%H2SO4��Һ����������Һ��Ϊ��ɫ |
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com