
设NA为阿伏加德罗常数的值,下列有关叙述正确的是
A.0.1mol NH3溶于足量水中(不考虑氨气挥发),溶液中N原子的数目为0.1NA
B.标准状况下,22.4LNO与CO2的混合气体中含有O原子数为3NA
C.0.1molN2与足量的H2反应,转移的电子数是0.6NA
D.58.5 g的NaCl固体中含有NA个氯化钠分子
 口算题天天练系列答案
口算题天天练系列答案科目:高中化学 来源: 题型:
只用一种试剂鉴别澄清石灰水、盐酸和蒸馏水三瓶失去标签的无色液体,提供的试剂:①碳酸钠溶液,②紫色石蕊溶液,③无色酚酞溶液,可以将它们鉴别出来的试剂是( )
A.只有① B.只有②
C.①或② D.①或③
查看答案和解析>>
科目:高中化学 来源: 题型:
实验室需用240mL 1mol/L的氢氧化钠溶液。填空并请回答下列问题:
(1) 配制所需体积的 1mol/L的氢氧化钠溶液
| 应称取氢氧化钠固体的质量/g | 应选用容量瓶的规格/mL | 除烧杯、托盘天平、容量瓶、量筒外还需的其它仪器 |
(2)配制时,其正确的操作顺序是(字母表示,每个字母只能用一次) ;
A.用30mL水洗涤烧杯2—3次,洗涤液均注入容量瓶,振荡
B.用托盘天平准确称取所需的氢氧化钠固体,倒入烧杯中,再加入少量水(约30mL),用玻璃棒慢慢搅动,使其充分溶解
C.将已冷却的溶液沿玻璃棒注入一定规格的容量瓶中
D.将容量瓶盖紧,振荡,摇匀
E.改用胶头滴管加水,使溶液凹面恰好与刻度相切
F.继续往容量瓶内小心加水,直到液面接近刻度1—2cm处
(3)操作A中,将洗涤液都移入容量瓶,其目的是 ,溶液注入容量瓶前需恢复到室温,这是因为
;
(4)若出现如下情况,对所配溶液浓度将有何影响(填“偏高”、“偏低”或“无影响”)?
若没有进行A操作 ;若加蒸馏水时不慎超过了刻度 ;若定容时俯视刻度线___________________。
(5)若实验过程中出现如下情况如何处理?
加蒸馏水时不慎超过了刻度 ;
向容量瓶中转移溶液时(实验步骤②)不慎有液滴掉在容量瓶外面
。
查看答案和解析>>
科目:高中化学 来源: 题型:
某工业残渣主要成分为Fe2O3。(含有少量FeO、Cu、Mg等杂质)某课外兴趣小组利用该残渣制取Fe2O3粉末的实验流程如下:(说明:流程中向黄色溶液中加入MgO的目的是调节溶液的酸碱性,使Fe3+ 生成沉淀而Mg2+不沉淀。)
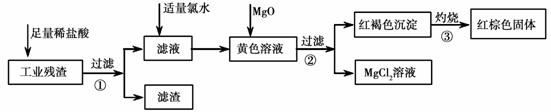
请回答下列问题:
⑴加入足量稀盐酸后,发生化学反应的类型有_____________(填写代号)。
A.置换反应 B.化合反应 C.分解反应 D.复分解反应 E.氧化还原反应
⑵加入适量氯水的作用是 ;
⑶写出灼烧红褐色沉淀时发生反应的化学方程式 。实验室灼烧红褐色沉淀可选用的装置是__________(填序号)。
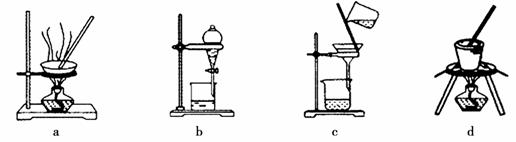
⑷若向黄色溶液中加入过滤①后的滤渣发生反应的离子方程式为 。
⑸用铝粉和Fe2O3做铝热反应实验,需要的试剂还有 。
a.KCl b. KClO3 c. MnO2 d. Mg
取少量铝热反应所得到的固体混合物,将其溶于足量稀H2SO4,滴加KSCN溶液无明显现象, (填“能”或“不能”)说明固体混合物中无Fe2O3,理由是
(用离子方程式说明)。
查看答案和解析>>
科目:高中化学 来源: 题型:
工业上用铝土矿(主要成分为Al2O3,Fe2O3等)提取Al2O3作冶炼铝的原料,由熔盐电解法获得的粗铝中含一定量的金属钠和氢气,这些杂质可采用吹气精炼法除去,产生的尾气经处理后可用于钢材镀铝。工艺流程如下图所示:
(已知:NaCl熔点为801℃;AlCl3在181℃升华)
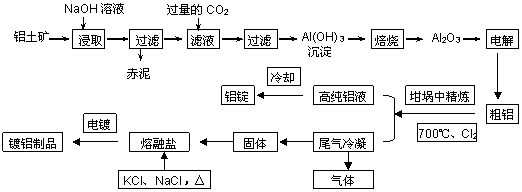
(1)赤泥中的主要成分是 (化学式);向滤液中通入过量CO2所发生反应的离子方程式为 。
(2)精炼前,需清除坩埚表面的氧化铁和石英砂,防止精炼时它们分别与铝发生置换反应产生新的杂质,则铝和氧化铁反应的化学方程式为 。
(3)将Cl2连续通入坩埚中的粗铝熔体,杂质随气泡上浮而除去。气泡的主要成分除Cl2外还含有______。固态杂质粘附于气泡上,在熔体表面形成浮渣,浮渣中肯定存在________。
(4)镀铝电解池中,金属铝为阳极,熔融盐电镀液中铝元素主要以AlCl4-形式存在,则阳极的电极反应式为_____________。
(5)钢材镀铝后,抗腐蚀性能会大大增强,其原因是_____________。
查看答案和解析>>
科目:高中化学 来源: 题型:
家用炒菜铁锅用水清洗放置后,出现红棕色的锈斑,在此变化过程中不发生的化学反应是
A.4Fe(OH)2+2H2O+O2=4Fe(OH)3 B.2Fe+2H2O+O2=2Fe(OH)2
C.2H2O+O2+4e-=4OH- D.Fe-3e-=Fe3+
查看答案和解析>>
科目:高中化学 来源: 题型:
某二元弱酸(简写为H2A)溶液,按下式发生一级或二级电离:
H2A 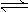 H++HA-,HA-
H++HA-,HA- 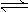 H++A2-
H++A2-
已知相同浓度时的电离度α(H2A)>α(HA-),设有下列四种溶液:
A、0.01mol/L的H2A溶液
B、0.01mol/L的NaHA溶液
C、0.02mol/L的HCl与0.04mol/L的NaHA溶液等体积混合
D、0.02mol/L的NaOH与0.02mol/L的NaHA溶液等体积混合
据此,填写下列空白(填代号):
(1)c(H+)最大的是 ,最小的是 ;
(2)c(H2A)最大的是 ,最小的是 ;
(3)c(A2-)最大的是 ,最小的是 。
查看答案和解析>>
科目:高中化学 来源: 题型:
(1)FeCl3的水溶液呈 (“酸”、“中”、“碱”)性,常温时的pH 7(填“>”、“=”、“<”),原因是(用离子方程式表示): 。
(2)实验室在配制 FeCl3的溶液时,常将FeCl3固体先溶于 中,然后再用蒸馏水稀释到所需的浓度。
(3)把FeCl3溶液蒸干,灼烧,最后得到的主要产物是 。
(4)普通泡沫灭火器内的玻璃筒里盛硫酸铝溶液,铁筒中盛碳酸氢钠溶液,其化学反应的原理是(用离子方程式解释) 。碳酸氢钠溶液中的电荷守恒式为 ,溶液中离子浓度由大到小的顺序为 。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com