
喹硫平可用于精神疾病的治疗,其结构为:
( )2·
)2· ,它的合成路线如下:
,它的合成路线如下:

已知:(Ⅰ)反应①为取代反应;(Ⅱ)A的系统命名为1,4-二溴―2―丁烯。
请回答下列问题:
(1)反应①的产物
 中除硫醚键(-S-)外,还含有的官能团名称
中除硫醚键(-S-)外,还含有的官能团名称
为 ▲ , ▲ 。
(2)反应③的类型是 ▲ 反应,反应⑤的目的是 ▲ 。
(3)写出反应④的化学方程式 ▲ 。
(4)物质B的同分异构体有多种,其中既含有羟基,又含有醛基的同分异构体有 ▲ 种。
(5)已知:-SH的性质与-OH相似。
物质 一定条件下形成聚合物的结构简式为 ▲ 。
一定条件下形成聚合物的结构简式为 ▲ 。
【答案】
⑴硝基、羧基
⑵加成,保护碳碳双键,防止被酸性KMnO4氧化
⑶ BrCH2CH=CHCH2Br+2NaOH HOCH2CH=CHCH2OH+2NaBr
HOCH2CH=CHCH2OH+2NaBr
⑷5
⑸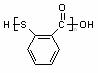
【解析】
(1)反应①的产物
 中含硫醚键、硝基、羧基。
中含硫醚键、硝基、羧基。
(2)反应③的类型是加成反应,反应⑤的目的是保护碳碳双键,防止被酸性KMnO4氧化
⑶ BrCH2CH=CHCH2Br+2NaOH HOCH2CH=CHCH2OH+2NaBr
HOCH2CH=CHCH2OH+2NaBr
(4)物质B的同分异构体有多种,其中既含有羟基,又含有醛基的同分异构体有:CH3CH2CH(OH)CHO、CH3CH(OH)CH2CHO、CH2(OH)CH2CH2CHO、CH3C(CHO)(OH)CH3、CH3CH(CHO)CH2OH。
⑸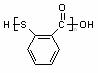


 孟建平小学滚动测试系列答案
孟建平小学滚动测试系列答案科目:高中化学 来源: 题型:
有机物A的结构简式为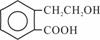 ,可通过它用不同化学反应分别制得B、C和D 三种物质。
,可通过它用不同化学反应分别制得B、C和D 三种物质。
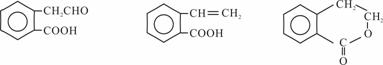
B C D
(1)B中的含氧官能团名称是 ;A→C的反应类型是 。
(2)由A生成B的化学方程式是 。
(3)C在一定条件下发生加聚反应的化学方程式是 。
(4)C的同分异构体中,有多种反式结构,写出其一种的结构简式 。
(5)D在酸性条件下水解的化学方程式是 。
查看答案和解析>>
科目:高中化学 来源: 题型:
下列各组溶液中,用括号内的试剂及物质间相互反应不能鉴别的一组是( )
A.Ba(OH)2、KSCN、NaCl、Mg(NO3)2(FeCl3溶液)
B.NaNO3、NaHCO3、(NH4)2SO3、Na2SiO3(H2SO4溶液)
C.NH4Br、K2CO3、NaI、CaCl2(AgNO3溶液)
D.(NH4)3PO4、NaBr、CuSO4、AlCl3(KOH溶液)
查看答案和解析>>
科目:高中化学 来源: 题型:
要检验某溴乙烷中的溴元素,正确的实验方法是
A.加入氯水,观察有无红棕色液体生成
B.加入NaOH溶液共热,滴入AgNO3溶液,再加入稀盐酸呈酸性,观察有无淡黄色沉淀生成
C.加入NaOH溶液共热,然后加入稀硝酸呈酸性,再滴入AgNO3溶液,观察有无淡黄色沉淀生成
D.加入AgNO3溶液,观察有无浅黄色沉淀
查看答案和解析>>
科目:高中化学 来源: 题型:
膳食纤维具有的突出保健功能,近年来受到人们的普遍关注,被世界卫生组织称为人体的“第七营养素”。木质素是一种非糖类膳食纤维,其单体之一是芥子醇,结构如下图所示。下列有关芥子醇的说法正确的是
A.芥子醇的分子式为C11H12O4,属于芳香族化合物
B.芥子醇分子中所有碳原子可能在同一平面上
C.芥子醇分子中含9种不同化学环境的H原子
D.1mol芥子醇能与足量溴水反应消耗1molBr2
查看答案和解析>>
科目:高中化学 来源: 题型:
在H2与Cl2生成HCl的反应中,已知断裂1 mol氢氢键吸收的能量为akJ,断裂1 mol氯氯键吸收的能量为bkJ,形成1 mol氢氯键放出的能量为ckJ,则生成1 molHCl放出的能量为( )
A.(c-a-b)kJ B.(a+b-c)kJ C.(2c-a-b)kJ D.(2c-a-b)/2kJ
查看答案和解析>>
科目:高中化学 来源: 题型:
阿伏加德罗常数为NA,下列说法正确的是 ( )
 A.1 mol 硫酸钾中阴离子所带电荷数为NA
A.1 mol 硫酸钾中阴离子所带电荷数为NA
B.乙烯和环丙烷以任意比混合气体28 g,含有4 NA个氢原子
 C.将0.1 mol氯化铁溶于1 L水中,所得溶液含Fe3+数为0.1 NA
C.将0.1 mol氯化铁溶于1 L水中,所得溶液含Fe3+数为0.1 NA
D.标准状况下,22.4 L氯气与足量氢氧化钠溶液反应转移的电子数为2 NA
查看答案和解析>>
科目:高中化学 来源: 题型:
下表列出了①~⑩十种元素在周期表中的位置:
| 族 周期 | ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | 0 |
| 2 | ① | ② | ||||||
| 3 | ③ | ④ | ⑤ | ⑥ | ⑦ | ⑧ | ⑩ | |
| 4 | ⑨ |
⑴上述①~⑩十种元素中(用元素符号填空):
构成有机物的主要元素是 ,构成岩石与许多矿物的基本元素是 ,
化学性质最不活泼的元素 ,气态氢化物的水溶液呈碱性的元素 。
⑵上述①~⑨元素的最高价氧化物对应的水化物中:
碱性最强的物质的电子式为 ,
酸性最强的物质的化学式为 。
⑶若以元素④和⑤的单质为电极,与元素③的最高价氧化物对应的水化物的水溶液组成原电池,则④的单质在此原电池中作 极(填“正”或“负”)
⑷元素⑦的某氧化物为有刺激性气味的无色气体,其氢化物为有臭鸡蛋气味的无色气体。若这两种气体混合,会生成一种淡黄色粉末。此反应化学方程式为 。若此反应中氧化产物的质量为3.2g,则反应中转移的电子数为 (填数值)。
⑸元素⑧和元素⑨两者核电荷数之差是 ,这两种元素中非金属性较弱的元素是 (填元素名称),能说明这两种元素的非金属性强弱的实验事实是(用离子方程式表示)
。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com