
���� ��1�������¶ȡ�������䣬�ٳ���PCl5��g����n������ѹǿ�����ѹǿ��ƽ���ƶ���Ӱ�������
��2�����º��������£��ٳ���HI��g�����൱��ѹǿ�����2HI��g��?I2��g��+H2��g��ǰ������ϵ��������ص��жϽ��
��3�����º��ݣ��ٳ���N2O4��g����ѹǿ����ƽ�������ƶ����Դ������
��� �⣺��1�������¶ȡ�������䣬�ٳ���PCl5��g����n������ѹǿ���÷�ӦΪ�����������ķ�Ӧ��������ѹǿƽ�������ƶ���PCl5��g����ת���ʼ�С��
�ʴ�Ϊ���淴Ӧ����С��
��2�����º��������£��ٳ���HI��g����ѹǿ����2HI��g��?I2��g��+H2��g��ǰ������ϵ������ȣ�ѹǿ��Ӱ��ƽ���ƶ����ﵽƽ���HI�ķֽ��ʲ��䣻
�ʴ�Ϊ�����ƶ������䣻
��3�����º��ݣ���ƽ����ٳ���N2O4���壬�൱��ԭƽ����ϵ����ѹǿ��ƽ�������ƶ�������ƽ���NO2��g����ת��������
�ʴ�Ϊ���淴Ӧ������
���� ���⿼�黯ѧƽ���ƶ���Ϊ��Ƶ���㣬�����������ʱ���ʵ�����ѹǿ�Ĺ�ϵΪ���Ĺؼ������ط�����Ӧ�������Ŀ��飬ע��ѹǿ��ƽ���ƶ���Ӱ�죬��Ŀ�ѶȲ���


 �ǻ�С��ϰϵ�д�
�ǻ�С��ϰϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ������

�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ���ѡ��
| �� | �� | |
| �� | �� | �� |
| A�� | ԭ�Ӱ뾶���주������ | |
| B�� | �����ԣ��ף��� | |
| C�� | ���������ˮ������ԣ����������� | |
| D�� | �������������ף��� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | NaOH��NaCl | B�� | C��CO2 | C�� | Fe2O3��Fe | D�� | NaHCO3��Na2CO3 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
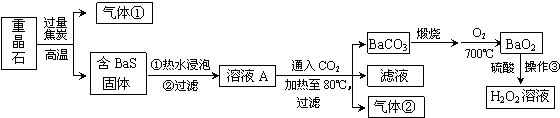
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | �ۢ� | B�� | �٢ڢ� | C�� | �ڢ� | D�� | �ܢݢ� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
| �¶� | 250��600��1000��2000�� |
| ��Ҫ�ɷ� | Fe2O3 Fe3O4 FeO Fe |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ���ѡ��
| A�� | NaClO��Һ | B�� | ������ˮ | C�� | �������� | D�� | ϡH2SO4 |
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com