
【题目】某化学兴趣小组为探究铜跟浓硫酸的反应,用如图装置进行有关实验。请回答:
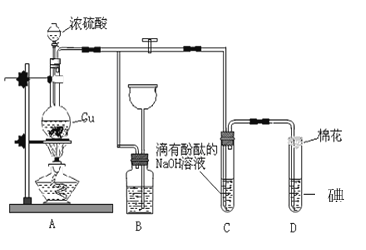
(1)装置A中发生的化学反应的化学方程式: _________________________________。
(2)装置B 的作用是__________________,B中广口瓶内应盛放的液体是_________(填序号)
①水 ②澄清石灰水
③Na2CO3溶液 ④饱和的NaHSO3 溶液
(3)装置C和D 中产生的现象相同,但原因却不同。C中反应的方程式:_______________________________________,而D 中则是由于SO2 具有_______性,D中反应的方程式:________________________。
(4)实验中,0.1molCu与含0.2mol硫酸的溶液反应后,铜和硫酸都有剩余。 可以证明有余酸的实验方案是___________
A.可再加入锌粒 B.可再加入氯化钡溶液
C.再加入银粉 D.再滴入碳酸氢钠溶液
【答案】Cu + 2H2SO4 ![]() CuSO4 + SO2 + 2H2O 贮存多余的气体 ④ NaOH + SO2 → NaHSO3 还原 SO2 + I2 + 2H2O → H2SO4 + 2HI A D
CuSO4 + SO2 + 2H2O 贮存多余的气体 ④ NaOH + SO2 → NaHSO3 还原 SO2 + I2 + 2H2O → H2SO4 + 2HI A D
【解析】
浓硫酸具有强氧化性,在加热条件下与铜发生氧化还原反应: ![]() ,反应生成的二氧化硫具有酸性和还原性,可用排饱和亚硫酸氢钠溶液收集,具有漂白性,可使品红溶液褪色,随着反应的进行,硫酸浓度不断降低,稀硫酸与铜不反应。
,反应生成的二氧化硫具有酸性和还原性,可用排饱和亚硫酸氢钠溶液收集,具有漂白性,可使品红溶液褪色,随着反应的进行,硫酸浓度不断降低,稀硫酸与铜不反应。
(1)浓硫酸具有强氧化性,在加热条件下与铜发生氧化还原反应生成硫酸铜、二氧化硫和水,Cu + 2H2SO4 ![]() CuSO4 + SO2 + 2H2O;
CuSO4 + SO2 + 2H2O;
(2)装置B的作用是贮存多余气体,二氧化硫易溶于水,具有酸性和还原性,可与酸性高锰酸钾、亚硫酸钠溶液反应,难溶于水饱和的NaHSO3溶液,可用排饱和NaHSO3溶液收集,;
(3)二氧化硫溶液具有酸性,可与NaOH溶液反应,发生: ![]() ,则滴加酚酞的氢氧化钠溶液褪色,具有漂白性,可使品红溶液褪色,;
,则滴加酚酞的氢氧化钠溶液褪色,具有漂白性,可使品红溶液褪色,;
(4)证明酸有剩余,只需证明有多余的氢离子即可,故可加入活泼金属或者碳酸盐,答案选AD。


科目:高中化学 来源: 题型:
【题目】A、B、C代表3种元素。请填空:
(1)A的原子的3p轨道上只有1个电子的自旋方向与其他电子的自旋方向相反,写出该原子价电子的轨道表示式:_______________________________,核外电子运动状态有_______种。
(2)B是原子序数为35的元素,其原子中有___________个电子层,有_________个能级。
(3)C元素基态原子的M层全充满,N层没有成对电子,只有一个未成对电子,元C素基态原子的电子排布式为_________________,其单质在一定条件下能与浓硫酸反应,试写出该反应方程式:____________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】X、Y、Z、W、R为五种短周期主族元素,Y、Z、W是原子序数递增的同周期相邻元素,且最外层电子数之和为15;X比Y核外少一个电子层;R的质子数是X、Y、Z、W四种元素质子数之和的![]() .下列说法正确的是( )
.下列说法正确的是( )
A. 简单离子半径:![]()
B. X与Y形成的二元化合物常温下一定为气态
C. W和R形成的化合物是离子化合物
D. Y与W、Z与W形成的二元化合物都是大气污染物
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】一定温度下,固定体积的密闭容器中发生反应M(g)+N(g)![]() 2W(g),能说明该反应一定达到平衡的是( )
2W(g),能说明该反应一定达到平衡的是( )
A.v(W)消耗=v(W)生成B.v正=v逆=0
C.容器内气体总质量不变D.n(M)∶n(N)∶n(W)=1∶1∶2
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】辉钼矿的主要成分是MoS2(Mo呈+4价),含少量SiO2以及Re的化合物等杂质。由辉钼矿可制得金属缓蚀剂钼酸钠晶体(Na2MoO4·10H2O)、催化剂Mo2C和氧化剂KReO4,其主要流程如下:

(1)焙烧辉钼矿时发生的反应及反应开始的温度(T)与真空度的关系如下图所示:(真空度P/P0表示反应时的压强与标准大气压之比)

为获得碳化钼,在真空度为0.5的条件下,适宜的反应温度应控制___________。
(2)焙烧时,生成Mo2C的反应中被还原的元素有___________(填元素符号);水洗烧结物时,洗去的物质除Na2S、Na2CO3之外,还有___________。
(3)用 NaClO2氧化MoS2时,MoS2转化为MoO42-和SO42-,写出该反应的离子方程式___________。
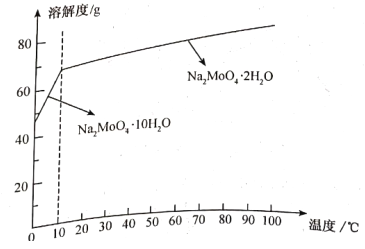
(4)已知钼酸钠的溶解度曲线如下图,获得Na2MoO4·10H2O的操作A为___________、___________、过滤。
(5)生成KReO4晶体的化学方程式为___________;加入KCl时,同时加入乙醇的作用是___________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】形成酸雨的原理之一可表示如下:

请回答下列问题:
(1)未污染的雨水的pH一般小于7大于5.6,这是由于溶解了___的缘故;酸雨的pH小于5.6,主要含有硫酸、___和一些有机酸等。
(2)图中三个反应不属于氧化还原反应的是___(填标号);写出反应②的化学方程式___。
(3)某研究性学习小组取来雨水做水样进行测定,随时间的推移雨水样品的pH值会变小,主要原因是为___(用化学方程式表示)。
(4)你认为减少酸雨产生的途径可采取的措施是____。(选填字母编号)
①少用煤做燃料 ②把工厂的烟囱造高 ③燃料脱硫 ④在已酸化的土壤中加石灰 ⑤开发新能源
A.①②③ B.②③④⑤ C.①③⑤ D.①③④⑤
(5)从保护环境的角度出发,一些工厂采用“钙基固硫法”,即在含硫的煤中混入生石灰后燃烧,大部分SO2最终将转化为_____。
(6)汽车尾气中的CO,NO排放也是城市空气的污染物,治理的方法之一是在汽车的排气管上装一个“催化转化器”,使CO与NO反应,生成两种无毒气体,其中之一是N2。写出NO与CO反应的化学方程式___,此反应的缺点是在一定程度上提高空气的酸度,其原因是___。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列事实不能用勒夏特列原理(平衡移动原理)解释的是
①铁在潮湿的空气中容易生锈
②二氧化氮与四氧化氮的平衡体系,加压缩小体积后颜色加深
③实验室可用排饱和食盐水的方法收集氯气
④钠与氯化钾共融制备钾 Na(l)+KCl(l)![]() K(g)+NaCl(l)
K(g)+NaCl(l)
⑤开启啤酒瓶后,瓶中马上泛起大量泡沫
A. ③④ B. ①② C. ①⑤ D. ①②⑤
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(4分)水的电离平衡曲线如图所示:
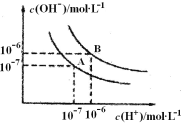
(1)A点表示25℃时水电离平衡时离子的浓度,当温度升高到100℃时,水的电离平衡状态变到B点,则100℃时水的离子积为_____________。
(2) 100℃时,若10体积的某强酸溶液与l体积的某强碱溶液混合后溶液呈中性,则混合之前,该强酸的pHa与强碱的pHb之间应满足的关系是______________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】氯碱工厂生产的氯气和氢气可以进一步用于生产盐酸,主要过程如下:

(1)其中关键的一步为氯气和氢气在燃烧管口燃烧生成HCl,氯气有毒,应采取的措施是____。合成盐酸厂要求合成气中的HCl的含量要大于97%,试用最简便的方法进行分析是否含量大于97%____。
(2)氯碱工厂生产的氯气和氢氧化钠溶液可以用于制取“84消毒液”,反应的化学方程式为__。
(3)某同学欲证明盐酸与氯化氢气体性质不同,他分别向A、B、C三支洁净试管中各放入一片干燥的蓝色石蕊试纸,然后往A试管内加入盐酸,试纸显___色,往B试管中通入干燥的氯化氢气体,试纸显___色.最后向C试管中加入物质___(填化学式),他之所以加入这种物质的理由是____。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com