
在一定条件下,Na2CO3溶液中存在CO32-+H2O HCO3-+OH-平衡。下列说法不正确的是( )
HCO3-+OH-平衡。下列说法不正确的是( )
A.稀释溶液, 减小 减小 | B.加入NaOH固体, 减小 减小 |
| C.升高温度,平衡常数增大 | D.通入CO2,溶液pH减小 |
A
解析试题分析:A.稀释后C(OH-)、C(CO32-)都减小,但平衡正向移动使的C(OH-)又有所增加,C(CO32-)又有所减小。因此C(OH-)减小的少,C(CO32-)减少的多,故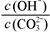 增大。错误,符合题意。B.加入NaOH固体,平衡逆向移动,C(HCO3-)减小,C(CO32-)增大,所以
增大。错误,符合题意。B.加入NaOH固体,平衡逆向移动,C(HCO3-)减小,C(CO32-)增大,所以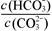 减小。正确,不符合题意。C. 升高温度,促进盐的水解,平衡向正反应方向移动,平衡常数增大。正确,不符合题意。D.通入CO2,发生反应:CO2+Na2CO3+H2O=2NaHCO3,平衡逆向移动,溶液的C(OH-)减小,溶液pH减小 。正确,不符合题意。
减小。正确,不符合题意。C. 升高温度,促进盐的水解,平衡向正反应方向移动,平衡常数增大。正确,不符合题意。D.通入CO2,发生反应:CO2+Na2CO3+H2O=2NaHCO3,平衡逆向移动,溶液的C(OH-)减小,溶液pH减小 。正确,不符合题意。
考点:考查外界条件对盐水解平衡及对溶液中离子浓度的大小的影响。


科目:高中化学 来源: 题型:单选题
常温下,pH=11的氨水和pH=1的盐酸等体积混合(混合溶液体积为两溶液体积之和),恰好完全反应,则下列说法错误的是
| A.氨水的浓度大于盐酸的浓度 |
| B.原氨水中有1%的含氮微粒为NH4+ |
| C.氨水中水电离出的c(H+)是盐酸中水电离出的c(H+)的100倍 |
| D.混合溶液中c(NH4+)+c(NH3·H2O)+c(NH3)=5×10-4mol/L |
查看答案和解析>>
科目:高中化学 来源: 题型:单选题
今有室温下四种溶液,有关叙述不正确的是
| | ① | ② | ③ | ④ |
| pH | 11 | 11 | 3 | 3 |
| 溶液 | 氨水 | 氢氧化钠溶液 | 醋酸 | 盐酸 |
查看答案和解析>>
科目:高中化学 来源: 题型:单选题
体积相同浓度均为0.1mol·L-1的NaOH溶液、氨水,分别稀释m倍、n倍,溶液的pH都变成9,则m和n的关系正确的是
| A.m>n | B.m=n | C.m<n | D.不能确定 |
查看答案和解析>>
科目:高中化学 来源: 题型:单选题
下列有关沉淀溶解平衡的说法正确的是
A.Ksp(AB2)小于Ksp(CD),则AB2的溶解度小于CD的溶解度
B.在AgCl的沉淀溶解平衡体系中,加入蒸馏水,AgCl的Ksp增大
C.在AgI的沉淀溶解平衡体系中,加入K2S固体,AgI沉淀可转化为Ag2S沉淀
D.在CaCO3的沉淀溶解平衡体系中,通入CO2气体,溶解平衡不移动
查看答案和解析>>
科目:高中化学 来源: 题型:单选题
已知水的电离方程式:H2O  H+ + OH-。下列叙述中,正确的是
H+ + OH-。下列叙述中,正确的是
| A.升高温度,KW增大,pH不变 |
| B.向水中加入氨水,平衡向逆反应方向移动,c(OH-)降低 |
| C.向水中加入少量硫酸,c(H+)增大,KW不变 |
| D.向水中加入少量固体CH3COONa,平衡向逆反应方向移动,c(H+)降低 |
查看答案和解析>>
科目:高中化学 来源: 题型:单选题
化学用语是学习化学的重要工具,下列用来表示物质变化的化学用语中,正确的是( )
| A.用惰性电极电解饱和食盐水:2Cl-+ 2H+=H2↑+ Cl2↑ |
| B.碱性氢氧燃料电池的正极反应式:O2+2H2O+4e-=4OH- |
| C.钢铁发生电化学腐蚀的正极反应式:Fe-2e-=Fe2+ |
| D.碳酸钠溶液呈碱性:CO32-+2H2O=H2CO3+2OH- |
查看答案和解析>>
科目:高中化学 来源: 题型:单选题
用0.10 mol·L-1的盐酸滴定0.10 mol·L-1的氨水,滴定过程中不可能出现的结果是
| A.c(NH4+) > c(Cl-),c(OH-) > c(H+) |
| B.c(Cl-) > c(NH4+),c(OH-) > c(H+) |
| C.c(NH4+) = c(Cl-),c(OH-) = c(H+) |
| D.c(Cl-) > c(NH4+),c(H+) > c(OH-) |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com