
![]()
有机产物半缩醛对氧化剂及还原剂很稳定,但在稀酸溶液中易水解变为原来的醛:
![]()
现欲将柠檬醛分子中的C=C双键加氢还原,
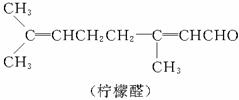
采用如下合成路线:
![]()
试写出B的结构式和C的分子式:B________________,C_________________。
 名校课堂系列答案
名校课堂系列答案科目:高中化学 来源: 题型:
 碳是化合物种类最多的元素,其单质及化合物是人类生产生活的主要能源物质.
碳是化合物种类最多的元素,其单质及化合物是人类生产生活的主要能源物质.查看答案和解析>>
科目:高中化学 来源: 题型:
| 1 |
| 2 |
| 1 |
| 2 |
| 1 |
| 2 |
| 1 |
| 2 |
| A、-126.89 kJ?mol?? |
| B、-324.4 kJ?mol?? |
| C、-30.56 kJ?mol?? |
| D、题中数据不足,无法计算 |
查看答案和解析>>
科目:高中化学 来源: 题型:阅读理解
| 1 |
| 2 |
| 1 |
| 2 |
查看答案和解析>>
科目:高中化学 来源: 题型:
(2)化学反应2NO(g)+2CO(g)![]() N2(g)+2CO2(g),在298 K、100 kPa下:ΔH=-113.0 kJ·mol-1 ΔS=-145.3 J·mol-1·K-1,反应在常温下_______(填“能”或“不能”)自发进行。?
N2(g)+2CO2(g),在298 K、100 kPa下:ΔH=-113.0 kJ·mol-1 ΔS=-145.3 J·mol-1·K-1,反应在常温下_______(填“能”或“不能”)自发进行。?
(3)求反应2HCl(g)![]() H2(g)+Cl2(g)的标准熵变。已知:HCl(g)的S=186.6 J·K-1·mol-1,H2(g)的S=130 J·K-1·mol-1,Cl2(g)的S=223 J·K-1·mol-1,ΔS=______________。?
H2(g)+Cl2(g)的标准熵变。已知:HCl(g)的S=186.6 J·K-1·mol-1,H2(g)的S=130 J·K-1·mol-1,Cl2(g)的S=223 J·K-1·mol-1,ΔS=______________。?
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com